XiaoMi-AI文件搜索系统
World File Search SystemmiRNA/CXCR4信号轴损害糖尿病关键肢体缺血中的单伏和血管生成
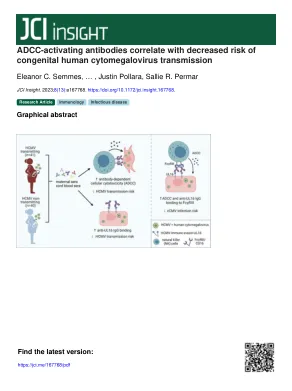
引言人类巨细胞病毒(HCMV)是全球最常见的垂直传播感染,与死产,神经发育障碍,感觉性听力损失和儿童白血病有关(1,2)。全世界有超过80%的生殖年龄妇女是HCMV血清阳性的,先天性传播可能会在原发性或非主要HCMV感染后发生,其中可能包括重新感染因病毒潜伏期的新菌株或重新激活(3)。尽管存在这些疾病风险和先天性HCMV(CCMV)感染的普遍性,但我们缺乏有效的治疗剂和疫苗来防止HCMV转移。中和针对HCMV进入包膜糖蛋白(例如,糖蛋白B [GB]和五聚糖复合物)的抗体和T细胞反应一直是迄今为止疫苗发育中的主要靶标,但是这些疫苗只能限制为适度的效率(4)。此外,一些研究发现,母体中和抗体滴度与CCMV感染的风险降低无关(5,6)。我们最近还报道说,针对多种HCMV菌株的中和抗体滴度在HCMV传输妊娠中较高,并且与保护无关(7)。Mater-NAL用HCMV高免疫球蛋白(HCMV-HIG),这是HCMV - 异位阳性供体的IgG的合并多克隆制备,怀孕期间初次感染后也无法防止2个随机临床试验中的结合(8,9)。因此,迫切需要对预防CCMV传播的母体抗体反应的改进理解,以指导疫苗和免疫疗法的发展(10,11)。
鸡感染性贫血病毒:家禽行业免疫抑制疾病的病因
由于非洲鸡感染性贫血的新兴状况,尤其是埃及及其与传染性囊泡疾病的相似之处,因此有必要调查这种疾病。本评论文章的目标是提请人们注意鸡肉贫血病毒(CAV)如何影响家禽行业以及疫苗接种如何帮助控制疾病。CAV是一种免疫抑制疾病,因此对家禽行业造成了巨大的经济损失。它是由鸡感染性贫血病毒引起的,这是陀螺病毒家族的成员Annelloviridae。红细胞和髓样系列的祖细胞是受影响的主要细胞。这种疾病会导致鸡的临床和亚临床疾病,并水平和垂直传播。鸡充当主要的天然宿主。由于骨髓中的红细胞细胞破坏和皮质胸腺细胞的还原,骑士在幼鸡中产生严重的贫血和免疫力。免疫差异是由皮质胸腺细胞耗竭引起的,导致并发感染和疫苗接种衰竭增强。CAV诊断取决于临床体征和总病变,因此可以使用各种血清学和分子技术进行确定性诊断。最准确的CAV诊断方法是PCR。该疾病目前没有特定的治疗;但是,适当的疾病控制和管理技术,繁殖者免疫计划以及其他措施可以帮助制止CAV疫情。总而言之,通过免疫母鸡并改善DNA和重组疫苗策略,可以减少骑士对家禽鸟类的经济影响。
语言遵循一种独特的基因组外进化模式
语言是人类最特殊但又最多样化的行为之一,它受到基因组和基因组外进化的影响。这些进化模式之间共享的方法和模型极大地促进了我们对语言的理解,并启发了语言进化的普遍理论。然而,语言的基因组外进化(即语言进化)仅部分映射到其他进化形式,这阻碍了进步。通过将其与真核生物的生物进化和技术的文化进化(这是最容易理解的模型)进行对比,我们发现语言进化的特殊之处在于它产生了一种静止的动态而不是稳定的解决方案,并且这种动态允许使用语言变化进行社会分化,同时保持其全球适应性。此外,语言进化与技术进化的不同之处在于需要垂直传播,从而允许重建系统发育;它与真核生物进化的不同之处在于它放弃了基因型与表型的区别,允许有意识和有偏见的变化。认识到这些差异将改善我们的实证工具,并为分析当语言在原始人类谱系中出现时语言、文化和生物进化如何相互作用开辟新途径。重要的是,我们的框架将有助于应对前所未有的科学和伦理挑战,这些挑战目前源于快速的文化进化对语言的影响,最紧迫的是语言障碍的干预性临床工具、技术对语言的潜在表观遗传影响、人工智能和语言传播者,以及全球语言多样性和身份的丧失。除了语言之外,这里所做的区分还可以识别其他形式的生物和文化进化的变化,为实证研究开发新的视角。
语言遵循一种独特的基因组外进化模式
语言是人类最特殊但又最多样化的行为之一,它受到基因组和基因组外进化的影响。这些进化模式之间共享的方法和模型极大地促进了我们对语言的理解,并启发了语言进化的普遍理论。然而,语言的基因组外进化(即语言进化)仅部分映射到其他形式的进化,这阻碍了进步。通过将其与真核生物的生物进化和技术的文化进化(这是最容易理解的模型)进行对比,我们发现语言进化的特殊之处在于它产生了一种静止的动态而不是稳定的解决方案,并且这种动态允许使用语言变化进行社会分化,同时保持其全球适应性。此外,语言进化与技术进化的不同之处在于它需要垂直传播,从而允许重建系统发育;它与真核生物进化的不同之处在于它放弃了基因型与表型的区别,允许有意识和有偏见的变化。认识到这些差异将改善我们的实证工具,并为分析当语言在原始人类谱系中出现时语言、文化和生物进化如何相互作用开辟新途径。重要的是,我们的框架将有助于应对前所未有的科学和伦理挑战,这些挑战目前源于快速的文化进化如何影响语言,最紧迫的是语言障碍的干预性临床工具、技术对语言、人工智能和语言传播者的潜在表观遗传影响以及全球语言多样性和身份的丧失。除了语言之外,这里所做的区分还可以识别其他形式的生物和文化进化中的差异,为实证研究开发新的视角。
将硅噬菌体变成体内噬菌体:
crass样噬菌体最初是从涉及元基因组测序的研究和来自多个个体(Crass-cr oss asbly)的读取的研究中得出的高度丰富和肠道微生物组的普遍成员。最近,已经确定了粘膜类细菌的骨状噬菌体感染细菌。最令人兴趣的面孔样噬菌体之一是它们在实验室和肠道中持续数量高的能力,而不会显着影响其细菌宿主的丰富性。在这里,我们重述了迄今为止,从2014年的硅硅发现以及随后鉴定唯一基因组特征的含量噬菌体,到Crass001的第一个隔离以及阐明由Vivo In Vivo的Phage-Host对研究引起的各种生物学特征的首次分离。在相对较短的时间内收集了大量信息,但是很明显,类似骨状的噬菌体研究仍处于起步阶段。未来的研究在于进一步的体内工作,与噬菌体 - 宿主对一起工作,再加上从较大的群体中分离出进一步的crass样噬菌体。引言泥泞的噬菌体是人类肠道微生物组的有趣成员。它们既多产又广泛,占肠道病毒基因组的86%以上。(Yutin等,2021)在来自全球各地的粪便中都发现了它们,并且在从婴儿到老年人的所有年龄段中都发现了它们(Edwards等,2019)。也已显示它们被转移并稳定地植入虽然crassphages很少是新生微生物组的组成部分,但它们在生命的第一年就变得越来越普遍。已经表明,垂直传播会导致这种初始定植(McCann等,2018; Siranosian等,2020)。
语言遵循一种独特的基因组进化模式
作为最具体,最多样化的人类行为之一,语言是基因组和基因组进化的影响。共享这些进化方式之间的共享方法和模型显着提高了我们对语言的理解,并激发了其进化的广义理论。的进步受到了阻碍,这是语言的典型演变,即语言进化,仅部分映射到其他形式的进化。将其与真核生物的生物学演变和技术的文化演变作为最佳理解的模型进行了对比,我们表明语言演化是特殊的,它通过产生固定的动态而不是稳定的解决方案而不是稳定的解决方案,并且这种动态允许语言变化用于社会差异,同时保持其全球适应性。语言进化与技术进化不同,通过需要垂直传播,允许重建系统发育。它与真核生物生物学的进化不同,它通过预言基因型与表型的区别,允许故意和偏见的变化。认识到这些差异将改善我们的经验工具,并开放新的途径,以分析当语言在人类谱系中出现时语言,文化和生物学进化如何相互作用。除了语言之外,这里提出的区别允许识别其他形式的生物和文化进化的变化,从而发展了实证研究的新观点。重要的是,我们的框架将有助于应对前所未有的科学和道德挑战,这些挑战目前是由于文化进化的迅速影响而引起的,最急需的语言疾病临床工具,技术对语言对语言的潜在表观遗传作用,人工英特尔语,人工领域,人工领域以及语言交流和全球语言损失的语言损失和语言学多样性和身份。
共生细菌和真菌在滞育中增殖,并可能在孤独的蜜蜂中增强冬季的生存
宿主 - 微生物相互作用是包括蜜蜂在内的许多宏观生物的发展和适应性的基础。尽管许多社会蜜蜂受益于垂直传播的肠道细菌,但当前的数据表明,孤立的蜜蜂构成了蜜蜂中绝大多数物种多样性,但缺乏高度专业的肠道微生物组。在这里,我们研究了整个野生蜜蜂bonthophora bomboides Standfordiana的整个生命周期中细菌和真菌的成分和丰度。与期望相反,未成熟的蜜蜂阶段保持了一个独特的核心微生物组,该核心体由静脉细菌属(链霉菌,诺卡氏菌)和真菌Moniliella spathulata组成。休眠(尿布)幼虫蜜蜂占据了最丰富,最独特的细菌和真菌,分别达到其初始拷贝数的33和52倍。我们测试了关于尿布蜜蜂的微生物功能的两个自适应假设。首先,使用孤立的细菌和真菌,我们发现来自育雏细胞的链霉菌抑制了多种致病性丝状真菌的生长,这表明当蜜蜂面对高病原体压力时,在越冬期间在病原体保护中起作用。第二,糖酒精成分随着真菌丰度的重大变化而变化,这表明与蜜蜂冷耐受性或越冬的生物学有联系。我们发现,炸弹抗体有一个保守的核心微生物组,可以通过幼虫的发育和滞育提供关键的适应性优势,这提出了一个问题,即如何维持和忠实地传播这种微生物组。我们的结果表明,关注成熟或活跃的昆虫发育阶段的微生物组可能会忽略宿主休眠期间特定阶段的共生体和微生物适应性的贡献。
人工智能在抗击新冠肺炎疫情中的作用
过去二十年爆发了许多病毒性疾病,如基孔肯雅热、埃博拉、寨卡、尼帕、H7N9 禽流感、H1N1、SARS 和 MERS。这十年来,世界因一场新的疾病爆发而醒来。2019 年 12 月,中国湖北省武汉市爆发了一种新型冠状病毒。大多数最初确诊的患者都追溯到屠宰和销售活体动物的“海鲜市场”。该市场可能扮演了一个放大热点的角色,病毒从这里传播到中国其他地区,随后在很短的时间内传播到 213 个国家和地区。世界卫生组织于 2020 年 2 月 11 日将此疾病命名为“COVID-19”,这是 2019 冠状病毒病的缩写。截至 2020 年 8 月 17 日,全球共报告确诊病例 2120 万例,死亡人数 761,000 人 [1] 。美国、印度、巴西和俄罗斯报告了最严重的 COVID-19 疫情,这些国家的病例数已超过中国的确诊病例数。世界卫生组织于 2020 年 1 月 30 日将当前爆发的 COVID-19 宣布为“国际关注的突发公共卫生事件”,并于 2020 年 3 月 11 日宣布为“大流行”。尽管严重急性呼吸综合征冠状病毒 2 (SARS-CoV-2;2.9%) 的死亡率远低于 SARS-CoV (9.6%) 和 MERS-CoV (34.4%),但 SARS-CoV-2 与其他冠状病毒相比的高传染性已成为全球关注的问题。研究发现,男性的 COVID-19 死亡率和易感性高于女性,这可能归因于吸烟等其他性别行为 [2] 。COVID-19 的死亡率随年龄梯度而变化,也受到潜在合并症的影响,换句话说,糖尿病、高血压、癌症、心血管疾病和慢性呼吸系统疾病等疾病 [3–5] 。未观察到 COVID-19 母婴垂直传播 [6] 。儿童易感染 COVID-19,但往往只表现出轻微症状 [7] 。
16个ixodes的深度测序ricinus ticks揭示了他们与内共生体的相互作用的见解
背景:ixodes ricinus tick是众多病原体的媒介,这些病原体呈现出严重的健康威胁。此外,它们具有垂直传播的共生体,其中一些与疾病有关。隔离和培养这些共生体的困难阻碍了我们对它们的生物学作用,引起疾病的潜力和传播方式的理解。为了扩展我们对与人类疾病有关的tick共生二氯乙醇中心核的理解,并在人类中与疾病有关,我们使用了16个成年女性tick虫进行了深入的测序。其中,八个是从沿海沙丘环境中收集的,另外八个是从荷兰的森林地区获得的。结果:通过采用下一代和第三代测序技术的组合,我们成功地重建了来自11个个体的线粒体M. M. helvetica的完整基因组,来自八个个体的Helvetica和来自所有tick的线粒体基因组。此外,我们可视化了Helvetica在tick器官和两个共生体的构造基因组代谢模型(GEM)中的位置,以研究其与生长相关的环境依赖性。我们的分析表明,线粒体和线粒体基因组之间存在很强的辅助性,表明频繁的母体传播。相比之下,helvetica和线粒体基因组之间不存在Cophyly,并在雌性的ini ricinus internis seminis中的存在,提高了helvetica的父亲传播的可能性。值得注意的是,除了rick a毒力基因外,发现Helvetica的遗传多样性非常低,在该基因中,在33nt-long重复的插入中的存在导致了显着的差异。但是,这种变化无法解释荷兰八个不同位置观察到的感染率的差异。结论:通过采用深层测序,可以直接从其宿主生物体中提取共生体的完整基因组和遗传数据变得可行。这种方法是一种强大的方法,可以使他们对其相互作用的新见解。我们的观察结果表明,R. helvetica的父亲传播是一种相对尚未开发的壁虱传播方式,需要通过实验研究进行验证。rick中鉴定出的遗传变异r。
涉及病毒载体的研究指南:黄病毒...
病毒载体研究指南:黄病毒载体 黄病毒(黄病毒科)是有包膜的正义单链 RNA 病毒,通常通过昆虫媒介在脊椎动物宿主之间传播。一些病毒也被发现在子宫内或通过母乳从母亲到后代进行垂直传播,尤其是寨卡病毒的性传播令人担忧。黄病毒基因组由一个长的开放阅读框组成,该阅读框编码结构蛋白和非结构蛋白。进入细胞质后,病毒 RNA 可以作为 mRNA 并翻译成一个长的多聚蛋白,该多聚蛋白被细胞和病毒蛋白酶切割成单个蛋白质。因此,基于黄病毒的病毒载体需要将异源基因插入病毒编码区框架内,并由蛋白酶切割位点连接。通过用目标异源基因替换结构蛋白基因来生成复制缺陷型载体。作为替代方案,可以在内部核糖体进入位点序列的帮助下将基因插入非编码区。黄病毒和黄病毒载体在脊椎动物和无脊椎动物细胞中复制到中等滴度(在某些情况下大于 1x10 8 颗粒形成单位/毫升)。脊椎动物细胞的感染通常是溶解性的,尽管需要几天到一周的时间才能识别出细胞病变效应。昆虫细胞的感染是持续性的。黄病毒复制发生在细胞质中,因此黄病毒载体适合在靶细胞中瞬时表达感兴趣的基因。潜在的健康危害人类感染黄病毒通常是亚临床的,但也可能表现为轻度至重度的流感样症状。严重病例可能导致脑炎、肝炎和出血热,具体取决于病毒和先前的免疫力。其他病毒与先天畸形有关,包括受感染母亲所生儿童的小头畸形。传播方式 野生型黄病毒通常通过昆虫媒介在脊椎动物宿主之间传播,包括蚊子和蜱虫,具体取决于病毒。除了寨卡病毒外,尚未记录到直接的人际传播,寨卡病毒与性传播有关。人类可以作为某些黄病毒(如登革热病毒、寨卡病毒和黄热病病毒)的扩增宿主,并可在蚊子叮咬后感染蚊子。