XiaoMi-AI文件搜索系统
World File Search System患者护理指南、常规医嘱和规程
这些协议由 KBEMS 州医疗顾问修订或编写,并作为 KBEMS 的一项服务提供。当它们被服务采用时,它们将成为服务医疗主管的常规命令。应该注意的是,虽然这套协议旨在尽可能包容所有服务,但并非所有医疗主管都希望认证所有员工来执行每项程序。例如,虽然服务的协议集可能包括外科环甲膜切开术协议和 Melker 经皮环甲膜切开术协议,但并非所有护理人员都可能由服务医疗主管认证执行这两项(或其中一项)。EMS 服务和服务医疗主管有责任确定哪些提供者有资格执行哪些程序,并维护该决定的培训和文档要求。应该普遍假设
氨甲环酸对创伤性脑损伤血肿进展的影响:一项随机对照试验
创伤性脑损伤 (TBI) 是孟加拉国乃至全世界发病和死亡的主要原因。进行性脑内血肿、脑水肿加重、颅内压升高和随后的脑缺血造成的继发性脑损伤是 TBI 后发病和死亡的主要原因。创伤后凝血病会加重继发性脑损伤,这种情况发生在脑损伤患者中,并与死亡和发病风险增加有关。抗纤溶药物氨甲环酸 (TXA) 可减少血肿扩大,并显示出改善的临床结果,同时也降低了死亡率和发病率。这是一项在达卡医学院和医院神经外科进行的随机对照试验 (RCT)。根据计算机生成的代码列表,纳入的患者被随机分配接受静脉注射氨甲环酸 (A 组) 或安慰剂 (B 组) 治疗 (每组 50 名患者),同时接受创伤性脑损伤的常规医疗管理。入院后48小时以脑部CT扫描测量挫伤扩大程度(血肿加血肿周围水肿)为主要观察指标。两次测量均计算挫伤和水肿体积(入院时和48小时后)。观察48小时后格拉斯哥昏迷评分(GCS)和7天后格拉斯哥预后评分(GOS)。本研究显示两组血肿体积均增加(p<0.05)。但A组血肿体积的增加明显少于对照组。A组和B组平均总出血扩大量分别为(1.5±1.1)ml和(4.6±1.9)ml。A组有02例(4.0%)患者需要手术,B组有11例(22.0%)患者需要手术。两组结果有显著差异(p=0.023)。因此,使用氨甲环酸与血肿体积进展较少有关。A 组的平均 GCS(48 小时后)、平均 GOS(7 天后)结果明显更好(p<0.001)。这项研究得出结论,氨甲环酸对严重创伤性脑损伤患者有益。氨甲环酸有助于减少脑内挫伤进展并改善 TBI 患者的临床结果。
45-胸转移性CMF IV(环磷酰胺甲氨蝶呤)取代| EVIQ
剂量修改的证据是有限的,EVIQ提出的建议仅作为指导。他们通常是保守的,重点是安全。任何剂量修改均应基于临床判断,以及个体患者的状况,包括但不限于治疗意图(治愈性与姑息治疗),抗癌治疗方案(单一对组合疗法与化学疗法与化学疗法与免疫疗法),癌症的生物学,癌症,大小,突变,转移酶的其他副作用,良好的效果,表现良好,效果和其他副作用,表现为其他。修改基于临床试验结果,产品信息,已发表的指南和参考委员会共识。降低剂量适用于每个单独剂量,除非另有说明,否则不适用于治疗周期的总天数或持续时间。非血液学等级基于不良事件的共同术语标准(CTCAE),除非另有说明。肾脏和肝剂量修饰已
Biphentin®(甲化苯甲酯盐酸盐)
需要进行全面治疗计划的需求是该综合症患者的ADHD总治疗计划的组成部分,其中可能包括其他措施(即心理学,教育和/或社会)。该综合征患者可能不会指出药物治疗。药物治疗不适用于表现出继发于环境因素和/或其他原发性精神疾病(包括精神病)的症状的患者。适当的教育安置在此诊断和社会心理干预的儿童和青少年中至关重要。单独的补救措施不足,开处方药物治疗的决定将取决于卫生专业人员对患者症状的慢性和严重程度的评估。
对高温超导薄膜的表面和保护性绝缘膜的研究
高表面特性。tc ba-y-cu-o和通过薄绝缘子过层钝化。Takashi Hirao,Kentaro Setsune和Kiyotaka W asa。中央重新建筑实验室,Matsushita Electric Industrial Co.,Ltd.,3-15,Yagumonakamachi,Moriguchi,Osaka,Osaka 570
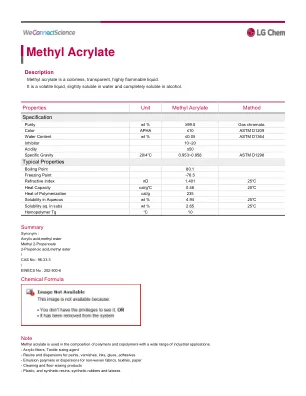
丙烯酸甲酯
本文包含的信息,包括但不限于数据,陈述和典型价值观,以真诚地给出。lg Chem不提供任何保证或保证,表示或暗示,(i)在本文中所述的结果将在结束条件下或(ii)在任何纳入LG化学材料,产品,建议或建议的设计的有效性或安全性下获得。此外,本文包含的任何信息均不得解释为具有法律约束力的一部分。尤其是,典型值应仅视为参考值,而不是结合最小值。每个用户都承担着自己确定LG Chem材料,产品,建议或建议其自身特定用途的适用性的全部责任。每个用户必须识别并执行所需的所有测试和分析,以确保其成品零件包含LG化学材料或产品将是安全且适合在最终使用条件下使用的。由于产品的质量提高,可以更改本文包含的数据。
使用鸡蛋绒毛膜膜膜的异种移植模型
背景:非转移性肌肉浸润性尿路上皮膀胱癌(MIBC)的预后较差,护理标准(SOC)包括基于新辅助顺铂的化学疗法(NAC)与膀胱切除术相结合。接受NAC的患者与单独的膀胱切除术相比,总体生存率的最多<10%。这个主要的临床问题强调了我们对抵抗机制的理解和对可靠的临床前模型的需求。鸡肉胚胎绒毛膜膜膜(CAM)代表了免疫功能低下的小鼠的快速,可扩展且具有成本效益的替代方法,用于在体内建立患者衍生的异种移植物(PDX)。cam- PDX利用易于获得的植入支架和富含血管的,免疫抑制的环境,用于植入PDX肿瘤和随后的功能研究。方法:我们使用CAM-PDX模型优化了原发性MIBC肿瘤的植入条件,并在基于顺铂的化学疗法反应之间进行了一致性,对患者的化学疗法反应与使用免疫组织化学标志物相结合的PDX肿瘤对PDX肿瘤进行了匹配。我们还使用肿瘤生长测量方法和对增殖标记物的免疫检测,KI-67测试了CAM-PDX上抗化疗的膀胱癌的精选激酶抑制剂反应。结果:我们的结果表明,在CAM上生长的原发性,耐NAC的MIBC肿瘤具有组织学特征 - 以及基于顺铂的基于顺铂的化学疗法耐药性,可在诊所观察到匹配的父母人类肿瘤标本。结论:我们的数据表明,基于顺铂的化学疗法抗性表型与原发性患者肿瘤和CAM-PDX模型之间的一致性。患者肿瘤标本成功地植入了CAM上,并显示出对双重EGFR和HER2抑制剂治疗的肿瘤生长大小和增殖的降低,但对CDK4/6或FGFR抑制没有明显的反应。此外,蛋白质组知情的激酶抑制剂在MIBC CAM-PDX模型上使用了新型治疗剂的快速体内测试的整合,从而为更复杂的细胞前小鼠PDX实验提供了更为有效的临床试验设计,旨在为具有有限治疗选择的患者提供最佳的精确药物。