XiaoMi-AI文件搜索系统
World File Search System基于AI的痴呆病因鉴别诊断多模式数据 抑郁症中食物奖励的期待钝了
Chonghua Xue 1 , 2 , ∗ , ∗ , Sahana S. Kowshik 1 , 3 1 † , Brigid C. Dwyer 6 † , Chad W. Farris 8 † Asim Z. Mian 6 † , Daniel L. Murman 10 † , Sarah A. O'Shea 11 † Setty 6 † , Juan E. Small 13 † , Arun Swaminan 14 † 3 ‡
对比增强超声检查的定量分析在良性和恶性骨盆肿瘤的鉴别诊断中的临床价值
是女性最常见的十大癌症之一(1)。其中,卵巢癌被认为是“沉默的杀手”,因为大多数患者的症状很少或在晚期阶段被诊断出(III和IV)(2,3)。因此,早期发现,诊断和治疗对于总体上对这种疾病和妇女健康的管理至关重要。传统的超声检查和多普勒超声检查在检查较小的病变方面的用途有限,改善恶性肿瘤的早期诊断对于增强治疗的功效至关重要。对比增强的超声检查(CEU)已被广泛应用于肝脏,甲状腺,乳腺癌和肾脏疾病的诊断中,由于其高敏感性和特异性,其肿瘤的诊断价值一直被一致识别(4-7)。然而,到目前为止,只有少数研究对骨盆肿瘤的鉴别诊断进行了定性或定量分析。此外,良性和恶性病变中有定量指数的交叉,每个指数缺乏均匀的标准(8,9)。定性分析也容易受到相当大的主观和操作差异的影响,这限制了其临床应用(10)。在这项研究中,对鉴定良性和恶性骨盆肿瘤病变的多个指标进行了全面的定量分析。总体而言,这项研究的发现有可能提高CEU的诊断准确性,并可以作为肿瘤临床管理的更可靠的参考。我们按照明星报告清单介绍本文(可在https:// qims。amegroups.com/article/view/10.21037/qims-23-582/rc)。
定量能谱CT在产生醛固酮腺瘤和生产皮质醇的腺瘤的鉴别诊断中
APA和CPA的策略是不同的。在手术治疗方面,CPA是患病一侧的肾小球切除术,而APA在患病方面是完全肾上腺切除术,因此需要准确的鉴别诊断来指导临床治疗计划(2)。 但是,患有APA或CPA的患者显示出一些相似的临床症状和大量的常规成像表现重叠,这使分化很难。 尽管肾上腺静脉抽样(AVS)的经皮插管是APA诊断的“黄金标准”,但该程序的难度,成本和侵入性限制了其在临床实践中的广泛使用。 在传统的成像检查中,评估主要基于肿瘤的大小,密度,边界和增强度,帮助放射学家和临床医生区分肾上腺肿块是肾上腺瘤还是非腺瘤。 其他将ACA功能作为APA或CPA的功能进一步区分(3)。 作为成像技术,双能计算机断层扫描(DECT)或称为Spectrum CT具有为组织内部各种材料提供多种定量信息(4)的优点,以阐明良性和恶性肿瘤(5,6)。 DECT可以通过覆盖更广泛的能量参数来直接准确地反映病变中的血液供应和血管生成状态,从而提供更丰富的定性和定量诊断信息。 到目前为止,据我们所知,使用这种成像模式将APA与CPA区分开的几乎没有相关的报告。 COM/ARTICE/VIEW/10.21037/QIMS-22-1279/RC)。在手术治疗方面,CPA是患病一侧的肾小球切除术,而APA在患病方面是完全肾上腺切除术,因此需要准确的鉴别诊断来指导临床治疗计划(2)。但是,患有APA或CPA的患者显示出一些相似的临床症状和大量的常规成像表现重叠,这使分化很难。尽管肾上腺静脉抽样(AVS)的经皮插管是APA诊断的“黄金标准”,但该程序的难度,成本和侵入性限制了其在临床实践中的广泛使用。在传统的成像检查中,评估主要基于肿瘤的大小,密度,边界和增强度,帮助放射学家和临床医生区分肾上腺肿块是肾上腺瘤还是非腺瘤。其他将ACA功能作为APA或CPA的功能进一步区分(3)。作为成像技术,双能计算机断层扫描(DECT)或称为Spectrum CT具有为组织内部各种材料提供多种定量信息(4)的优点,以阐明良性和恶性肿瘤(5,6)。DECT可以通过覆盖更广泛的能量参数来直接准确地反映病变中的血液供应和血管生成状态,从而提供更丰富的定性和定量诊断信息。到目前为止,据我们所知,使用这种成像模式将APA与CPA区分开的几乎没有相关的报告。COM/ARTICE/VIEW/10.21037/QIMS-22-1279/RC)。我们研究的目的是探索APA和CPA之间能量谱参数的差异,筛选有意义的能量谱指标,并为两者的鉴别诊断提供了理论基础。我们按照明星报告清单介绍本文(可在https://qims.amegroups。
人工智能驱动的鉴别诊断列表对诊断准确性的影响医生:一项开放标签随机对照研究
摘要:背景:展示了人工智能(AI)驱动的自动病史采集系统与人工智能驱动的鉴别诊断列表对医生诊断准确性的有效性。然而,考虑到人工智能驱动的鉴别诊断列表的负面影响,例如遗漏(医生拒绝人工智能建议的正确诊断)和犯错(医生接受人工智能建议的错误诊断),应评估不带人工智能驱动的鉴别诊断列表的人工智能驱动的自动病史采集系统对医生诊断准确性的有效性。目的:本研究旨在评估带或不带人工智能驱动的鉴别诊断列表的人工智能驱动的自动病史采集系统对医生诊断准确性的有效性。方法:这项随机对照研究于 2021 年 1 月进行,纳入了 22 名在大学医院工作的医生。参与者需要阅读 16 个临床案例,其中 AI 驱动的真实患者病史为每个病例生成最多三个鉴别诊断。参与者被分为两组:有和没有 AI 驱动的鉴别诊断列表。结果:两组的诊断准确率没有显著差异(分别为 57.4% 和 56.3%;p = 0.91)。在 AI 生成的列表中包含正确诊断的案例对医生的诊断准确性显示出最大的积极影响(调整后的优势比 7.68;95% CI 4.68–12.58;p < 0.001)。在使用 AI 驱动的鉴别诊断列表的组中,15.9% 的诊断是遗漏错误,14.8% 是犯错错误。结论:医生使用人工智能驱动的自动化病史的诊断准确性在有和没有人工智能驱动的鉴别诊断列表的组之间没有差异。
扩散加权成像在髓母细胞瘤和室管膜瘤鉴别诊断中的准确性
脑肿瘤是儿童最常见的实体肿瘤之一,也是儿童癌症相关死亡的原因(1)。脑肿瘤主要根据组织发生原理进行分类,该原理允许基于与几种假定的起源细胞及其假定的分化阶段的微观相似性对肿瘤进行分类(2)。髓母细胞瘤是一种常见的恶性脑肿瘤,发生于儿童期,占儿童脑肿瘤的 15- 20%(3, 4)。肿瘤通常发生在小脑,在三分之一的病例中常侵入第四脑室,并发展为整个脊髓转移(5)。相关症状不明显,诊断通常会延迟。然而,70% 至 80% 的病例在转移前被诊断出来,而 20% 至 30% 属于高危人群(6)。室管膜瘤是起源于中枢神经系统 (CNS) 的罕见肿瘤。世界卫生组织 (WHO) 已根据组织学将该病分为三类(I、II 或 III),其中
昆士兰州兽医重大疾病调查研讨会
7.45注册8.00简介和管家8.10欢迎来到JCU和JCU兽医科学更新John Cavalieri教授,兽医科学主管8.30欢迎。重大疾病调查;昆士兰首席兽医官8.50紧急动物疾病爆发反应 - 紧急动物疾病反应一致性(EADRA)和奥斯维特计划9.10国家动物生物安全计划9.30重大,生物类动物和紧急动物疾病(EAD)诊断10.00次诊断10.00,昆士兰州作为EADS的鉴别诊断(包括fmd,LSD)12.00昆士兰州的地方性猪病作为EADS的鉴别诊断(包括ASF)13.00午餐14.00昆士兰州的地方性家禽疾病作为EADS的鉴别诊断(包括ND, HPAI) 14.45 Disease investigation group scenario exercise 15.45 Afternoon tea 16.00 Forum discussion - Zoonotic diseases for veterinary practitioners in Queensland – anthrax, Brucella suis, Q fever, Hendra virus, rabies, WHS, infection control and PPE 17.00 Close
HSE AMRIC 指南
• 结核病(特别是怀疑或确诊为耐药性结核病) • 猴痘 * 注意不同进化枝之间的区别: • 采取空气传播预防措施,直到确定水痘的鉴别诊断。 • 水痘(水痘) • 麻疹
昆士兰州兽医重大疾病调查(人畜共患和紧急动物疾病)研讨会
7.45 注册,提供茶和咖啡 8.00 介绍和日常事务 8.10 欢迎来到昆士兰大学并了解昆士兰大学兽医学的最新情况 兽医学院院长 Nigel Perkins 教授 8.30 欢迎。重大疾病调查;加强一般监测和私人兽医的作用 昆士兰州首席兽医官 Allison Crook 博士 8.50 紧急动物疾病爆发响应 – 紧急动物疾病响应协议(EADRA)和 AUSVETPLAN 9.10 国家动物生物安全计划 9.30 重大人畜共患和紧急动物疾病(EAD)诊断检测 10.00 样品保存、包装和提交 10.30 早茶 11.00 昆士兰州地方性反刍动物疾病作为 EAD 的鉴别诊断(包括 FMD、LSD) 12.00 昆士兰州地方性猪病作为 EAD 的鉴别诊断(包括 ASF) 13.00 午餐 14.00 昆士兰州地方性家禽疾病作为 EAD 的鉴别诊断(包括 ND、HPAI) 14.45 疾病调查组情景练习 15.45 下午茶 16.00 论坛讨论- 昆士兰州兽医的人畜共患疾病 - 炭疽病、猪布鲁氏菌病、Q 热病、亨德拉病毒、狂犬病、WHS、感染控制和 PPE 17.00 关闭
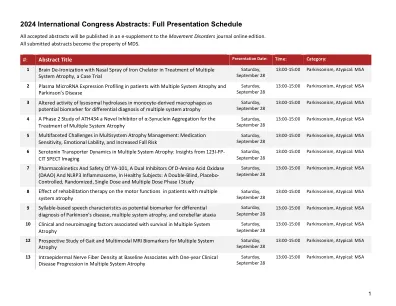
2024 年国际大会摘要:完整演讲时间表
62 进行性核上性麻痹和多系统萎缩的鉴别诊断中的外周炎症严重程度——中性粒细胞与淋巴细胞比率、血小板与淋巴细胞比率和中性粒细胞与高密度脂蛋白胆固醇比率的实用性
数字健康导航未来:生成AI和大型语言模型在医疗保健中的影响
最近发表在《医学互联网研究杂志》上的一项研究发现,在初级和急诊环境中所有医学专业中,Chatgpt在临床决策中的CHATGPT准确性约为72%。这项研究评估了从初始患者互动到整个护理过程的Chatgpt效用,突出了其作为医学增强工具的潜力。该研究涉及分析ChatGpt对36个标准化临床小插曲的反应,以检查其在鉴别诊断,诊断测试,最终诊断和管理方面的能力。虽然CHATGPT在最终诊断中表现出很高的精度(77%),但在鉴别诊断(60%)和临床管理决策(68%)中的准确性较差。该研究还指出,在各种护理环境中,ChatGpt的稳定表现及其在回应中缺乏性别偏见。