XiaoMi-AI文件搜索系统
World File Search System与黄热有关的公共卫生风险评估
这种快速的风险评估(RRA)旨在评估2024年上一学期和2025年开始在美国地区流行国家的最新公共卫生风险。考虑了以下标准进行了此RRA:(i)人类健康的潜在风险(包括暴露风险,疾病的临床 - ePIDEPIDEMIological行为,严重性和严重性的指标以及更详细的风险因素和确定性因素),基于2024和2025和2025年案件中的案件确认趋势的增加,以及在2024年和202.50%(50%)的情况下(2024); (ii)传播的风险,特别是潜在扩散到历史上被归类为疾病风险低的地区,以及(iii)在特有国家内的早期发现,预防和控制能力的不同能力的公共卫生风险,低疫苗覆盖率,低疫苗覆盖率,以及该地区黄热病疫苗短缺的情况。黄热病是一种急性出血性疾病,在十二个国家和南美一个领土上是特有的:阿根廷,玻利维亚,巴西,哥伦比亚,欧洲厄瓜多尔,埃克斯利亚岛,圭亚那,圭亚那,圭亚那,圭亚那,巴拿马,巴拉那,巴拉圭,秘鲁,秘鲁,Surinidad,Trinidad和Tobago和Belivarian(1)(1)(1.1(1)(1)(1)(1)(1)这种疾病在整个历史上引起了许多流行病的死亡率高。病例可能很难与其他病毒出血的发烧,例如体育症病毒,汉塔病毒或登革热。在2024年,在美洲地区确认了61例黄热病病例,其中30例致命(病例死亡比率,CFR = 50%),分布在五个国家之间(3)。在登革热爆发正在发展的情况下,疾病的诊断,尤其是在早期阶段,可能很困难,尤其是当医护人员缺乏检测和治疗病例的经验时(1)。在2025年流行病学周(EW)1和EW 4之间,已有16例确认的黄热病病例,其中7例致命。在2024年,案件主要据报道,整个玻利维亚,巴西,哥伦比亚,圭亚那和秘鲁的亚马逊地区。在2025年,案件主要记录在巴西的圣保罗州和哥伦比亚托利玛部,这两个国家的亚马逊地区以外地区(3)。在美洲,有两个黄热传播周期:Sylvatic和Urban。所有案件发生在由于工作或生态旅游活动而导致野生和/或森林地区(Sylvatic Croce)中有史的人(1-3)。美洲地区黄热病爆发的风险很高。在2024年报告中报告的大多数病例没有黄热病疫苗接种病史(3)。,即使区域黄热病疫苗覆盖率在1920年至2023年之间的疫苗接种覆盖率之前并不是最佳,但在2020年至2023年之间,疫苗接种的覆盖率大大下降,从而增加了所有地方性国家的易感人群的数量。在2023年,厄瓜多尔和圭亚那获得了大于或等于95%的黄热疫苗覆盖率,只有两个国家苏里南,特立尼达和多巴哥的覆盖范围在90%至94%之间。此外,六个国家的黄热病疫苗覆盖率不到80%:阿根廷,玻利维亚的多元状态,巴西,巴拿马,秘鲁和委内瑞拉玻利瓦尔共和国(4)。
黄热病蚊子埃及伊蚊(双翅目:蚊科)对花香和植物挥发物的嗅觉受体
成年蚊子需要定期进食糖类食物,包括花蜜,才能在自然栖息地生存。雄性和雌性蚊子都利用一种叫做嗅觉受体 (OR) 的感觉蛋白来定位潜在的糖源,这种受体被植物挥发物激活,从而定位到花朵或蜜露。黄热病蚊子埃及伊蚊 (Linnaeus, 1762) 拥有一个庞大的嗅觉受体基因家族,其中许多基因家族可能能够检测花香。在这项研究中,我们使用一组与环境相关的植物来源的挥发性化学物质和异源表达系统,发现了埃及伊蚊一组嗅觉受体的配体-受体配对。我们的研究结果支持以下假设:这些气味介导蚊子中枢神经系统对花香的感觉反应,从而影响食欲或厌恶行为。此外,这些嗅觉受体在其他蚊子中保存良好,表明它们在不同物种中发挥着类似的功能。这些信息可用于评估蚊子的觅食行为并制定新的控制策略,特别是结合蚊子诱杀技术的策略。
南非高级委员会尼日利亚签证...
医生。完整填写的卡片应包含以下信息:i. 申请人的全名;ii. 护照号码;iii. 出生日期;iv. 性别;v. 申请人的签名;vi. 接种疫苗的日期;vii. 医生的签名和接种/管理疫苗的中心名称;viii. 疫苗的制造商和批号;ix. 疫苗接种中心的官方印章;x. 疫苗的有效期。10 岁及以下的儿童应提交诊所/健康免疫接种卡。任何新签发的黄热病卡都应符合 2005 年《国际卫生条例》。唯一可接受的黄热病卡(国际旅行证件)是港口卫生部门签发的卡。
肺炎球菌疫苗接种计划获得、免疫原性以及肺炎球菌结合物和黄热病疫苗联合给药研究
简明英语摘要背景和研究目标全球对肺炎球菌疾病的控制受到肺炎球菌结合疫苗 (PCV) 成本的限制。2009 年,冈比亚采用常规三剂接种方案(不加加强剂)(“3+0”方案)引入了 PCV。PCV 的引入已导致侵袭性肺炎球菌疾病(由于疫苗中包含的血清型和严重肺炎)大幅减少。现在疫苗型侵袭性肺炎球菌疾病已得到控制,肺炎球菌疫苗接种方案 (PVS) 研究将比较持续使用的 3+0 方案与过渡到替代的两剂接种方案(包括加强剂、一剂早期剂量和一剂加强剂)。这项拟议的 PVS 子研究旨在评估加强剂量对鼻咽肺炎球菌感染的影响、两种方案的免疫原性以及 PCV 与黄热病疫苗的共同给药。
STAMARIL 数据表
罕见的是,接种疫苗后,曾报告出现黄热病疫苗相关神经性疾病 (YEL-AND),在某些情况下会出现后遗症或致命后果(见第 4.8 节不良反应)。其他神经系统并发症包括格林-巴利综合征 (GBS)、急性播散性脑脊髓炎 (ADEM) 和延髓麻痹。迄今为止,大多数 YEL-AND 病例报告发生在初次接种疫苗者中,发病时间在接种疫苗后 30 天内。60 岁以上和 9 个月以下的人群风险似乎更高(包括从哺乳期母亲传播给婴儿),尽管其他年龄组也有病例报告。先天性或后天性免疫缺陷也被认为是一种易感疾病(见第 4.3 节禁忌症)。然而,在没有确定风险因素的个体中也报告了 YEL-AND 病例。应指导接种疫苗的人,如果接种疫苗后出现任何疑似黄热病的症状,如高烧伴有头痛或精神错乱、性格改变,或者感到极度疲倦、颈部僵硬、痉挛、部分或全部身体失去运动或感觉,应立即就医;还应提醒接种疫苗的人告知其医疗保健专业人员其已接种黄热病疫苗(见第 4.8 节不良反应)。
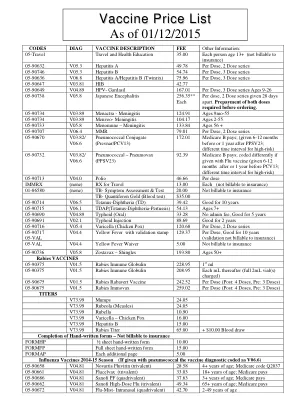
截至2015年1月12日
05-90734 V03.89 Menactra - Meningitis 124.91 Ages 9mo-55 05-90734 V03.89 Menveo- Meningitis 104.17 Ages 2-55 05-90733 V05.8 Menomune – Meningitis 133.84 Ages 56 + 05-90707 V06.4 MMR 79.01 Per Dose, 2剂量系列05-90670 v03.82/ v06.6肺炎球菌联合(PrevNar/ pcv13)172.01 Medicare B Pays; (在PPSV23前6-12个月或PPSV23之后的1年;高风险的不同时间间隔)05-90732 V03.82/ V06.6肺炎球菌 - 肺炎 - 肺炎(PPSV23)92.39 Medicare B Pays; coded differently if given with Flu vaccine (given 6-12 months after or 1 year before PCV13; different time interval for high-risk) 05-90713 V04.0 Polio 46.66 Per dose IMMRX (none) RX for Travel 13.00 Each (not billable to insurance) 01-86580 (none) TB- Symptom Assessment & Test 20.00 Not billable to insurance TB- Quantiferon Gold (Blood测试)$ 35.00 05-90714 v06.5破伤风 - 白喉(TD)39.42 10年10年05-90715 V06.1 TDAP(TETANUS-DIPHTHERIA-PERTUSSIS)54.13 AGES 7+ 7+ 05-90690 V04.89 TY4.89 TYPHIAD(或者) 05-90691 v02.1伤寒注射88.69有用2年05-90716 v05.4 varicella(鸡肉痘)每剂量120.68,2剂量系列05-90717 05-90717 05-VAL V04.4黄热病v04.4黄热病与验证邮票的黄热病为10年,适用于10年的效果(效果为10.37)。 5.00不可账接保险
不要在疫苗存储和处理中犯这些可预防的错误!
可以使用直到小瓶的到期日期,除非有实际污染或在适当条件下不会存储小瓶。然而,必须在重组后的确定时期内使用重构疫苗的多剂量(例如脑膜炎球菌多糖和黄热病)。请参阅包装插入以获取信息。