机构名称:
¥ 1.0
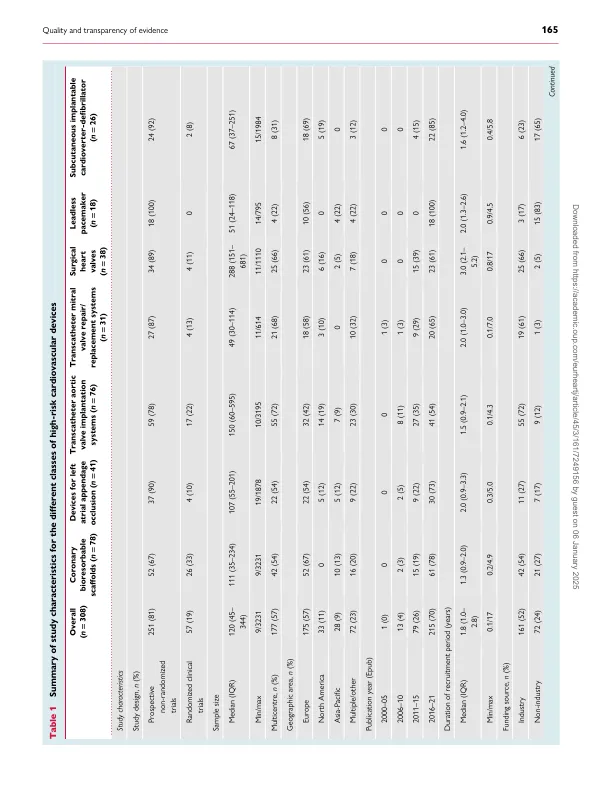
结果至少确定了一项预先指定的设备的70%(50/71)的前瞻性临床试验。总体而言,有473项预期设计的研究(招募97 886个个体)的报告被认为是符合条件的,其中包括81%(251/308)前瞻性非偶然的临床试验(66个186个个体)和19%(57/308)(57/308)随机临床试验(31 700个个人)。研究方案的预期措施可在49%(150/308)的研究中获得,而16%(48/308)具有同行评审的公开协议。在82%(253/308)的研究中评估了与设备相关的不良事件。报告了39%(120/308)的结果裁决过程。与非随机试验相比,随机分组的样本量较大(中位数为304 vs. 100个个体,p <.001)。在CE-MARK批准之前,没有确定任何设备的随机临床试验。非随机临床试验主要在评估中的设备的相应CE-MARK AP(89%,224/251)之后发表。样本量对于之前发表的研究(中位数)(中位数)的样本量小于CE-MARK批准(p <.001)。具有较大样本量(> 50个个体)和招募期更长的临床试验更有可能在CE-MARK批准后发布,并且在2016 - 21年期间更为频繁。
质量和透明的证据 - 可植入 -