XiaoMi-AI文件搜索系统
World File Search System放线菌研究进展:2019 年 ActinoBase 综述
收到日期:2020 年 2 月 21 日;接受日期:2020 年 5 月 28 日;发布日期:2020 年 6 月 19 日 作者隶属关系:1 英国东英吉利大学生物科学学院,诺里奇研究园区,诺里奇,诺福克 NR4 7TJ,英国;2 英国斯特拉斯克莱德大学斯特拉斯克莱德药学和生物医学科学研究所,格拉斯哥大教堂街 161 号,G4 0RE,英国;3 英国兰开夏郡 Edge Hill 大学生物系,L39 4QP;4 英国诺里奇约翰英纳斯中心分子微生物学系,NR4 7UH。 *通讯作者:Thomas C. McLean,T.mclean@uea.ac.uk 关键词:ActinoBase;放线菌;抗生素;发展;方法学;微生物生态学;调节;特殊代谢物;链霉菌;共生。缩写:antiSMASH,抗生素和次级代谢物分析壳;ARTS,抗生素耐药性靶向搜索者;BCI,巴罗科罗拉多岛;BGC,生物合成基因簇;c-di-GMP,3',5'-环二鸟苷酸;ChIP-seq,染色质免疫沉淀测序;DSB,双链断裂;EHEC,肠出血性大肠杆菌;EPEC,肠致病性大肠杆菌;GMC,共同进化的地理马赛克理论;GNPS,全球天然产物社会分子网络;GPA,糖肽抗生素;GPA,糖肽抗生素;HMM,隐马尔可夫模型;ISBA,放线菌生物学国际研讨会;LEE,肠细胞消除位点;MAG,宏基因组组装基因组;NRPS,非核糖体肽合成酶; PKS,聚酮合酶;RiPP,核糖体合成和翻译后修饰肽;SNP,单核苷酸多态性;TCS,双组分系统;T3SS,III 型分泌系统;WGS,全基因组测序。† 这些作者对本作品的贡献相同 000944 © 2020 作者
STAT1-GSDME 焦亡回路的药理激活增强了肝细胞癌的表观遗传免疫治疗
摘要 背景 基因组筛查发现,在对免疫检查点阻断 (ICB) 有耐药性的肿瘤中存在干扰素-γ (IFN γ) 通路缺陷。然而,其非突变调控和治疗发展的可逆性仍不太清楚。 目的 我们旨在鉴定与 ICB 耐药性相关的可用药组蛋白去乙酰化酶 (HDAC),并开发一种针对肝细胞癌 (HCC) 患者的易于转化的联合治疗方法。 设计 我们通过单细胞 RNA 测序将来自 pembrolizumab 试验 (NCT03419481) 的 HCC 患者的预后结果与所有 HDAC 亚型的肿瘤细胞表达相关联。我们使用免疫分析、单细胞多组学和染色质免疫沉淀测序研究了选择性 HDAC 抑制在 4 种 ICB 耐药原位和自发模型中的治疗效果和作用机制,并通过基因调控和共培养系统进行验证。结果 HDAC1 / 2 / 3 表达较高的 HCC 患者表现出 IFN γ 信号传导缺陷,并且在 ICB 治疗中生存率较差。选择性 I 类 HDAC 抑制剂 CXD101 的短暂治疗使 HDAC1/2/3 高肿瘤对 ICB 疗法重新敏感,导致 CD8 + T 细胞依赖性抗肿瘤和记忆 T 细胞反应。从机制上讲,CXD101 与 ICB 协同作用,通过增强染色质可及性和 IFN γ 反应基因的 H3K27 过度乙酰化来刺激 STAT1 驱动的抗肿瘤免疫。肿瘤内募集 IFN γ + GZMB + 细胞毒性淋巴细胞进一步促进 CXD101 诱导的 Gasdermin E (GSDME) 的裂解,从而以 STAT1 依赖的方式触发细胞焦亡。值得注意的是,GSDME 的缺失模仿了 STAT1 敲除,通过阻止细胞焦亡和 IFN γ 反应消除了 CXD101-ICB 联合疗法的抗肿瘤功效和生存益处。结论我们的免疫表观遗传策略利用 IFN γ 介导的网络来增强癌症免疫循环,揭示了自我强化的 STAT1-GSDME 细胞焦亡回路作为正在进行的 II 期试验的机制基础,以应对 ICB 耐药性(NCT05873244)。
乙酰转移酶Nat10抑制T-细胞免疫和...
抽象背景免疫抑制显着有助于鼻咽癌(NPC)的治疗失败。Messenger RNA(mRNA)修饰(例如甲基化和乙酰化)在免疫抑制中起着至关重要的作用。然而,N4-乙酰环甲胺(AC4C),唯一在NPC中很少研究乙酰化修饰事件。方法首先,使用临床组织样品和裸小鼠模型来探索NPC中N-乙酰基转移酶10(NAT10)的表达及其对其的影响。第二,使用癌症基因组免疫数据库和转基因小鼠外周血液免疫细胞板来验证主要受NAT10影响的免疫细胞。然后,通过乙酰化的RNA免疫沉淀序列与RNA测序结合,探索了NAT10 AC4C乙酰化的修饰和显着上调转录因子的表达。然后,通过荧光素酶报告和染色质蛋白元素免疫致敬,分析了CCAAT增强子结合蛋白γ(CEBPG),死盒解旋酶5(DDX5)和类似于解析酶样转录因子(HLTF)的下游调节基因。最后,通过动物模型验证了NAT10对抗编程细胞死亡蛋白1(PD-1)治疗敏感性的影响。在这项研究中,我们旨在探索NAT10(负责AC4C修饰的酶,在NPC进展和患者预后中)的作用。NAT10升高促进了NPC的进展,并与NPC患者的预后不良相关。NAT10的抑制增加了对PD-1治疗的敏感性。NAT10的抑制增加了对PD-1治疗的敏感性。NAT10介导的CEBPG,DDX5和HLTF mRNA的AC4C修饰提高了其稳定性和翻译效率,NAT10/ AC4C/ DDX5轴上调了高移动性组Box 1(HMGB1)(HMGB1),并抑制CD4+和CD4+和CD8+ T细胞。此外,发现HLTF在转录调节Nat10上,表明形成了HLTF-NAT10阳性反馈回路。结论我们的研究阐明了NAT10/DDX5/HMGB1轴通过促进T细胞功能障碍来促进NPC的免疫抑制的机制。此外,NAT10敲低可以增强抗PD-1治疗敏感性作为NPC的组合疗法。
“领养组织”计划推动了识别马组织特异性组蛋白标记的努力
马遗传学和基因组学研究界有着长期的协同合作历史,致力于开发工具和资源来推动马生物学的发展。从 1995 年由 Dorothy Russell Havemeyer 基金会支持举办的第一届国际马基因图谱研讨会 ( Bailey, 2010 ) 开始,研究人员合作构建了全面的马连锁图谱 ( Guérin 等人, 1999, 2003; Penedo 等人, 2005; Swinburne 等人, 2006 )、辐射杂交和比较图谱 ( Caetano 等人, 1999; Chowdhary 等人, 2002 )、物理标记和 BAC 重叠群图谱 ( Raudsepp 等人, 2004, 2008; Leeb 等人, 2006 )、马的参考基因组 ( Wade 等人, 2009; Kalbfleisch 等人, 2018 ) 和基因分型阵列,以经济地绘制和研究马感兴趣的性状主人和饲养者(McCue 等人,2012 年;McCoy 和 McCue,2014 年;Schaefer 等人,2017 年)。为了延续基于社区的进步的传统,作为国际动物基因组功能注释 (FAANG) 联盟的一部分,一项新的集体努力于 2015 年启动,旨在对马的 DNA 元素进行功能注释(Andersson 等人,2015 年;Tuggle 等人,2016 年;Burns 等人,2018 年)。让人想起人类和小鼠的 ENCODE 项目(Dunham 等人,2012 年),FAANG 联盟的最终目标是注释家养动物物种基因组中的主要功能元素(Andersson 等人,2015 年)。具体来说,该联盟选择了四种组蛋白修饰来表征增强子(H3K4me1)、启动子和转录起始位点(H3K4me3)、具有活性调控元件的开放染色质(H3K27ac)和具有无法接近或受抑制的调控元件的兼性异染色质(H3K27me3)的基因组位置(Andersson 等人,2015;Giuuffra 和 Tuggle,2019)。最初的马 FAANG 努力通过对四个目标组蛋白标记进行染色质免疫沉淀测序(ChIP-Seq),在八个优先关注的组织(TOI)中确定了假定的调控区域(Kingsley 等人,2020)。在该研究中,整个马基因组中表征了超过一百万个假定的调控位点。马生物库中储存了 80 多种组织、细胞系和体液(Burns 等人,2018 年),因此有更多机会扩大注释工作的范围。为了充分利用生物库的优势,合作赞助
脑和脑脊液中的神经丝轻链物种以及阿尔茨海默氏病的改变
神经纤维灯光是急性和慢性神经元损伤的完善标记,并且在多种神经疾病中增加。然而,该蛋白质在脑组织或身体流体中没有很好地表征,尚不清楚通过商业测定和是否存在其他物种检测到哪些神经感染光种。我们使用针对各种神经纤维灯域的自定义抗体开发了一种免疫沉淀物质光谱测定法,包括靶向杆域(HJ30.13)的线圈1A/1B的抗体,杆域2B(HJ30.4)和尾部区域(HJ30.4)和尾部区域(HJ30.11)。我们利用我们的测定法来表征患有阿尔茨海默氏病痴呆症和健康对照的个体的脑组织和脑脊液中的神经丝灯光。然后,我们使用我们的定量免疫沉淀物谱法测定法和从患有和没有阿尔茨海默氏病疾病的人的UMAN诊断中,使用我们的定量免疫沉淀物谱法和UMAN诊断的市售免疫测定法进行了测定的定量版本,并测量了神经纤维光浓度。我们的验证队列包括来自30个有症状的淀粉样蛋白阳性参与者的CSF样品,16名无症状淀粉样蛋白阳性参与者,10名有症状的淀粉样蛋白阴性参与者和25个淀粉样蛋白阴性对照。我们在CSF中鉴定了至少三个主要的神经信蚀光种,包括N末端和C末端截断,以及包含尾巴的C末端片段。在CSF中未鉴定出全长神经素养光。这与脑组织形成鲜明对比,脑组织主要包含全长的神经膜和C末端尾域碎片。与健康对照组相比,我们观察到阿尔茨海默氏病患者的神经丝摄影光浓度的增加,而某些神经性抚慰光种的差异要大于其他人的差异。在包括NFL165(线圈1B),NFL324(COIL 2B)和NFL530(在C末端尾部结构域中)的神经纤维灯光片段中观察到了最大的差异。UMAN免疫测定与NFL324相关。这项研究提供了对大脑和CSF中神经纤维光的全面评估,并可以将来对神经感性光生物学和实用性作为生物标志物进行研究。
'SGLT2抑制剂减轻了狼疮中的足细胞损伤...
抽象目标骨关节炎是一种复杂的疾病,具有巨大的公共卫生负担。全基因组关联研究(GWAS)已经鉴定出数百个与骨关节炎相关的序列变体,但是支撑这些信号的效应基因在很大程度上仍然难以捉摸。了解三维(3D)空间中的染色体组织对于以组织特异性方式(例如,基因和调节元件之间的远处基因组特征(例如,基因和调节元件之间)之间的长距离接触至关重要。在这里,我们生成了原发性骨关节炎软骨细胞的第一个整个基因组染色体构象分析(HI-C)图,并确定了该疾病的新型候选效应基因。方法从8例膝关节骨关节炎患者收集的原发软骨细胞进行了HI-C分析,以将染色体结构与基因组序列联系起来。然后将鉴定的环与骨关节炎GWAS结果和来自原发性膝关节关节炎软骨细胞的表观基因组数据结合在一起,以通过增强子促进剂相互作用来鉴定参与基因调节的变体。结果,我们确定了与77个骨关节炎GWAS信号相关的染色质环锚固中的345种遗传变异。例如,PAPPA与胰岛素样生长因子1(IGF-1)蛋白的周转直接相关,而IGF-1是修复受损软骨细胞的重要因素。结论我们已经构建了第一张原代人软骨细胞的HI-C地图,并将其作为科学界的资源提供。这些变体中的十个直接存在于10个新描述的新描述的活跃增强子促进圈的增强区域中,并通过对公共可用的染色质免疫沉淀测序(CHIP-SEQ)进行多组学分析(CHIP-SEQ)和分析酶 - 可访问型染色体的分析(CHIP-SEQ),并使用测序对基因seeq for Generq for Negeq for Necter(ATAC-SEEQ)数据序列(ATAC-SEEQ)chornee chondeq forter(ATAC-SEEQ)序列(ch) SPRY4和PAPPA(与妊娠相关的血浆蛋白A)以及对已知参与骨关节炎的基因SLC44A2的进一步支持。通过将3D基因组学与大规模的遗传关联和表观遗传学数据整合在一起,我们确定了骨关节炎的新型候选效应基因,从而增强了我们对疾病的理解,并可以作为假定的高价值新型药物靶标。
本作品已获得 Creative Commons Attribution-NonCommercial 4.0 International License 许可。摘要 猪瘟是由一种
本作品根据知识共享署名-非商业性使用 4.0 国际许可证进行授权。摘要猪瘟是由黄病毒科猪瘟病毒属的包膜 RNA 病毒引起的,而非洲猪瘟 (ASF) 是由非洲猪瘟病毒科非洲猪瘟病毒属的双链 DNA 病毒引起的。这两种疾病都是毁灭性的,并因死亡、生长迟缓和繁殖性能低下而给养猪业造成巨大损失。非洲猪瘟和猪瘟的临床症状非常相似;因此,必须进行实验室检测来区分这两种疾病。已经开发出用于诊断 CSF 的病毒分离、荧光抗体测试 (FAT)、抗原捕获抗体酶联免疫吸附试验 (ELISA)、逆转录聚合酶链反应 (RT-PCR)、病毒中和试验 (VNT) 和抗体 ELISA。为了检测 ASF,已经开发了 ELISA、化学发光免疫分析 (CLIA)、PCR、荧光素酶免疫沉淀分析 (MB-LIPS)、环介导等温扩增 (LAMP) 和重组酶聚合酶扩增 (RPA)。为了发展养猪业,需要快速诊断和有效的预防措施来帮助管理和消灭这两种疾病。猪已经通过疫苗接种得到了针对这些疾病的保护。必须通过严格的检疫措施防止 CSF 和 ASF 病毒的进入。早期发现和了解疾病的流行病学对于防止疾病传播和制定有效的管理策略都至关重要。本综述提供了对这两种疾病的病原体、流行病学、传播方式、临床症状、发病机制、诊断和控制策略的见解。关键词:控制、生长、死亡率、猪、病毒正确引用:Rai,S。(2024 年)。关于养猪业中古典猪瘟和非洲猪瘟的流行病学、诊断和控制的最新见解。农业与自然资源杂志,7(1),127-144。DOI:https://doi.org/10.3126/janr.v7i1.73220 引言 在许多国家,养猪是家庭收入的主要来源。猪瘟对养猪业影响很大。该病是由黄病毒科疫病毒属的一种有包膜 RNA 病毒引起的。猪瘟是一种严重且造成经济损失的猪病,可以通过地方性和流行性方式感染家猪和野猪种群(Edwards 等人,2000 年)。由于肉类出口贸易限制以及该疾病造成的大面积动物死亡,猪瘟病毒(CSPV)在猪群中的存在会对肉类生产业产生严重的负面经济影响。非洲猪瘟病毒 (ASFV) 是非洲猪瘟病毒科中非洲猪瘟病毒属的成员(Gaudreault 等人,2020 年)。
双特异性抗体重定向合成激动剂受体改性T细胞针对黑色素瘤
背景肉瘤是间充质细胞起源的一个异源性群体,通常很难以较差的预后治疗。大约30%的肉瘤的特征是表达充当致癌驱动因素的融合蛋白。脱落的小圆形细胞肿瘤(DSRCT)是由病原体EWSR1-WT1融合事件定义的典型融合驱动的肉瘤。所得的EWSR1-WT1致癌融合蛋白包含与正常自我蛋白不同的共有氨基酸序列。我们假设克隆保守的融合蛋白可能会产生共享或公共新抗原(NeoAgs)的免疫原性子集(NEOAGS),这可能是新型免疫治疗方法的靶标。使用HLA免疫沉淀/质谱法(HLA-IP/MS)屏幕的方法和结果,我们确定了从EWSR1- WT1融合蛋白的Junctim中得出的9-氨基酸肽序列(SsygQQS EK),均经常出现在HLA-WT1融合蛋白中,并在HLA-a*03中均出现。结合同源肽。我们证实了相同的肽序列在生理上由HLA-A*03 + DSRCT细胞呈现。使用带有MS识别的NEOAG的荧光团偶联的HLA-Multimers(Dextramers),我们检测到在HLA + DSRCT患者子集中结合融合NEOAG的循环T细胞,确认了免疫原性。随后,我们使用融合NEOAG特异性T细胞的体外抗原指导的克隆膨胀来隔离n = 3 HLA-A*03限制性,n = 1 HLA-A*11限制性融合NeoAg反应性克隆。使用单细胞测序,我们检索了由这些T细胞表达的T细胞受体(TCR)的TCRAB基因序列,并将其克隆到逆转录病毒表达载体中。多克隆CD8 + T细胞被检索到的TCR基因结合融合融合的葡萄晶剂,而不是载有病毒肽的控制葡萄糖剂。此外,表达候选TCR的CD8 + T细胞与表达必要的HLA等位基因和EWSR1-WT1融合的细胞稳健上调TNF A,并特别裂解HLA + DSRCT细胞。有趣的是,我们确定了一个独特的TCR,该TCR以肽范围的方式结合了融合NEOAG,该方式可以特异性地裂解HLA-A*03 +和-a*11 + dsRCT细胞,但没有在HLA-A*02的上下文中使用融合NeoAg。这意味着单一的TCR治疗可能覆盖所有北美DSRCT患者的36%。结论我们的数据表明,复发性EWSR1-WT1融合的连接是自然处理的,并在DSRCT细胞普遍存在的HLA等位基因的背景下进行了预处理。这些发现确定了融合派生的公共NEOAG是融合驱动的恶性肿瘤的可行的治疗靶标的来源。这项工作为针对EWSR1-WT1和其他复发性致癌融合的新型T细胞基于T细胞的疗法的临床翻译奠定了基础。
414 科学文摘
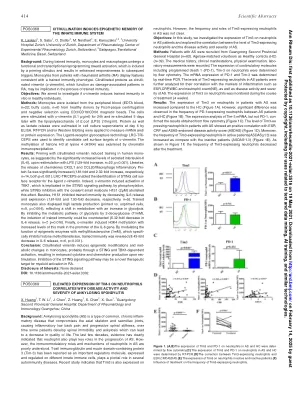
背景:在训练免疫过程中,单核细胞和巨噬细胞经历功能和转录重编程以达到激活状态,这是由启动刺激诱导的,并导致对后续触发的反应性增强。类风湿性关节炎 (RA) 患者的单核细胞表现出与训练免疫表型一致的特征。瓜氨酸化蛋白质如瓜氨酸化波形蛋白 (c-波形蛋白),在 RA 中起损伤相关模式的作用,可能与训练免疫过程有关。目的:我们旨在研究 c-波形蛋白是否在健康个体中体外诱导训练免疫。方法:通过 Ficoll-paque 离心和使用 CD3/CD19/CD56 磁珠进行负选择,从健康供体的外周血 (EDTA 血液,n=22;白膜,n=6) 中分离单核细胞。用 c-波形蛋白 (0.1 μg/ml) 刺激细胞 24 小时,5 天后用大肠杆菌脂多糖 (LPS) (10 ng/ml) 再次刺激。用 ELISA 测定第 6 天细胞培养上清液中的蛋白质和乳酸释放量。应用 RT-PCR 和/或 Western Blotting 测量 mRNA 和/或蛋白质表达。使用配体受体糖基捕获技术 LRC-TRi-CEPS 识别 c-波形蛋白的候选细胞表面靶点。通过染色质免疫沉淀检查组蛋白 H3 在赖氨酸 4 (H3K4) 处的甲基化。结果:用瓜氨酸化波形蛋白进行启动可诱导人类单核细胞进行训练,这可通过用 LPS 重新刺激后分泌的白细胞介素 6 (IL-6) 水平显著增加来证明(增加 1.29 倍,n=22,p<0.001)。同样,趋化因子 CXCL1 和 CCL20/巨噬细胞炎症蛋白 3a 的释放也显著增加(分别增加 1.81 倍和 2.32 倍,n=14,p 值均<0.001)。LRC-TRiCEPS 能够识别配体 c-波形蛋白的 STING 细胞表面受体。事实上,c-波形蛋白通过磷酸化诱导与 STING 信号通路有关的 TBK1 的激活,而用共价小分子 H151 (2μM) 抑制 STING 可消除这种影响。此外,H151 通过减少 IL-6 释放和表达来抑制训练免疫(分别减少 1.61 倍和 1.93 倍,n=5)。训练的单核细胞也表现出高乳酸产生(经引发与未引发的细胞,n=9,p=0.004),反映了代谢的转变和糖酵解的增加。通过抑制 2-脱氧葡萄糖(11mM)的糖酵解代谢途径,可以抵消训练免疫的诱导(IL-6 释放减少 5.32 倍,n=7,p=0.016)。最后,c-波形蛋白诱导 H3K4 甲基化,IL-6 基因启动子中该标记的水平增加。通过使用甲基硫腺苷 (1mM) 来调节表观遗传酶的功能,甲基硫腺苷 (1mM) 可特异性抑制组蛋白甲基转移酶,从而逆转训练后的免疫力(IL-6 释放减少 8.43 倍,n=6,p=0.031)。结论:瓜氨酸化波形蛋白可能通过 STING 和 TBK1 依赖性激活诱导单核细胞的表观遗传修饰和代谢变化,从而导致再刺激后细胞因子和趋化因子产生增强。抑制 STING 信号通路可能是 RA 中髓系激活的新治疗靶点。利益披露:未声明 DOI:10.1136/annrheumdis-2021-eular.3302
通过DNA脱甲基化促进GSDME表达以增加乳腺癌MCF-7 /紫杉醇细胞的化学敏感性< / div>
乳腺癌是全球女性中最常见的癌症[1],是癌症相关死亡的主要原因[2],其发病率逐年增加。在临床上,乳腺癌主要通过手术,放疗,化学疗法和靶向疗法进行治疗[3,4]。但是,大多数患者仍接受常规手术和化学糖尿化的治疗。其中,化学疗法被认为是避免术后癌症复发的关键联系。紫杉醇是一种广谱的抗肿瘤药物,是乳腺癌使用最广泛的Che-Mothapeutics之一[5,6]。它会干扰肿瘤细胞中微管的分解,导致细胞周期停滞,防止癌细胞复制,并最终导致细胞死亡[7]。不幸的是,随着紫杉醇的广泛使用,乳腺癌患者对其产生了抗药性,从而导致治疗衰竭[8-10]。因此,迫切重要性是寻求一种潜在的药物分析机制,并提高乳腺癌患者对紫杉醇的敏感性。Gasdermin(GSDMS)是一个形成孔的蛋白质,在细胞死亡中起重要作用。gsdme是Gasdermin家族的家伙。它最初被识别为DFNA5(耳聋,常染色体显性5)[11,12],也称为ICERE-1,因为它在雌激素受体中的表达较低[1]。最近,越来越多的研究表明,GSDME在调节细胞死亡中起着重要作用[2,13,14]。DNA甲基化是哺乳动物中最稳定的表观遗传修饰之一[19]。通过对加油动物家族与抗癌特性之间关系的深入研究,越来越多的研究人员认为,GSDME是各种癌症的重要预测标记[13,15,16]。作为肿瘤抑制剂,GSDME已被证明可以抑制癌细胞的增殖,迁移和分化[2,13,15]。随着研究的加深,我们发现缺乏GSDME表达可能与肿瘤化学疗法抗性有关[16-18]。此外,已经提出了GSDME表达的丧失会在某些黑色素瘤细胞中引起对依托泊苷的抗性[18]。然而,没有研究研究乳腺癌中GSDME表达与耐化学疗法的关系。我们的目的是测试调节GSDME表达的精力可能是改善乳腺癌化学疗法效应并降低耐药性的有效方法。异常基因表达是人类癌症的特征,DNA甲基化状态的变化可能对基因表达产生深远的影响。它主要发生在基因组稀疏分布的CpG二核中[20]。研究表明,异常的DNA甲基化不仅与人类疾病有关,而且还与有希望的生物候选标记有关[21]。在这项研究中,我们通过使用5-甲基胞霉素抗体富集甲基化的DNA片段进行了免疫沉淀。此方法可以快速识别CpG位点。与高通量测序结合使用,被认为是量化甲基化水平的全基因组技术。许多研究表明,DNA甲基化在大多数肿瘤细胞中降低了GSDME的表达,因此很难在肿瘤细胞中诱导凋亡[15,17,22,23]。因此,我们可以使用DNA甲基转移酶抑制剂(Decitabine)来增加某些癌细胞中GSDME的表达(例如胃癌,大肠癌,乳腺癌等)增加了其对化学疗法药物的敏感性[24,25]。化学疗法会以多种方式导致肿瘤细胞死亡,其中一种是凋亡。凋亡,也称为炎性细胞坏死,是一个新发现的程序性细胞