XiaoMi-AI文件搜索系统
World File Search System批准报告 - 应用A1299果糖基转移酶...
影响分析办公室(OIA)2对影响分析要求进行了更改。不再需要使用OIA完成影响分析。在发生这些更改之前,OIA建议FSANZ与处理辅助工具有关的应用不需要监管影响声明(RIS)(OIA23-06225)。这是因为与允许使用已确定安全的加工辅助工具有关的申请本质上是次要的,并且本质上是放松调节的,因为如果批准了有关变异草案,它们的使用将是自愿的。在这种方法下,FSANZ的评估是该应用不需要RIS。
下一代法呢基转移酶抑制剂 KO-2806 可增强结直肠癌对泛 RAS 抑制的敏感性
• 新兴临床和临床前机制数据表明,与肺癌相比,KRAS 突变型结直肠癌 (CRC) 对突变型选择性 KRAS 抑制剂的敏感性较低。 • 这种差异归因于 CRC 中更高的基底受体酪氨酸激酶 (RTK) 活性和频繁的致癌基因共突变。 • 泛 RAS 抑制剂(例如 RMC-6236)也在 CRC 中进行临床研究,但目前尚不清楚它们的疗效是否会受到类似谱系特异性因素的限制,因为泛 RAS 抑制应能阻止通过野生型 RAS 的信号传导重新激活。 • 我们之前已经表明,法呢基转移酶抑制剂 (FTI) 通过阻断 RHEB 对 mTOR 的激活,使肿瘤对靶向药物(例如 PI3Kα 和突变型选择性 KRAS 抑制剂)敏感。 • 我们假设 RTK 介导的 PI3K-AKT-mTOR 信号传导的重新激活仍然是 CRC 中泛 RAS 抑制剂的负担,并且 FTI KO-2806 将通过减弱这种适应性反应来增强 RMC-6236 在 RAS 抑制剂初治和预处理环境中的活性。
光化学探针鉴定刺猬酰基转移酶(HHAT)中的小分子抑制剂结合位点**
改善神经发育障碍的症状和认知缺陷是当前医学的关键挑战。引起了很多兴趣的神经发育障碍之一是注意力缺陷多动障碍(ADHD),这与影响日常生活和学术成就的不集中和多动症相关,并在执行功能和学习中造成了进一步的困难(Barkley,1997)。尽管儿童中的流行率很高,但最近的工作强调了多动症一直持续到成年(Sayal,Prasad,Daley,Ford,&Coghill,2017年)。非侵入性脑刺激技术已越来越有吸引力,作为一种有前途的工具,在健康和临床种群中显示出神经调节和行为影响,几乎没有不良反应(Reed&Cohen Kadosh,2018)。在这个问题中,Breitling等人的一项研究。(2020)研究了两种类型的经颅直流刺激(TDC)对右下额回的影响对ADHD儿童和青少年的工作记忆过程和表现的影响。
QSAR研究二酰基甘油酰基转移酶-1(DGAT-1 ... ) 1简介面部检测是对象的子集...
糖尿病是通常会感染所有年轻人和老年人的慢性疾病之一。目前尚无特殊药物可以治愈糖尿病。可以使用继续开发的某些酶疗法对糖尿病进行适当治疗。允许治疗糖尿病患者的一步是抑制二十二甘油酰基转移酶-1的生长(DGAT1)。在使用定量结构活动关系(QSAR)方法的硅中开发中,该方法通常用于预测尚未测试的化合物的生物学活性。本研究旨在使用二二酰甘油酰基转移酶-1化合物作为糖尿病生长的抑制剂来构建QSAR模型。使用粒子群优化(PSO)特征选择模型和支持矢量机(SVM)的预测方法,将在二二十二酰甘油酰基转移酶-1化合物中产生主要的描述符的组合建议,该化合物可用于抗糖尿病的发展。所使用的数据集是228个数据,其中包含有关二二酰甘油酰基转移酶-1种化合物的化合物活动的信息,多达1444个功能。使用的描述符信息是一个特征列,其偏差高于0.5。通过多项式内核获得了PSO选择的最佳结果,值为𝑅20.629,以及通过实施RBF模型获得的最佳预测结果,在每个内部验证𝑅2和外部验证2中获得得分,值为75%和67.2%。
QSAR研究二酰基甘油酰基转移酶-1(DGAT-1 ...1简介面部检测是对象的子集...
1简介面部检测是对象识别的子集,这是计算机科学众多研究领域之一。在当天同样,它被认为是软件工程师和执法人员中的一个非常重要的问题,并且知道如何改善犯罪调查和预防犯罪事故。面部检测一直是一个主要的学术主题[1]。这是一种用于检测人脸的计算机视觉方法。计算机视觉已经走了很长一段路,现在有许多可以认为可以实现的研究项目,其中一些被纳入了一个被称为“ OpenCV”的开源计算机视觉项目中。“创建的开源计算机视觉和机器学习软件库,该库为计算机视觉应用提供标准基础,并加速商业产品中的机器感知,” OpenCV网站[2]表示。
UDP-半乳糖 - 乳糖酰胺半乳糖基转移酶在发育过程中的大鼠脑髓素亚菌群中
在发育过程中,大鼠脑髓磷脂亚菌群中描述了含有含有神经酰胺半乳糖基转移酶的酶UDP-半乳糖糖羟基脂肪酸的定位和活性。其他脂质合成酶,例如脑硫磺硫酸光转移酶,UDP-葡萄糖 - 葡萄糖 - 陶瓷葡萄糖基转移酶和CDP-胆碱-1,2-二酰基甘油胆碱磷酸酶磷酸酶也已在肌蛋白亚纤维上和微晶片中进行比较。纯化的髓磷脂被异icnic蔗糖密度梯度离心分离。四个髓磷脂亚馏分分别在0.55 m-(浅绿色蛋白级分),0.75 m-(重膜蛋白级分)和0.85 m-核(膜馏分)和一个颗粒中,分离并纯化。在所有年龄段,在重肌蛋白馏分中发现了总髓磷脂蛋白的70-75%,而在轻膜林馏分中恢复了2-5%的蛋白质,而在膜分数中约为7-12%。大多数半乳糖基转移酶与重膜蛋白和膜分数有关。所研究的其他脂质合成酶似乎不与纯化的髓磷脂或髓磷脂亚菌群相关,而是在微体积 - 膜分数中富集。在发育过程中,当动物大约20天大然后下降时,微粒体半乳糖基转移酶的特异活性达到了最大值。相比之下,在重膜蛋白和膜级分中,半乳糖基转移酶的特异活性比16天大的动物中微粒体膜高3-4倍。酶在重绿色蛋白级分中的特定活性随着年龄的增长而急剧下降。对各个年龄段的重髓蛋白和髓磷脂亚折原的化学和酶学分析表明,膜级分所含的蛋白质与脂质有关,而不是重膜蛋白分数。与胆固醇相比,膜级分在磷脂中也富集,并含有2':3'-循环核苷酸3'-磷酸水解酶,而与重蛋白质和轻质蛋白质级别相比。膜馏分缺乏髓磷脂碱性蛋白和蛋白质蛋白,并富含高分子量蛋白。在髓鞘化刚刚开始的时候,半乳糖基转移酶在重膜蛋白和膜级分中的特定定位表明它可能在髓鞘化过程中起作用。
绿色氨作为空间能量矢量:评论
摘要:哺乳动物结合的O-Acyltransfer- ASE(MBOAT)超家族参与了生长,发育和食欲感应的生物学过程。MBoats是癌症和肥胖症中有吸引力的药物靶标。但是,关于小分子抑制的结合位点和分子机制的信息是难以捉摸的。这项研究报告了光化学探针的合理发展,以询问人类Mboat Hedgehog酰基转移酶(HHAT)中新型的小分子抑制剂结合位点。结构 - 活性关系研究确定了单个启动IMP-1575,这是最有效的HHAT抑制剂报告的待办事项,并指导了维持HHAT抑制效力的Photocroprosslink探针的设计。光叠链链接和HHAT的蛋白质组学测序对哺乳动物MBoat中的第一个小分子结合位点进行了鉴定。拓扑和同源性数据提出了HHAT抑制的潜在机制,该机制已通过动力学分析证实。我们的结果提供了最佳的HHAT工具抑制剂IMP-1575(K I = 38 nm),并提供了绘制MBOAT中小分子相互作用位点的策略。m的膜结合的O-酰基转移酶(MBOAT)蛋白质的超家族与几种至关重要的生物学途径有关。[1]在人类中,其中包括Wnt酰基转移酶(豪猪; Porcn),[2] Hedge- Hog酰基转移酶(HHAT)[3]和Ghrelin O -acyltransferase(Goat)[4],这些酶(山羊)[4]分别调节Wnt和HedgeHog信号传播以及食欲。这些MBoats是癌症和肥胖症中有吸引力的治疗靶标,[1],哺乳动物MBoats的结构信息受到了极大的追捧。各种哺乳动物MBoats的膜拓扑已通过实验确定,支持保守的
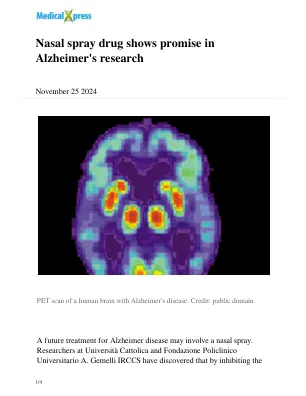
鼻喷药在阿尔茨海默氏症研究中显示出希望
阿尔茨海默氏症的发展是由某些蛋白质的改变驱动的,包括β-淀粉样蛋白和tau,这些蛋白质聚集并积聚在大脑中。这些蛋白质的功能受多种信号和修饰的调节,包括在称为“ S-甲米酰化”的生化反应中附着脂肪酸分子,该反应由S-酰基转移酶(ZDHHC)进行。
K-Ras 异戊烯化作为潜在的抗癌靶点
摘要 KRAS 是最常见的突变致癌基因之一,也是许多靶向疗法的阴性预测因素。因此,迫切需要开发针对突变 KRAS 的靶向策略。一种潜在的策略是破坏 K-Ras 的膜定位,这对其正常发挥功能是必需的。在这篇综述中,我们总结了目前关于 K-Ras 膜锚定重要性的数据,并对这种主要关注异戊烯化抑制的靶向范式进行了严格的评估。此外,我们对来自公开数据库(https://depmap.org/repurposing/)的三类异戊烯化抑制剂(他汀类药物、N-双膦酸盐和法呢基转移酶抑制剂)的异戊烯化相关药物敏感性数据进行了 RAS 突变特异性分析。我们观察到对 N-双膦酸盐和法呢基转移酶抑制剂的敏感性存在显著差异,具体取决于 KRAS 突变状态和组织来源。这些观察结果强调了影响异戊烯化抑制效果的因素的重要性,例如不同 KRAS 突变的不同特征、组织特异性突变模式、K-Ras 周转以及异戊烯化过程调节的变化。最后,我们列出了可能导致临床前和临床研究结果存在巨大差异的因素,包括方法学缺陷、对 K-Ras 蛋白周转的不完全理解以及 KRAS 突变肿瘤中 KRAS 依赖性的变化。
防御脂液滴:专为抗菌免疫设计的细胞器
fi g u r e 1脂质液滴:代谢,形态和组成。(a)主要代谢途径和中间代谢产物的简化方案参与LDS的生物发生和消耗。有关其他详细信息,请参见文本。fa,脂肪酸; FA-COA,酰基辅酶A; CPT1,肉碱棕榈转移酶I; CAC,柠檬酸周期; FASN,脂肪酸合酶; Oxphos,氧化磷酸化; ACC,乙酰辅酶A羧化酶; GPAT,甘油-3-磷酸酰基转移酶; AGPAT,1-酰基-SN-甘油-3-磷酸酰基转移酶; PAP,磷脂酸磷酸酶; DGAT,二甘油类酰基转移酶-1和-2; ACSL,酰基-COA合成酶; ATGL,脂肪甘油三酸酯脂肪酶; HSL,激素敏感脂肪酶; MAGL,单酰基甘油脂肪酶; NCEH,中性胆固醇酯水解酶。(b)内质网中发生的LD生物发生的示意图(ER)。酯化后,中性脂质积聚在ER双层中,形成透镜结构,该结构在ER双层内经过相位分离并成长为形成新生LD的细胞质。细胞质和ER蛋白被募集到LDS表面,促进其生长并萌芽到成熟的LDS中。附件蛋白在此过程中合作。在上面板(红色:TAG的化学结构)中说明了脂肪酸(FA)到三酰基甘油(TAG)中的酯化。(c)。用油酸处理肝HuH7细胞以诱导LD形成16小时(左图)。plin2(绿色)用特异性抗体定位,并用Lipidtox染色中性脂质。(n)表示细胞的核。箭头标记高放大倍数插图中的LD。THP-1细胞进行TEM分析(右图)。脂质液滴由它们的球形形态,相对较低的电子密度和通过单个磷脂单层界定。(d)代表LDS上主要蛋白质的简化方案。(e)该方案包含一些由病原体在宿主细胞中分泌的毒力因子操纵的LD蛋白(黑色)的例子(红色)(有关详细信息,请参见文本)。