XiaoMi-AI文件搜索系统
World File Search System脑缺血 - 再灌注,血管痴呆和阿尔茨海默氏病的线粒体和氧化应激的机制
在临床治疗和科学研究中,神经系统疾病始终代表了一个重大挑战。随着研究的进行,线粒体在神经疾病的发病机理和进展中的重要性越来越突出。线粒体不仅用作能源的来源,而且用作细胞生长和死亡的调节剂。氧化应激和线粒体都与线粒体密切相关,并且有越来越多的证据表明线粒体和氧化应激对神经系统疾病的发病机理产生了关键的调节作用。近年来,脑缺血/再灌注损伤(CI/RI),血管性痴呆(VAD)和阿尔茨海默氏病(AD)的患病率显着升高,这集体代表了一个重大的公共卫生问题。在CI/RI,VAD和AD中,已经观察到线粒体水平降低。通过线粒体水平的增加证明了相关病理的改善。CI/RI导致脑组织缺血和缺氧,这会导致氧化应激,血脑屏障(BBB)的破坏以及对脑脉管系统的损害。BBB的破坏和脑血管损伤可能在某种程度上诱导或加剧VAD。此外,由于血管损伤或功能改变引起的脑灌注不足可能会加剧淀粉样β(Aβ)的积累,从而导致或加剧AD病理学。静脉内组织纤溶酶原激活剂(TPA; Alteplase)和血管内血栓切除术是中风的有效治疗方法。但是,使用TPA和血栓切除术的机会狭窄,这导致CI/RI患者的残疾发生率明显升高。令人遗憾的是,目前还没有VAD和AD的具体药物。尽管美国食品药品监督管理局(FDA)批准了用于AD的临床一线药物,包括美金刚,盐酸多奈奈二奈二奈锡,但这些药物并未从根本上阻止AD的病理过程。在本文中,我们对神经系统疾病中的线粒体和氧化应激的机制进行了综述,近年来进行的临床试验的摘要,以及针对基于粘液和氧化应激的神经系统疾病的新策略的提议。
急性应激导致性别依赖性变化,使腹侧下调突触,电路和焦虑行为
抽象体验单个严重的压力源足以驱动性二态精神病的发展。腹侧下调(VSUB)作为一个部位出现,由于其性别特定的组织和在压力整合中的关键作用,压力可能引起性二态适应性。使用1小时的急性约束应力模型,我们发现应力导致女性VSUB活性的净减少,而女性有效,持久且由肾上腺素能受体信号传导驱动。相比之下,雄性表现出VSUB活性的净增加,该活动是瞬时和由皮质酮信号传导驱动的。我们进一步确定了VSUB输出的性别依赖性变化,以响应压力,并响应压力而焦虑行为。这些发现揭示了与性,细胞类型和突触特异性压力后,与精神疾病相关的大脑区域和行为发生了惊人的变化,这有助于我们理解性依赖性适应,这可能会影响与压力有关的精神病风险。突出显示
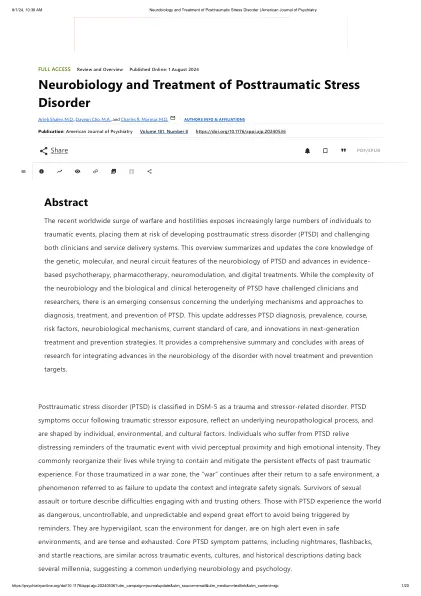
神经生物学和创伤后应激障碍的治疗
显示的是四个功能失调的电路中的已知连通性路径,它们在PTSD的心理病理学中发挥了作用:情感调节和执行功能,威胁检测,上下文处理和恐惧学习。(摘自《新英格兰医学杂志》,A。Shalev,I。Liberzon,C。Marmar,创伤后应激障碍,第1卷376,pp。2459–2469,版权所有©2017马萨诸塞州医学会。经许可转载。)
多不饱和脂肪酸状态和整个生命周期中氧化应激和炎症的标志物:在具有长寿个体的队列中的横断面研究
多不饱和脂肪酸(PUFA)对氧化和炎症性过程有调节作用。这项研究旨在确定172名受试者队列中氧化应激和炎症的循环标志物之间的关系。人口被性别分为三个年龄段:成年人(18 - 64岁,n = 69),老年人(65 - 89岁,n = 54)和长寿(LLIS,90 - 111岁,n = 49)。使用气相色谱法对全血PUFA含量进行了定量。添加了C反应蛋白(CRP),副氧酶(PON),Trolox等效抗氧化剂(TEAC)和马发二醛(MDA)的血清水平。我们的结果表明,成年女性中较高的omega-3(N-3)指数是MDA浓度较低的预测指标(P = 0.038)。相反,总N-3 PUFA和总N-6 PUFA与老年女性和LLI男性的MDA值呈正相关(P <0.05),而总N-6 PUFA与LLI女性的MDA水平成反比(P <0.05)。有趣的是,总N-3 PUFA和N-3指数的浓度增加与LLI男性的TEAC值呈正相关(P = 0.007),而蛛网膜酸(AA)/Eicosapentaenoic(EPA)比率(EPA)比率与LLI Females中的LLI aCEAR呈异常相关。这些发现表明,长寿雌性中的细胞抗氧化能力与AA/EPA比的变化成反比,而N-3 PUFA可能会增强长寿男性的血液抗氧化能力。总体而言,我们的研究强调了不同年龄段的PUFA轮廓与氧化应激和炎症标记之间的复杂性,性别特异性相互作用。
创伤后应激障碍动物模型中的钾通道:机械和治疗意义
频道,导致兴奋性和超极化降低。当代分类基于其亚基组成,跨膜域的数量和功能特性,识别K +通道的三到五个亚型的任何地方。四个最广泛认识的亚型是:(a)电压门控k通道(k v),(b)钙(Ca ++)激活的K通道(k CA),(c)内部矫正K通道(K IR)和(d)两孔域K通道(k 2p)。除此之外,还有一些由特定分子激活的配体K通道,例如环状核苷酸(Kuang等,2015)。k +通道在几个大脑区域都高度表达,包括额叶皮层,基底神经节,海马和杏仁核,在那里它们影响神经元填充,发射器释放和神经可塑性。涉及大脑中K +通道相关突变的孟德尔疾病与发育延迟,癫痫和症状有关,表明焦虑,多动症和自闭症谱系障碍(Alam等,2023)。这使研究人员研究了K +通道功能对非芒德尔精神病综合症的可能贡献。此类研究发现了精神分裂症,抑郁症和自闭症谱系障碍中K +通道活性改变的可能证据。这增加了旨在调节这些通道功能的新型治疗方法的可能性(Vukadinovic和Rosenzweig,2012; Cheng等,2021; Meshkat等,2024)。最近的研究强调了K +通道在与焦虑和恐惧相关的过程中的重要性。在动物模型中,已经发现K V通道在恐惧条件和类似焦虑的行为中起着关键作用(Stubbendor Q.等,2023; Page and Coutellier,2024)。在人类中,编码K V和K IR通道亚基的基因中的多态性与青年人的焦虑症脆弱性有关(Thapaliya等,2023)。本文研究了最近的翻译证据,暗示了创伤后应激障碍发病机理中K +通道功能的变化。
科学现状:长期暴露疗法治疗创伤后应激障碍
恐惧症以情绪加工理论 (EPT) 为基础,该理论首次由 Foa 和 Kozak (1986) 提出,用于解释焦虑相关疾病的发展、维持和恢复。Foa 和 Cahill (2001) 明确阐述了 EPT 在 PTSD 中的应用,并在后续研究中结合新的实验和临床研究结果进行了描述(例如 Foa & McLean, 2016)。EPT 深受 Lang (1979) 的恐惧生物信息理论的影响,根据该理论,创伤事件在记忆中表现为一种认知结构。这种认知结构包括有关痛苦刺激、情绪反应及其含义的信息。该结构中的信息是相互关联的,与结构的任何部分匹配的信息都会激活其整体。在非病理结构中,关联与现实相符(例如,枪声意味着危险),结构的激活会引发适应性行为(例如,寻求掩护)。相反,病理结构涉及不准确的联想(例如,人群意味着危险)并引发不利于安全的适应不良行为(例如,从商店逃跑)。非病理结构仅在威胁情境中被激活,而病理结构则以过度概括和对安全刺激的过度反应为特征。在 PTSD 中,认知结构还以在创伤事件期间和之后用自我无能为力的含义来表征某人的反应为特征(例如,“我是一个软弱的人,因为我没有阻止袭击”)。这些感知促使人们回避与创伤相关的想法、图像和情境,进而阻止情绪处理,从而维持 PTSD 症状。
内质网应激在化疗引起的粘膜炎发病机制中的作用:生理机制和治疗意义
摘要 化疗是治疗癌症的常见有效方法,但这些药物也会产生影响患者健康的严重副作用。其中一种令人衰弱的副作用是粘膜炎,其特征是胃肠道 (GI) 粘膜内壁的炎症、溃疡和生理功能改变。了解化疗引起的肠粘膜炎 (CIM) 的机制对于制定有效的预防措施和支持性护理至关重要。化疗药物不仅针对癌细胞,还针对胃肠道中快速分裂的细胞。这些药物会破坏内质网 (ER) 稳态,导致 ER 应激和各种肠上皮细胞类型中未折叠蛋白反应 (UPR) 的激活。 UPR 触发信号通路,加剧组织炎症和损伤,影响肠上皮细胞的分化和命运,损害肠粘膜屏障的完整性。这些因素对粘膜炎的发生和发展有重大影响。在这篇综述中,我们旨在深入概述 ER 应激在粘膜炎中的作用及其对胃肠道功能的影响。这将为潜在机制提供有价值的见解,并强调可能改善治疗结果和癌症患者生活质量的潜在治疗干预措施。
氧化应激,自噬和...
摘要:神经退行性疾病的发作涉及病理机制的复杂相互作用,包括蛋白质聚集,氧化应激和自噬受损。本综述着重于神经退行性疾病中氧化应激与自噬之间的复杂联系,突出了自噬作为疾病发病机理的关键。活性氧(ROS)在细胞稳态和自噬调节中起双重作用,并破坏了氧化还原信号导致神经变性的氧化物。NRF2途径的激活代表了一种关键的抗氧化剂机制,而自噬通过降解改变的细胞成分来保持细胞稳态。p62/SQSTM1,NRF2和KEAP1之间的相互作用是细胞应激反应必不可少的调节途径,其失调会导致自噬和骨料积累受损。靶向NRF2 -P62/SQSTM1途径有望治疗干预,减轻氧化应激和保留细胞功能。此外,本综述探讨了内源性大麻素系统与NRF2信号传导的潜在协同作用。需要进一步的研究来阐明所涉及的分子机制并制定针对神经变性的有效治疗策略。
脑脊液中的谷胱甘肽氧化为肌萎缩性侧向硬化症中氧化应激的生物标志物Trong Khoa pham 1,2,3,Nick Verber
1 Sheffield转化神经科学研究所(Sitran),谢菲尔德大学,英国S10 2HQ Sheffield,Sheffield 385号。2 School of Biosciences, University of Sheffield, Sheffield, S10 2TN, UK 3 biOMICS Facility, Faculty of Science Mass Spectrometry Centre, University of Sheffield, Sheffield, S10 2TN , UK 4 Neuroscience Institute, University of Sheffield, Sheffield, UK 5 NIHR Sheffield Biomedical Research Centre 6 Nuffield Department of Clinical Neurosciences, Level 6 West Wing, John Radcliffe医院,牛津OX3 9DU,英国。7神经肌肉部,运动神经元疾病中心,皇后广场神经病学研究所,英国伦敦大学伦敦皇后神经病学研究所†这些作者对这项工作和共享作者共享同样贡献 *相应的作者身份 *相应的作者摘要背景:氧化压力是几种神经退行性疾病的关键特征,包括几种amyotrophicrophicrophicrophicrophicrophic the Redic seplal scleral(Als)。鉴定可靠的氧化应激生物标志物将有益于药物目标参与研究。方法:我们进行了公正的定量质谱法(MS)的分析,以衡量来自ALS患者队列的脑脊液(CSF)的蛋白质丰度和氧化的变化,并在两个时间点(相距四个月)在两个时间点(大约四个月)进行了疾病进展。此外,我们开发了一种敏感且有针对性的定量MS方法,以测量相同的CSF样品中的谷胱甘肽氧化态。结果:CSF的蛋白质组学分析揭示了ALS患者的几种蛋白质的丰度,包括Chit1,Chi3L1,Chi3L2和Col18a1的统计学意义,与两个时间点相比。与健康对照组相比,ALS的几种蛋白质氧化位点显着改变,ALS患者的总可逆蛋白氧化水平升高。鉴于谷胱甘肽氧化可能是氧化应激的有用的生物标志物,我们还测量了谷胱甘肽及其在同一样品中CSF中的氧化态。在两个时间点,ALS的总GSH(TGSH),GSSG水平和GSSG/GSH的比率明显高于健康对照组。在第一次访问中,与HC相比,ALS中TGSH,GSSG和GSSG/GSH的比例分别为1.33(P = 0.0215),1.54(P = 0.0041)和1.80(P = 0.0454)。在第二次访问中,这些值分别为1.50(p = 0.0143),2.00(p = 0.0018)和2.14(p = 0.0120)。此外,我们发现疾病持续时间之间的正相关直到第一次访问与总谷胱甘肽(TGSH),GSSG和GSSG/GSH比率。最后,两次访问时ALS患者的可逆氧化蛋白的总强度与GSSG/GSH的比率之间存在很强的正相关。结论:我们建议测量CSF中谷胱甘肽氧化水平可以作为分层生物标志物,以选择ALS患者进行抗氧化剂治疗,并是监测靶向氧化应激的治疗剂的治疗反应的方法。
通过感觉运动技术来增强创伤后应激障碍疗法
1 1 阿维森医院,AP-HP,索邦纳大学巴黎诺德,巴比尼,法国2号,巴黎2学院和神经科学研究所法国4RenéDiatkine单位,法国巴黎第13座心理健康协会,法国5成人精神病学系,Impact,Mondor Hospital,AP-HP,AP-HP,Paris-Paris-EstCréteil,Créteil,法国克里斯蒂尔,法国6Brétigny-Sur-sur-Gorge 7 Institute ofCréteil,France 7 Institute france 7 Institute france 7 Institute france france 7州8 Inspiire,Inserm UMR 1319,洛林大学,南希,法国9 ADES,CNRS UMR 7268,AIX-MARSELILLILY UNIXPYSIL,MARSEILLE,MARSEILLE,法国10,CAEN NORMANDY UNISSHILY HOSTICY,CAEN NORMANDIY UNIXGYS HOSTICY,CAEN,CAEN,法国CAEN,法国,11月11日的物理病理学和成像, 1237年,诺曼底大学,法国坎恩,12个精神病学系,马萨诸塞州综合医院,美国马萨诸塞州波士顿,美国马萨诸塞州,美国13横向心理生成和心理病理学横向单位,索邦内大学巴黎诺德,法国Villetaneuse,法国14号国家弹性和疾病中心,国家杂志和疾病中心。马,美国