XiaoMi-AI文件搜索系统
World File Search System肥厚的心肌病概况 - 全局
1。Maron BJ等人。柳叶刀。2013; 381(9862):242-255。2。Naidu SS,编辑。 肥厚性心肌病。 伦敦,英语:Springer-Verlag; 2015。 3。 Garfikel AC,Seidman JG,Seidman CE。 肥厚和扩张心肌病的遗传发病机理。 心脏失败临床。 2018; 14(2):139-146。 4。 斯坦福医疗保健。 肥厚性心肌病。 2021年6月14日访问。https://stanfordhealthcare.org/medical-conditions/blood-hent-circulation/yypertrophic-cardiomyopathy.html 5。 Semsarian C,Ingles J,Maron MS,Maron BJ。 关于肥厚性心肌病患病率的新观点。 J Am Coll Cardiol。 2015; 65(12):1249-1254。 6。 Mayo诊所。 肥厚性心肌病。 https://www.mayoclinic.org/diseases-conditions/hypertrophic-cardiomyopathy/diagenosis-treatment/drc-20350204。 上次访问于2021年6月29日。 7。 马里兰大学医学中心。 肥厚的心肌病类型,症状和原因。 2021年6月14日访问。https://www.umms.org/ummc/health-services/heart-wascular/services/hyypertrophic-cardiomyopathy/types-sypoms-causes 8。 Jacobs C.成人的肥厚性心肌病:概述。 J Am Assoc护士实践。 2014; 26(9):465-470。Naidu SS,编辑。肥厚性心肌病。伦敦,英语:Springer-Verlag; 2015。3。Garfikel AC,Seidman JG,Seidman CE。肥厚和扩张心肌病的遗传发病机理。心脏失败临床。2018; 14(2):139-146。 4。 斯坦福医疗保健。 肥厚性心肌病。 2021年6月14日访问。https://stanfordhealthcare.org/medical-conditions/blood-hent-circulation/yypertrophic-cardiomyopathy.html 5。 Semsarian C,Ingles J,Maron MS,Maron BJ。 关于肥厚性心肌病患病率的新观点。 J Am Coll Cardiol。 2015; 65(12):1249-1254。 6。 Mayo诊所。 肥厚性心肌病。 https://www.mayoclinic.org/diseases-conditions/hypertrophic-cardiomyopathy/diagenosis-treatment/drc-20350204。 上次访问于2021年6月29日。 7。 马里兰大学医学中心。 肥厚的心肌病类型,症状和原因。 2021年6月14日访问。https://www.umms.org/ummc/health-services/heart-wascular/services/hyypertrophic-cardiomyopathy/types-sypoms-causes 8。 Jacobs C.成人的肥厚性心肌病:概述。 J Am Assoc护士实践。 2014; 26(9):465-470。2018; 14(2):139-146。4。斯坦福医疗保健。肥厚性心肌病。2021年6月14日访问。https://stanfordhealthcare.org/medical-conditions/blood-hent-circulation/yypertrophic-cardiomyopathy.html 5。Semsarian C,Ingles J,Maron MS,Maron BJ。关于肥厚性心肌病患病率的新观点。J Am Coll Cardiol。2015; 65(12):1249-1254。 6。 Mayo诊所。 肥厚性心肌病。 https://www.mayoclinic.org/diseases-conditions/hypertrophic-cardiomyopathy/diagenosis-treatment/drc-20350204。 上次访问于2021年6月29日。 7。 马里兰大学医学中心。 肥厚的心肌病类型,症状和原因。 2021年6月14日访问。https://www.umms.org/ummc/health-services/heart-wascular/services/hyypertrophic-cardiomyopathy/types-sypoms-causes 8。 Jacobs C.成人的肥厚性心肌病:概述。 J Am Assoc护士实践。 2014; 26(9):465-470。2015; 65(12):1249-1254。6。Mayo诊所。 肥厚性心肌病。 https://www.mayoclinic.org/diseases-conditions/hypertrophic-cardiomyopathy/diagenosis-treatment/drc-20350204。 上次访问于2021年6月29日。 7。 马里兰大学医学中心。 肥厚的心肌病类型,症状和原因。 2021年6月14日访问。https://www.umms.org/ummc/health-services/heart-wascular/services/hyypertrophic-cardiomyopathy/types-sypoms-causes 8。 Jacobs C.成人的肥厚性心肌病:概述。 J Am Assoc护士实践。 2014; 26(9):465-470。Mayo诊所。肥厚性心肌病。https://www.mayoclinic.org/diseases-conditions/hypertrophic-cardiomyopathy/diagenosis-treatment/drc-20350204。上次访问于2021年6月29日。7。马里兰大学医学中心。肥厚的心肌病类型,症状和原因。2021年6月14日访问。https://www.umms.org/ummc/health-services/heart-wascular/services/hyypertrophic-cardiomyopathy/types-sypoms-causes 8。Jacobs C.成人的肥厚性心肌病:概述。J Am Assoc护士实践。2014; 26(9):465-470。2014; 26(9):465-470。
围产期心肌病 - 评论文章
诊断不明确和通知标准多变是确定 PPCM 流行病学的限制因素。3 例如,在尼日利亚,发病率估计为每 102 次分娩中 1 次,在日本,发病率估计为每 15,000 次分娩中 1 次。在美国,PPCM 的发病率估计为每 938 次分娩中 1 次;根据住院登记,36 至 54 岁年龄段的患者数量是 15 至 35 岁年龄段患者的两倍多,黑人患者的 PPCM 患病率是 15 至 35 岁年龄段患者的三倍。4 高龄产妇、非裔美国人、妊娠期高血压疾病和多胎妊娠是 PPCM 的主要危险因素。最常见的合并症是动脉高血压(36.2%)、贫血(23.65%)、肥胖(17.6%)、吸烟(17.2%)、慢性肺部疾病(11.8%)、糖尿病(6.3%)和滥用非法药物(3.9%)。5
肥厚型心肌病治疗的创新
肥厚性心肌病 (HCM) 因其异质性表型和临床病程而具有复杂的诊断和预后挑战。人工智能 (AI) 和机器学习 (ML) 技术有望改变心电图 (ECG) 在 HCM 诊断、预后和管理中的作用。人工智能(包括深度学习 (DL))使计算机能够从数据中学习模式,从而开发出能够分析心电图信号的模型。卷积神经网络等 DL 模型在准确识别心电图中与 HCM 相关的异常方面表现出了良好的前景,超越了传统的诊断方法。在诊断 HCM 时,ML 模型在区分 HCM 和其他心脏病方面表现出很高的准确性,即使在心电图结果正常的情况下也是如此。此外,人工智能模型通过预测导致心脏猝死的心律失常事件和识别有心房颤动和心力衰竭风险的患者,增强了风险评估。这些模型结合了临床和影像数据,提供了对患者风险状况的全面评估。挑战依然存在,包括需要更大、更多样化的数据集来提高模型的通用性并解决罕见事件预测中固有的不平衡问题。尽管如此,人工智能驱动的方法有可能通过根据个体患者风险状况提供及时准确的诊断、预后和个性化治疗策略来彻底改变 HCM 管理。本综述探讨了人工智能在 HCM 心电图分析中的当前应用前景,重点关注人工智能方法的进步及其在 HCM 护理中的具体应用。© 2024 作者。由 Elsevier Inc. 出版。这是一篇根据 CC BY 许可开放获取的文章(http://creativecommons.org/licenses/by/4.0/)
围产期心肌病的异常表现
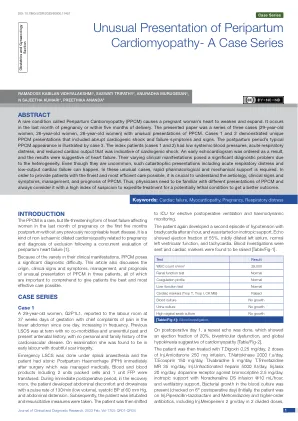
摘要 一种称为围产期心肌病 (PPCM) 的罕见疾病会导致孕妇心脏衰弱和扩张。它发生在怀孕的最后一个月或分娩后的五个月内。本文介绍了三例(29 岁女性、26 岁女性、26 岁女性)的 PPCM 异常表现病例。病例 1 和 2 表现出独特的 PPCM 表现,包括突然的心源性休克和衰竭症状和体征。病例 3 说明了产后时期的典型 PPCM 表现。指标患者(病例 1 和 2)全身血压低、急性呼吸窘迫和心输出量减少,这表明有心源性休克。因此,早期超声心动图检查结果提示心力衰竭。由于异质性,它们不同的临床表现带来了重大的诊断问题。尽管并不常见,但包括急性呼吸窘迫和低输出量心力衰竭在内的灾难性表现还是可能发生的。在这些不寻常的情况下,需要快速的药物和机械支持。为了给患者提供尽可能最优质、最有效的护理,了解 PPCM 的病因、临床体征和症状、治疗和预后至关重要。因此,医生需要熟悉 PPCM 的不同表现,并始终保持高度警惕,以加快对潜在致命疾病的治疗,从而获得更好的结果。
反复发作的Takotsubo心肌病
功能障碍。管理主要涉及提供服务,其中一小部分患者发展为心源性休克。4 TC的复发很少见,估计为1 E 6%,“超级复发”(定义为2 TC复发)异常罕见。5,6复发性TC的拟议的病理生理机制涉及调节胺激增,导致瞬时心肌收缩性和功能障碍。7 Kato等。 试图通过对1400名被诊断为TC的患者进行回顾性分析来确定与复发性TC相关的患者风险因素。 8有趣的是,糖尿病和高胆固醇血症在复发性TC的患者中更为普遍,而患有明显的心血管危险因素的糖尿病和胆固醇血症与复发性TC无关。 8在复发性TC的患者中,人们更频繁地观察到更频繁地观察到频率更高的频率,包括焦虑,癫痫发作,脑血管疾病和偏头痛。 8这项研究突出了与TC相关的重要风险因素。 8,7 Kato等。试图通过对1400名被诊断为TC的患者进行回顾性分析来确定与复发性TC相关的患者风险因素。8有趣的是,糖尿病和高胆固醇血症在复发性TC的患者中更为普遍,而患有明显的心血管危险因素的糖尿病和胆固醇血症与复发性TC无关。8在复发性TC的患者中,人们更频繁地观察到更频繁地观察到频率更高的频率,包括焦虑,癫痫发作,脑血管疾病和偏头痛。8这项研究突出了与TC相关的重要风险因素。8,
观点 - ABC心力衰竭和心肌病
让我们讨论与FEJ相比的一些问题。简单地说,Fejve反映了VE与该腔中存在的血液相关的血液的百分比。让我们思考一些方面:首先,我们将讨论收缩储备(RC),这反映了与努力(锻炼)(努力测试)或药理学(例如多丁胺)相比静止收缩力之间的差异。2我们当中有多少人使用超声心动图(ECO)的努力来计算RC,即在压力下EV的性能?总而言之,我们对RC一无所知,并且对FEJ的信息感到满意。其次,我们分析心室维度与功能概念。在图1中,我们有四个示例具有不同的EV尺寸,但产生相同的收缩期体积(VS)。较小的尺寸(例如,主动脉狭窄或肥厚的心肌病),将尝试以多甲型的方式增加VS。在另一个极端情况下,我们拥有出色的,多动力的VE,可以适应通过空腔扩张的努力条件。请注意,VS在不同的FEJ值中是相同的。他们有什么共同点?无法在努力下产生更大的VS。3 FEJ告诉我们很少。
儿童心肌病的治疗策略
摘要:美国心脏协会的这一科学陈述着重于儿童心肌病(心肌疾病)的治疗策略和方式,并作为有关儿童心肌病的分类和诊断的最新陈述的伴侣科学陈述。我们建议,儿科心肌病的治疗基础是基于这些原理作为心脏病儿童的个性化疗法:(1)鉴定特定的心脏病理生理学; (2)确定心肌病的根本原因,以便如果适用,可能会发生特定原因治疗(精密医学); (3)基于患者相关的临床环境应用疗法。这些临床环境包括患有心肌病风险的患者(心肌病表型阴性),无症状的心肌病患者(表型阳性),有症状性心肌病的患者和终阶段心肌病患者。这种科学陈述主要集中在儿童中发生的最常见的表型,那是扩张和肥厚的。其他较不频繁的心肌病,包括左心室非计算,限制性心肌病和心律不齐的心肌病,较不详细地讨论。建议是基于以前的临床和研究经验,将成人心肌病的疗法推送给儿童,并注意到这种经验中引起的问题和挑战。与成人疾病相比,这些可能强调了儿童心肌病的发病机理甚至病理生理学的明显差异。这些差异可能会影响某些成人治疗策略的效用。因此,除了有症状治疗外,还特别强调了儿童预防和衰减其心肌病的特定原因疗法。还讨论了当前的研究策略和治疗,包括研究管理策略的未来方向,试验设计和协作网络,因为它们有可能进一步完善和改善未来患有心肌病的儿童的健康和结果。
评论文章 - 肥厚性心肌病
肥厚性心肌病是普通人群中最常见的遗传性心脏病,其特征是左心室不对称肥厚。然而,这种心肌病的表型变化远远超出了心室肥大,还包括二尖瓣装置、乳头肌和右心室的变化。由于肥大病因繁多,鉴别诊断困难,心脏磁共振成像在该心肌病的诊断和预后评估中发挥了重要作用。电影磁共振成像可用于确定肥大的位置和程度、晚期增强、检测心肌纤维化的区域,以及用于评估间质纤维化和细胞外体积的 T1 图等最新技术;最后利用组织追踪分析心肌变形。
liraglutide通过幼虫减弱糖尿病心肌病...
1 PharmD计划,药学学院,国王沙特大学,里亚德11451,沙特阿拉伯; shathamajed4@gmail.com(s.m.a. ); rahaf11301@gmail.com(R.M.A。 ); 441200367@student.ksu.edu.sa(r.r.a. ); 441200476@student.ksu.edu.sa(l.a.a. ); 442200723@student.ksu.edu.sa(D.H.A. ); 441200489@student.ksu.edu.sa(s.e.a.-a. ); 441200322@student.ksu.edu.sa(s.o.a. ); 439201033@student.ksu.edu.sa(r.a.a.) 2药理学和毒理学系,沙特国王大学药学学院,里亚德11451,沙特阿拉伯; aaloneazi@ksu.edu.sa(a.s.a. ); nalrasheed@ksu.edu.sa(N.M.A。 ); mahaali@ksu.edu.sa(M.A.A。 ); talshammary@ksu.edu.sa(t.k.a. ); abindayel@ksu.edu.sa(A.F.B.D. ); naldamri@ksu.edu.sa(N.T.A。 ); halghibiwi@ksu.edu.sa(H.K.A. ); dalkhelb@ksu.edu.sa(d.a.a.) 3沙特国王大学理学院动物学系,里亚德11451,沙特阿拉伯; elnagard1@yahoo.com 4动物学系,埃及艾因·沙姆斯大学女士,埃及11566 *通信:nrasheed@ksu.edu.edu.sa;电话。 : +966-1180506821 PharmD计划,药学学院,国王沙特大学,里亚德11451,沙特阿拉伯; shathamajed4@gmail.com(s.m.a.); rahaf11301@gmail.com(R.M.A。); 441200367@student.ksu.edu.sa(r.r.a.); 441200476@student.ksu.edu.sa(l.a.a.); 442200723@student.ksu.edu.sa(D.H.A.); 441200489@student.ksu.edu.sa(s.e.a.-a.); 441200322@student.ksu.edu.sa(s.o.a.); 439201033@student.ksu.edu.sa(r.a.a.)2药理学和毒理学系,沙特国王大学药学学院,里亚德11451,沙特阿拉伯; aaloneazi@ksu.edu.sa(a.s.a. ); nalrasheed@ksu.edu.sa(N.M.A。 ); mahaali@ksu.edu.sa(M.A.A。 ); talshammary@ksu.edu.sa(t.k.a. ); abindayel@ksu.edu.sa(A.F.B.D. ); naldamri@ksu.edu.sa(N.T.A。 ); halghibiwi@ksu.edu.sa(H.K.A. ); dalkhelb@ksu.edu.sa(d.a.a.) 3沙特国王大学理学院动物学系,里亚德11451,沙特阿拉伯; elnagard1@yahoo.com 4动物学系,埃及艾因·沙姆斯大学女士,埃及11566 *通信:nrasheed@ksu.edu.edu.sa;电话。 : +966-1180506822药理学和毒理学系,沙特国王大学药学学院,里亚德11451,沙特阿拉伯; aaloneazi@ksu.edu.sa(a.s.a.); nalrasheed@ksu.edu.sa(N.M.A。); mahaali@ksu.edu.sa(M.A.A。); talshammary@ksu.edu.sa(t.k.a.); abindayel@ksu.edu.sa(A.F.B.D.); naldamri@ksu.edu.sa(N.T.A。); halghibiwi@ksu.edu.sa(H.K.A.); dalkhelb@ksu.edu.sa(d.a.a.)3沙特国王大学理学院动物学系,里亚德11451,沙特阿拉伯; elnagard1@yahoo.com 4动物学系,埃及艾因·沙姆斯大学女士,埃及11566 *通信:nrasheed@ksu.edu.edu.sa;电话。: +966-118050682