XiaoMi-AI文件搜索系统
World File Search System多发性骨髓瘤中嵌合抗原受体(CAR)T细胞疗法的新型进展
蛋黄酱中心分析了286例对硼替佐米和免疫调节剂的耐药性或在这些疗法后复发的患者。中值无事件生存期(EFS)时期仅为5个月,中位总生存期(OS)期为9个月。这些结果表明,抗硼替佐米的患者的预后和原发性/次级免疫调节剂极差(3)。其他新药包括针对骨髓微环境,PD-1/PD-L1信号传导途径抑制剂,组蛋白脱乙酰基酶抑制剂,单克隆抗体抗体CD38 MAB,B-cell b-cell Actipating Mab等(4,5)。上述药物的出现提高了MM患者的功效和预后,但大多数药物通过改变肿瘤细胞的生长环境而产生抗肿瘤作用,而没有特别影响肿瘤细胞的所有阶段。因此,有必要解决更有效,更具体且毒性较小的疗法,以充分实现免疫系统的抗肌瘤潜力。
应用嵌合抗原受体自然杀伤细胞用于1型糖尿病的治疗
在过去的100年中,补充胰岛素一直是1型糖尿病(T1D)治疗的主要手段,其特征是兰格尔汉(Langerhans)胰岛胰岛中产生胰岛素β细胞的渐进性自身介导的损失在过去几十年中,在过去的几十年中,在Glucose Monitoring和Therapeut和The Thepapepation中的技术进一步促进了该技术的高度培训。然而,对于T1D患者而言,发病率,死亡率和生活质量仍然是挑战。胰岛移植已成功进行,但是有几个限制因素,例如缺乏尸体供体以及对终身免疫抑制治疗的需求。因此,对替代治疗方法有很大的医疗需求。在当前的综述中,总结了使用嵌合抗原受体(CAR)-T细胞和天然杀伤(NK)细胞的潜力的当前对T1D治疗的新方法的知识。
CAR 能加速 Treg 的生长吗?嵌合抗原受体 Treg 可诱导移植耐受性
Treg 代表具有抑制能力的 CD4 + CD25 + 细胞的独立 T 细胞谱系 4,5,其在胸腺中生成 (tTreg) 并控制对自身抗原的耐受性,或来自外周 CD4 + T 细胞 (pTreg) 并控制对外来抗原的免疫反应。6-8 通过主转录因子叉头框蛋白 P3 (FoxP3) 的转基因表达以及体外 CD3/CD28、IL-2、雷帕霉素和 TGF- β 的刺激,可以将幼稚 CD4 + T 细胞诱导成为 Treg,也称为 iTreg。9,10 tTreg 的发育和抑制功能由 FoxP3 决定;11 FoxP3 介导的 Treg 编程至关重要,因为 FoxP3 的功能丧失突变会消除 Treg 抑制能力,导致外周耐受性的丧失和严重的自身免疫。 12,13 tTreg 具有更稳定的表观遗传程序 14,并且相当不易回复为效应 CD4 + T 细胞,因为它们在 Treg 特异性去甲基化区域 (TSDR) 上表现出表观遗传稳定状态。15 这与 pTreg 和 iTreg 形成对比,后者缺乏 TSDR 去甲基化 16,具有转化为致病 CD4 + T 细胞亚群的固有风险。Treg 作用于多种促炎细胞,包括 T 细胞
在嵌合抗原受体T细胞疗法之前进行桥接放射疗法的结果
结果:在51例患者中,有25.5%的患有笨重的疾病,而64.7%的患者在RT时患有III/IV期。仅针对所有疾病部位的综合BRT均递送至51%的患者,而29.4%的患者则被全身治疗。中位随访时间为10.3个月(95%CI:7.7-16.4)。在卡尔-T输注后30天时,总体响应率(ORR)为82.4%。中位总生存期(OS)为22.1个月(6.6个未达到),中位无进展生存期(PFS)为7.4个月(5.5-30)。OS/PFS分别为1年的80%(66-99)/78%(64-87),分别为2年的59%(44-71)/54%(40-67)。综合的RT与疾病的所有部位有关,与改善的PFS和OS相关,P≤0.04。此外,ECOG≥2和III/IV期疾病预测OS差(P≤0.02)。疾病大量,IPI≥3和非GCB组织学是疾病的预测因子不良 -
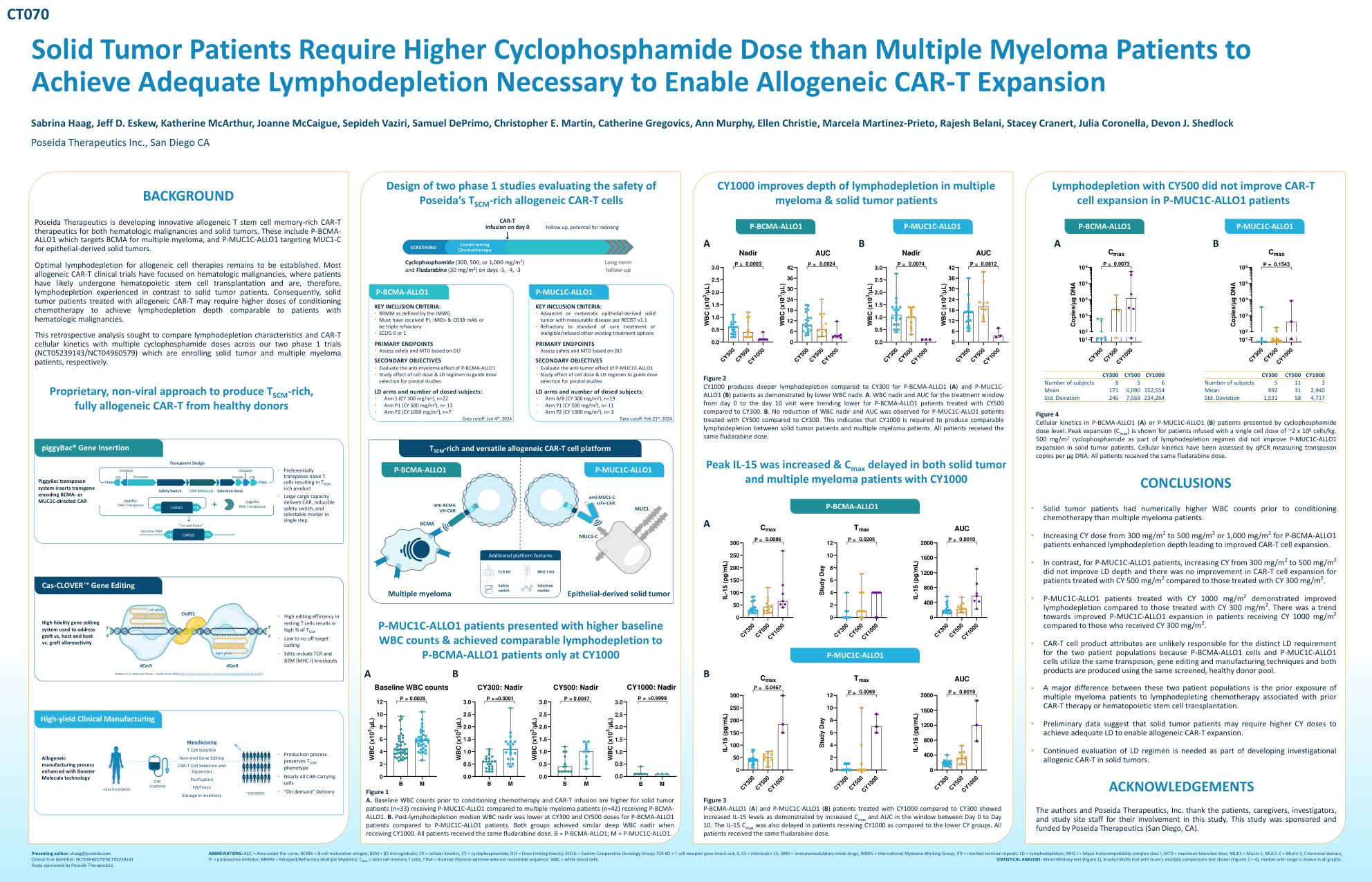
完全同种异体嵌合抗原受体 T 细胞 P-BCMA-ALLO1 的早期安全性和有效性结果
缩写:AUC = 曲线下面积;BCMA = B 细胞成熟抗原;B2M = β2 微球蛋白;CK = 细胞动力学;CY = 环磷酰胺;DLT = 剂量限制毒性;ECOG = 东部肿瘤协作组;TCR KO = T 细胞受体基因敲除;IL-15 = 白细胞介素 15;IMiD = 免疫调节酰亚胺药物;IMWG = 国际骨髓瘤工作组;ITR = 倒置末端重复序列;LD = 淋巴细胞耗竭;MHC I = 主要组织相容性复合体 I 类;MTD = 最大耐受剂量;MUC1 = 粘蛋白 1;MUC1-C = 粘蛋白 1,C 端结构域;PI = 蛋白酶体抑制剂;RRMM = 复发/难治性多发性骨髓瘤;T SCM = 干细胞记忆 T 细胞; TTAA = 胸腺嘧啶-胸腺嘧啶-腺嘌呤-腺嘌呤核苷酸序列;WBC = 白细胞。统计分析:Mann-Whitney 检验(图 1)、Kruskal-Wallis 检验与 Dunn 的多重比较检验(图 2 – 4),所有图表均显示中位数和范围。演示作者:shaag@poseida.com 临床试验标识符:NCT04960579/NCT05239143 由 Poseida Therapeutics 赞助的研究
进展到嵌合抗原受体T细胞疗法后大B细胞淋巴瘤患者的治疗结果
摘要超过60%的复发/难治性(R/R)大细胞淋巴瘤(LBCL)患者接受嵌合抗原受体(CAR)T细胞会经历疾病的进展。在这种情况下,没有标准的下一步治疗和信息是稀缺和异质的。我们分析了387 R/R LBCL患者,他们从2018年7月至2022年3月在西班牙和英国进行了CAR T细胞的进展。中位总生存期(OS)为5.3个月,根据输注和进展之间的间隔(<2个月[1.9个月],2-6个月[5.2个月],> 6个月[未达到])。进展后,237名(61%)患者接受了治疗。着重于首次治疗,Polatuzumab - Bendamustine - Rituximab(Pola)(Pola),双特异性抗体(BSAB)(BSAB)的总体(38%)为67%(38%),45%(35%)的51%(36%),用于放射线疗法(RADI),IIF(26%),33%(26%)(26%)(26%)(26%)(26%)(26%)(26%(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26% (0%)为列纳莱度胺(LENA),化学疗法(CT)的25%(14%)。在生存方面,Pola的12个月进行生存,OS为36.2%和51.0%,BSAB为32.0%和50.1%,RT为30.8%和37.5%,ICI为29.9%和27.8%,ICI为7.3%和20.8%,Lena和6.1%和6.1%和18.3%的CT占CT。三十二名(14%)患者接受了同种异体造血细胞移植,其中位数后中位数为15.1个月后未达到中位OS。总而言之,在CAR T细胞疗法后的前2个月内进展的R/R LBCL患者会出现惨淡的结局。新型的靶向剂,例如polatuzumab和bsabs,可以在CAR T细胞治疗衰竭后长期生存。
进展到嵌合抗原受体T细胞疗法后大B细胞淋巴瘤患者的治疗结果
摘要超过60%的复发/难治性(R/R)大细胞淋巴瘤(LBCL)患者接受嵌合抗原受体(CAR)T细胞会经历疾病的进展。在这种情况下,没有标准的下一步治疗和信息是稀缺和异质的。我们分析了387 R/R LBCL患者,他们从2018年7月至2022年3月在西班牙和英国进行了CAR T细胞的进展。中位总生存期(OS)为5.3个月,根据输注和进展之间的间隔(<2个月[1.9个月],2-6个月[5.2个月],> 6个月[未达到])。进展后,237名(61%)患者接受了治疗。着重于首次治疗,Polatuzumab - Bendamustine - Rituximab(Pola)(Pola),双特异性抗体(BSAB)(BSAB)的总体(38%)为67%(38%),45%(35%)的51%(36%),用于放射线疗法(RADI),IIF(26%),33%(26%)(26%)(26%)(26%)(26%)(26%)(26%(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26%)(26% (0%)为列纳莱度胺(LENA),化学疗法(CT)的25%(14%)。在生存方面,Pola的12个月进行生存,OS为36.2%和51.0%,BSAB为32.0%和50.1%,RT为30.8%和37.5%,ICI为29.9%和27.8%,ICI为7.3%和20.8%,Lena和6.1%和6.1%和18.3%的CT占CT。三十二名(14%)患者接受了同种异体造血细胞移植,其中位数后中位数为15.1个月后未达到中位OS。总而言之,在CAR T细胞疗法后的前2个月内进展的R/R LBCL患者会出现惨淡的结局。新型的靶向剂,例如polatuzumab和bsabs,可以在CAR T细胞治疗衰竭后长期生存。
嵌合抗原受体T细胞疗法在免疫介导的神经疾病中的作用
尽管使用了“高效率”疾病改良疗法,疾病活动和不同免疫介导的神经系统疾病的临床进展仍在某些患者中,导致残疾积累,社会和心理健康,以及对患者和社会的高经济成本。尽管自体造血干细胞移植是一种有效的治疗方式,但它是一种基于强化化学疗法的治疗,具有一系列短期和长期副作用。嵌合抗原受体T细胞疗法(CAR-T)彻底改变了B细胞和其他血液恶性肿瘤的治疗,从而赋予了难治性疾病的长期缓解。然而,这种治疗的毒性,尤其是细胞因子释放综合征和免疫效应物细胞相关的神经毒性综合征,生产的复杂性需要在治疗中心进行高水平的专业化。在免疫介导的B细胞驱动疾病中,CAR-T疗法的早期试验,例如全身性红斑狼疮,神经司肌炎谱谱系障碍和肌无力的GRAVIS,显示出巨大的临床反应,且少数不良事件。基于其他免疫介导的神经系统疾病的常见生理病理学,CAR-T疗法,包括多发性硬化症,慢性炎症性多律性多栏病变,自身免疫性脑炎和僵硬的人综合征,可能是患者的有效选择,避免了长期免疫抑制药物的需求。与自体造血干细胞移植相比,它可能被证明是一种更具选择性的免疫方法,可能会增加效率和较低的不良事件。在这篇综述中,我们介绍了在这种情况下使用CAR-T的最新技术和未来方向。Ann Neurol 2024; 00:1 - 12
B细胞淋巴瘤中嵌合抗原受体T细胞的其他可能性:联合疗法
+ B细胞血液学恶性肿瘤,随着更多免疫治疗方法的可用性,对常规化疗的需求继续下降。将利妥昔单抗添加到CHOP(环磷酰胺,阿霉素,长春新碱和泼尼松)中,将完全缓解(CR)的病例百分比从63%增加到76%,2年的免费生存(EFS)从38%到57%到57%,总体生存率(OS),以及57%至70%至70%(6)。目前,R-Chop(Chop Plus Rituximab)仍然是许多类型B-NHL的标准一线治疗:50%至60%的用R-Chop治疗的患者可实现临床治疗。但是,30%至40%的患者将复发。患有复发/难治性疾病的患者通过二线营救化疗治疗。那些反应的人,然后接受自体干细胞移植(HDC/ASCT)的高剂量化学疗法。不适合HDC/ASCT的患者可能会接受随后的化学疗法。此外,引入靶向药物(例如编程死亡1(PD-1) /程序性细胞死亡凸型1(PD-L1)抑制剂,Bruton的酪氨酸激酶(BTK)抑制剂(BTK)抑制剂,组蛋白脱乙酰基酶(HDACS)抑制剂(HDAC)抑制剂,在相互重复的b-cell b-cell b-cell b-cell b-cell b-cell b-cell beclory bection(HDAC)抑制剂(HDAC)抑制剂(HDAC)中。
嵌合抗原受体T细胞治疗实体瘤的淋巴结蛋白:专注于脑肿瘤
嵌合抗原受体(CAR)-T细胞疗法在血液学恶性肿瘤中表现出显着的功效,正在扩展到包括脑部在内的难治性实体瘤的治疗。淋巴结序(LD)是一个必不可少的预处理过程,通过促进CAR-T细胞的扩张和体内持久性来增强CAR-T功效,并已成为血液学癌症的标准方案。CAR-T治疗对实体瘤的最新临床结果,包括脑肿瘤,表明环磷酰胺/基于氟达拉滨的预处理具有潜在的好处,并且正在实体瘤CAR-T试验中逐渐被采用。此外,一些针对固体TUMOR的CAR-T试验正在尝试开发专门针对实体瘤的LD方案,这与血液学癌症中使用的标准LD方案不同。相比之下,针对脑肿瘤的CAR-T治疗经常在肿瘤或脑脊液中使用局部重复给药,与其他实体瘤相比,LD的使用频率较低。然而,一些临床研究表明,LD仍可能为CAR-T扩展和全身性CAR-T给药的临床反应改善提供潜在的好处。本综述中提出的研究表明,尽管LD可以有益于提高CAR-T效力,但必须考虑其与CAR-T给药途径的兼容性,基于CAR-T结构特征的潜在过度激活以及在正常器官中的靶标表达。此外,鉴于脑部TUMOR的独特特征,可能需要优化的LD剂选择以及剂量和方案,从而突出了进一步研究的需求。