XiaoMi-AI文件搜索系统
World File Search System癌症治疗的新视野
摘要:最近的发现彻底改变了人们将核糖体视为统一的分子机器的观念,揭示了复杂的核糖体异质性。与核糖体实体可互换的传统观念相反,新兴研究强调存在专门的核糖体,每种核糖体都具有独特的组成和功能。细胞和组织特异性、发育和生理状态以及外部刺激(包括昼夜节律)等因素显著影响核糖体的组成。例如,肌肉细胞和神经元分别以不同的核糖体蛋白组和动态行为为特征。此外,核糖体 RNA(rRNA)的替代形式及其转录后修饰为这种异质性增加了另一个维度。这些变化由空间、时间和条件因素协调,使各种专门的核糖体得以表现出来,每种核糖体都具有潜在的不同功能。这种特化不仅影响 mRNA 翻译和基因表达,还对更广泛的生物学背景具有重要意义,尤其是在癌症研究领域。随着对核糖体多样性的理解不断加深,它也为探索细胞功能的新途径铺平了道路,并为翻译的分子复杂性提供了新的视角。
有关步骤治疗的问题?
› Graft Versus Host Disease (GVHD) or › Immune Thrombocytopenia (ITP) or › Multiple Sclerosis or › Neuromyelitis Optica (NMO) Spectrum Disorder or › Systemic Lupus Erythematous (SLE) [Lupus] or › Thrombotic Thrombocytopenic Purpura (Acquired) or › Evans Syndrome or › Bullous肺炎或›免疫疗法相关的脑炎或›免疫介导的肌病/特发性炎症性肌病或›免疫球蛋白G4相关疾病(IgG4-RD)或›疗程疗法或›疗程性疗法或›疗程疗法或›最小变化疾病疾病或›最小变化疾病或›抗体介导的侵犯(Amr)。
辅助治疗的建议...
Psychotherapeutic framework ............................................................................................................................................................................................................................................................................................................................. 18 Preparation ..................................................................................................................................................... 20 Psychedelic experience: Substance, Setting ............................................................................................................... 22 Integration ............................................................................................................................................................................................................................................................................................. 27
癌症治疗的光敏剂
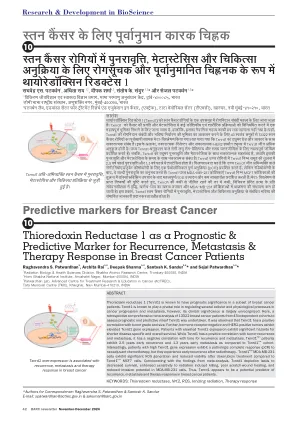
Sarasham Thiadow sunrd1(Txnrd1)以Roginadanan的威严而闻名。 txnrd1以更新在头部的git和terces和meta的terce和meta的«««bhimka(替代酶)的临床意义而闻名。在这里,制作了TXNRD1的Roginadan关系和Bhiwya Nidget的Bhimka,43-_至13322ȗ至13322 - Rigay Sir Rigay Sir Rigay to«Yapi-Yapi-Yapi Yapi Meta-vai-e-e-e-e-e-e-e-Vii。发现txnrd1具有aƿƿ适应TXNRD1适应的患者对于微型疾病和问题很重要«jokhamģ««««««。 While, TXNRD1 has ƿ ƿ ƿ ƿ ƿ ƿ ƿ ƿ dž dž dž dž dž dž dž î î î î î î î î î î î î î है है है है ingredients, and its recurrence is rejuvenated and meta î with timing of tesus. TXNRD1 U'Rigayȗ具有txnrd1的txnrd1,与ȃ2。5年«首次复发dž和1。3年«第一次meta -tesus。事实上,带有患者的TXNRD1基因,一种非常适合化学疗法的病理理性,做一个病理完美的«文章或(PCR)ģ(PCR)ȍ(PCR)ȍȍ,但是在再培养治疗后,但是经过再过疗法后,经验丰富。 TXNRD1 U'MDA-MB-231危机Txnrd1 Niyam McF7 Kisarkas与ȃ博士ǘ在TXNRD1存在的情况下,TXNRD1的存在,在有导师的情况下,对Khar-Dha-Dhavas和MDA-MB-231 Kanchakas的治疗不佳。整体减少了。这辆汽车,txnrd1 - rigya sir rigya sir rigyaȗȗdždždž_____________基î -___ģģ ģģ div>
基因治疗的ABC
通过您用来在家中运送您的软件包简化研究。病毒载体就像盒子一样 - 它是传输DNA或RNA的抗性容器。盒子上的标签用于确保将交付给正确的地址。包裹到达您的房子后,将其带到房子并将其打开。 同一件事也发生在细胞中 - 他们识别运输标签并将载体带入其中。 一旦病毒载体在细胞内部,打开包装并释放其含量以开始治疗。 一种病毒载体称为AAV(Adeno -Annexiated病毒)。 这是输送小DNA或RNA的最佳包装。 AAV载体的各种亚型可以针对特定的细胞类型。 AAV9是能够靶向神经元的载体,因此,它是神经系统疾病基因治疗的良好运输系统。包裹到达您的房子后,将其带到房子并将其打开。同一件事也发生在细胞中 - 他们识别运输标签并将载体带入其中。一旦病毒载体在细胞内部,打开包装并释放其含量以开始治疗。一种病毒载体称为AAV(Adeno -Annexiated病毒)。这是输送小DNA或RNA的最佳包装。AAV载体的各种亚型可以针对特定的细胞类型。AAV9是能够靶向神经元的载体,因此,它是神经系统疾病基因治疗的良好运输系统。
社论:镰状细胞病治疗的进展和基因治疗的潜力
自首次描述以来,镰状细胞病 (SCD) 一直是临床医生试图帮助患者忍受这种可怕疾病后果的治疗挑战。这种终身疾病从第一次危机开始,就以改变患者生理环境的过程开始。在慢性贫血的情况下,这些过程可能导致神经症状恶化和器官损伤,这是那些患有频繁和复发性血管闭塞危机的患者的特征。因此,很明显,降低血红蛋白 S 水平造成的负面影响确实是改善患者长期前景的最佳方法。主要治疗方法是为 SCD 患者提供长期输血支持。然而,许多患者无法忍受已知的伴随螯合疗法的不良事件,而螯合疗法需要减少长期输血造成的铁负荷。我们介绍了各种与 SCD 相关的主题,描述了治疗这种疾病的概念和进展。大多数 SCD 患者从儿童时期就表现出这种疾病的症状和并发症。考虑到这一点,本期刊登了一项来自法属圭亚那的大型研究,该研究描述了儿科患者随时间推移的并发症发病率和类型,并确定了急性胸部综合征和缺血性中风等并发症的发病率(Gargot 等人)。重要的是,尽管这些数据表明缺血性中风的风险低至 3.1%,但到患者进入青少年时期,这一风险却翻了一番。这些数据强调,SCD 患者的治疗方法应侧重于儿童早期的针对性干预,以减少并发症。对于诊断和检测,本期还重新讨论了 SCD 患者的红细胞和网织红细胞计数作为血管闭塞性危象的预测指标(Feugray 等人)。本研究的作者建议使用全血细胞计数获得的网织红细胞参数。具体而言,较高的网织红细胞计数与较高的中等网织红细胞荧光相结合对预测迫在眉睫的危机具有最高的灵敏度和特异性(分别为 81% 和 88%)。
透明质酸作为潜在辅助治疗的癌症靶向治疗的最新进展
结果:从文献中发现,HA可以识别癌组织或细胞外表面大量异常显露的不同受体;因此,它可以与抗癌药物结合,从而有利于其对癌细胞的治疗活性比对正常细胞的治疗活性更强。还发现基于 HA 的药物输送系统可提高抗癌剂在生物环境中的稳定性和溶解度。基于这些发现和优势,HA 已被广泛研究作为一种有前途的生物材料,用于各种递送系统,例如胶束、脂质体、水凝胶、纳米颗粒等。根据最近的研究,基于HA的系统为免疫治疗、基因治疗、靶向化疗和联合治疗提供了巨大的应用空间,可以开发出高效且经济的癌症治疗方法。
有关糖尿病患者(IWGDF 2023)患者诊断和治疗的诊断和治疗的指南
15207560,2024,3,从https://onlinelibrary.wiley.com/doi/10.1002/dmrr.3646下载,由法国Cochrane France,Wiley Online Library,on [04/04/2024]。有关使用规则,请参见Wiley Online Library上的条款和条件(https://onlinelibrary.wiley.com/terms-and-conditions); OA文章由适用的Creative Commons许可