XiaoMi-AI文件搜索系统
World File Search System波形蛋白促进化疗后存活的三阴性乳腺癌细胞的侵袭性
摘要:在了解三阴性乳腺癌 (TNBC) 的化疗耐药性方面,已经积累了大量数据。然而,在联合和序贯治疗中存活的癌细胞的变化仍然鲜为人知。为了模拟临床新辅助治疗,我们首先用表柔比星和环磷酰胺治疗 MDA-MB-231 和 SUM159-PT TNBC 细胞系 2 天,然后用紫杉醇再治疗 2 天。恢复 4 天后,在细胞和分子水平上对治疗中存活的持久细胞进行了表征。持久细胞在体外和斑马鱼模型中表现出生长增加和侵袭性更强。持久细胞富含波形蛋白高亚群,使用 siRNA 方法敲低波形蛋白降低了持久细胞的侵袭性和球体形成能力以及 Akt 磷酸化,表明波形蛋白参与了化疗治疗引起的 TNBC 侵袭性增强。有趣的是,原生细胞中异位的波形蛋白过表达增加了细胞侵袭和球体形成以及 Akt 磷酸化。此外,仅波形蛋白过表达使原生细胞对药物产生耐药性,而波形蛋白敲低使它们对药物更敏感。总之,我们的数据表明,波形蛋白可以被视为 TNBC 耐药性和复发状态中新的可靶向参与者。
稳定波形蛋白磷酸化抑制杂种上皮/间质癌的茎状细胞特性和转移
上皮 - 间质转变(EMT)赋予上皮细胞具有间质和类似茎状的属性,促进转移,这是癌症相关死亡率的主要原因。杂交上皮 - 间质(E/M)细胞保留上皮和间质特征,表现出增强的转移潜力和干性。间充质中间丝,波形蛋白在EMT期间被上调,增强了癌细胞的弹性和侵入性。波形蛋白的磷酸化对其结构和功能至关重要。在这里,我们确定在丝氨酸56处稳定波形蛋白磷酸化会诱导多核,特别是在具有干性特性的杂化E/M细胞中,而不是上皮或间质细胞。癌症干细胞尤其容易受到波形蛋白诱导的多核相对于分化细胞的影响,从而导致自我更新和干性的降低。结果,波形蛋白诱导的多核导致对干性特性,肿瘤起始和转移的持续抑制。这些观察结果表明,波形蛋白中的单个可靶向磷酸化事件对于具有杂化E/M特性的癌中的干性和转移至关重要。
Suprewicz Łukasz、Zakrzewska Magdalena (micro)、Okła Sławomir、Głuszek Katarzyna、Sadzyńska Alicja、Deptuła Piotr、Fiedoruk Krzysztof、Bucki Robert:E
波形蛋白是一种中间丝状蛋白,主要因其在维持细胞结构中的细胞内作用而受到认可,最近引起了越来越多的关注,并成为免疫调节和宿主 - 病原体相互作用中的关键细胞外参与者。虽然细胞外波形蛋白的功能最初被其细胞骨架作用所掩盖,但现在越来越多的证据凸显了其在各种生理和病理事件中的重要性。本综述探讨了细胞外波形蛋白在调节免疫反应和协调宿主细胞与病原体之间相互作用方面的多方面作用。它深入研究了波形蛋白释放到细胞外环境中的潜在机制,阐明了其非常规分泌途径并确定了关键的分子触发因素。此外,还讨论了将细胞外波形蛋白用于诊断和作为疾病治疗的靶蛋白的未来前景。
414 科学文摘
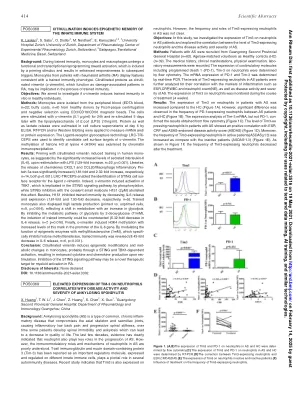
背景:在训练免疫过程中,单核细胞和巨噬细胞经历功能和转录重编程以达到激活状态,这是由启动刺激诱导的,并导致对后续触发的反应性增强。类风湿性关节炎 (RA) 患者的单核细胞表现出与训练免疫表型一致的特征。瓜氨酸化蛋白质如瓜氨酸化波形蛋白 (c-波形蛋白),在 RA 中起损伤相关模式的作用,可能与训练免疫过程有关。目的:我们旨在研究 c-波形蛋白是否在健康个体中体外诱导训练免疫。方法:通过 Ficoll-paque 离心和使用 CD3/CD19/CD56 磁珠进行负选择,从健康供体的外周血 (EDTA 血液,n=22;白膜,n=6) 中分离单核细胞。用 c-波形蛋白 (0.1 μg/ml) 刺激细胞 24 小时,5 天后用大肠杆菌脂多糖 (LPS) (10 ng/ml) 再次刺激。用 ELISA 测定第 6 天细胞培养上清液中的蛋白质和乳酸释放量。应用 RT-PCR 和/或 Western Blotting 测量 mRNA 和/或蛋白质表达。使用配体受体糖基捕获技术 LRC-TRi-CEPS 识别 c-波形蛋白的候选细胞表面靶点。通过染色质免疫沉淀检查组蛋白 H3 在赖氨酸 4 (H3K4) 处的甲基化。结果:用瓜氨酸化波形蛋白进行启动可诱导人类单核细胞进行训练,这可通过用 LPS 重新刺激后分泌的白细胞介素 6 (IL-6) 水平显著增加来证明(增加 1.29 倍,n=22,p<0.001)。同样,趋化因子 CXCL1 和 CCL20/巨噬细胞炎症蛋白 3a 的释放也显著增加(分别增加 1.81 倍和 2.32 倍,n=14,p 值均<0.001)。LRC-TRiCEPS 能够识别配体 c-波形蛋白的 STING 细胞表面受体。事实上,c-波形蛋白通过磷酸化诱导与 STING 信号通路有关的 TBK1 的激活,而用共价小分子 H151 (2μM) 抑制 STING 可消除这种影响。此外,H151 通过减少 IL-6 释放和表达来抑制训练免疫(分别减少 1.61 倍和 1.93 倍,n=5)。训练的单核细胞也表现出高乳酸产生(经引发与未引发的细胞,n=9,p=0.004),反映了代谢的转变和糖酵解的增加。通过抑制 2-脱氧葡萄糖(11mM)的糖酵解代谢途径,可以抵消训练免疫的诱导(IL-6 释放减少 5.32 倍,n=7,p=0.016)。最后,c-波形蛋白诱导 H3K4 甲基化,IL-6 基因启动子中该标记的水平增加。通过使用甲基硫腺苷 (1mM) 来调节表观遗传酶的功能,甲基硫腺苷 (1mM) 可特异性抑制组蛋白甲基转移酶,从而逆转训练后的免疫力(IL-6 释放减少 8.43 倍,n=6,p=0.031)。结论:瓜氨酸化波形蛋白可能通过 STING 和 TBK1 依赖性激活诱导单核细胞的表观遗传修饰和代谢变化,从而导致再刺激后细胞因子和趋化因子产生增强。抑制 STING 信号通路可能是 RA 中髓系激活的新治疗靶点。利益披露:未声明 DOI:10.1136/annrheumdis-2021-eular.3302