XiaoMi-AI文件搜索系统
World File Search System精确的位点特异性和mRNA特异性控制...
Cold Spring Harbor Laboratory Press on February 27, 2025 - Published by rnajournal.cshlp.org Downloaded from Cold Spring Harbor Laboratory Press on February 27, 2025 - Published by rnajournal.cshlp.org Downloaded from Cold Spring Harbor Laboratory Press on February 27, 2025 - Published by rnajournal.cshlp.org Downloaded from Cold Spring Harbor Laboratory Press on February 2025年2月27日 - 由rnajournal.cshlp.org出版于2025年2月27日从冷春港实验室出版社下载 - 由rnajournal.cshlp.org出版于2025年2月27日从冷春港实验室出版社下载 - 由rnajournal.cshlp.org.cshlp.org plocalional出版。
特异性抑制剂阻止了...
摘要◥目的:综合应力反应(ISR)激酶PERK是增殖和休眠癌细胞的生存因子。,我们旨在验证PERK抑制作用,作为一种新的策略,以特定地消除最终恢复和起源转移的次要部位中孤立传播的癌细胞(DCC)。实验设计:在小鼠的合成和PDX模型中测试了一种新型的临床级PERK抑制剂(HC4),该模型在上调ISR的微型转移性病变中呈现静止/休眠DCC或生长降落的癌细胞。结果:HC4通过杀死quies-Cent/慢速循环ISR高,而不是增殖的ISR低DCC来阻止转移。HC4阻止了含有ISR高慢循环细胞的已建立的微米的扩展。in Ingle细胞基因表达和成像表明,肺部中有一定比例的孤立性DCC确实处于休眠状态,并显示了未解决的ER应力为
构建多特异性抗体
创伤性脑损伤(TBI)是由外部力量引起的脑部损伤(车辆,事故,暴力,运动伤害,工业事故,跌倒)。脑创伤可能是由于穿透头骨的物体或快速加速(加速)或大脑的减速(速度放慢或停止)而发生。创伤性脑损伤(TBI)是死亡率和残疾的主要原因,尤其是在儿童和年轻人中。Based on the Glasgow Coma Scale (GCS), the neurological scale used to measure a person's level of consciousness after a brain injury, traumatic brain injury is classified as: mild (GCS 13 - 15), moderate (GCS 9 - 12), severe (GCS 8 or less), and evaluates the following functions: Eye Opening (E), Motor Re- sponse (M), and Verbal Response (V), to determine a patient's overall GCS,将目光响应,运动反应和言语回应的分数添加在一起。分数从3到15。得分为8或更少,表示昏迷。symptoms可以根据头部受伤的严重程度而有所不同。一个轻度创伤性脑损伤的人可以保持意识,或者可能会丧失意识丧失几秒钟或几分钟。其他症状可能包括头痛,混乱,头晕,视力变化,耳朵响起或听力,疲劳或嗜睡的变化,睡眠模式,行为或情绪变化以及认知和/或执行功能问题的变化。注意力缺陷/多动障碍次要患有中度或严重创伤性脑损伤的人可能会出现相同的症状,但头痛可能会变得更糟,反复呕吐或恶心,抽搐或癫痫发作,无法唤醒睡眠,一个或两个学生的眼睛,slurred语,弱点,弱点,弱点或无数的差异,以及每圆形的损失,或者丧失的范围,或者是丧失。
双特异性抗体
行动机制 - 它们如何工作?双特异性抗体(BSABS)是一种新的免疫疗法药物(使用人体免疫系统来对抗癌症的药物),旨在识别在细胞表面上表达的两个不同靶标,称为抗原。这些药物可以静脉注射(直接注入静脉)或皮下(皮肤下方)。在血液中,BSABS会在整个体内传播,并将自己固定在具有特定抗原的细胞上。根据其作用机理(药物如何在体内产生影响),这些药物可以分为细胞桥接的BSAB(最常用的)和抗原交联的BSAB。细胞桥接的BSAB与癌细胞的一种抗原结合(例如,CD20或CD19在B细胞淋巴瘤中)和一种来自健康免疫细胞的抗原(例如 CD3在T细胞中或自然杀伤中的CD16中的CD1)。 相反,抗原交联BSAB与同一细胞中的两个抗原结合。CD20或CD19在B细胞淋巴瘤中)和一种来自健康免疫细胞的抗原(例如CD3在T细胞中或自然杀伤中的CD16中的CD1)。相反,抗原交联BSAB与同一细胞中的两个抗原结合。
使用等位基因特异性PCR
这项研究范围内的改进是可能的,包括将测定法应用于早期繁殖线,最初通过病原体测试验证标记呼叫和更快的提取技术。KASP标记如果我们可以在人口达到近亲状态之前为其选择它们,将特别有用。f2至F4选择是理想的选择,因为杂合子和那些纯合子与易感性连接标记等位基因的纯合子可以立即被丢弃。在随后的几代人中较少的植物/线条将节省繁殖计划中的时间和空间。病原体测试
临床文档中的特异性:
在表面上,很容易看出在护理点上失去特异性如何影响患者的整体健康状况。当患者真正患有糖尿病时,在糖尿病中打字,这是由于潜在的疾病而患有糖尿病,患有第4期慢性肾脏疾病,并且长期使用胰岛素的使用本身并不是不正确的,但显然对下一位参与患者护理的临床医生可能没有任何帮助。在人口水平上,缺乏粒度也具有重大影响。在这种情况下,数据不能保持许多健康技术解决方案所需的细节水平,以正确处理数据并提供有意义的见解。没有该患者糖尿病的细节以及每个患者糖尿病的相关细节 - 也不可能创建准确的价值集,以产生可以改善患者健康和福祉的人群健康数据。
COV2特异性细胞免疫
建议使用二价mRNA疫苗来解决冠状病毒疾病变异,并建议对高危组提出其他剂量。但是,有效性,最佳频率和剂量数量仍然不确定。在这项研究中,我们检查了接受血液透析的患者第五次给药后,我们检查了mRNA严重急性呼吸综合征2(SARS-COV-2)疫苗后的长期细胞和体液免疫反应。据我们所知,这是第一项研究,旨在监测五剂mRNA疫苗接种(包括双重mRNA疫苗)后,高危人群中的体液和细胞免疫动力学的长期数据。虽然大多数患者在整个观察期保持体液免疫,但我们观察到降低的细胞免疫反应性,如由祖先策略所刺激的ELISPOT分析所测量的,在一部分患者中。第五剂剂量三个月后,一半的个体(50%; 14/28)保持了细胞免疫力,尽管获得了体液免疫。阳性对照与T点反应性之间没有关系表明这些免疫改变是对SARS-COV-2的特异性改变。在多变量分析中,年龄≥70岁的参与者显示出反应性结果的可能性较小。值得注意的是,在接受异源疫苗的14个人中,有13个成功获得了细胞免疫,支持了此
多发性骨髓瘤双特异性抗体
随着免疫疗法的出现,多发性骨髓瘤 (MM) 的治疗方案发生了重大转变。以肿瘤抗原为重点的新型疗法现在推动了 MM 研究的进步。双特异性抗体 (bsAbs) 利用生物工程技术的革命性进步,体现了第二代基于抗体的肿瘤疗法。最近对复发/难治性 MM 病例的 bsAbs 研究显示,其疗效显著,安全性可接受。elranatamab 和 teclis-tamab 的获批代表了 MM 治疗用 bsAbs 的下一步发展。本综述文章讨论了针对治疗耐药性 MM 的 bsAbs 的抗原靶向、疗效、安全性和应用策略,重点关注临床试验和真实世界数据。
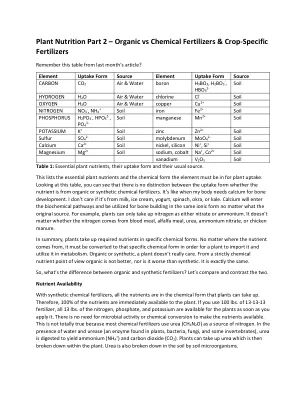
有机与化肥和特异性肥料
使用合成化肥,所有养分都处于植物可以占用的化学形式。因此,100%的养分可立即用于植物。如果您使用100磅。13-13-13肥料,全部13磅。 施用氮,磷酸盐和钾的,植物就可以使用它。 无需微生物活性或化学转化即可使营养可用。 这不是完全正确的,因为大多数化肥将尿素(CH 4 N 2 O)作为氮的来源。 在存在水和脲酶的情况下(在植物,细菌,真菌和某些无脊椎动物中发现的酶)消化以产生铵(NH 4 +)和二氧化碳(CO 2)。 植物可以吸收尿素,然后将其分解在植物内。 尿素也被土壤微生物在土壤中分解。13-13-13肥料,全部13磅。,植物就可以使用它。无需微生物活性或化学转化即可使营养可用。这不是完全正确的,因为大多数化肥将尿素(CH 4 N 2 O)作为氮的来源。在存在水和脲酶的情况下(在植物,细菌,真菌和某些无脊椎动物中发现的酶)消化以产生铵(NH 4 +)和二氧化碳(CO 2)。植物可以吸收尿素,然后将其分解在植物内。尿素也被土壤微生物在土壤中分解。