XiaoMi-AI文件搜索系统
World File Search SystemI型干扰素对全身性红斑狼疮患者的Aarifrolumab封锁,在两个3期试验的基因表达和蛋白质组学分析中调节关键的免疫病理途径
抽象目标是评估单次验证骨髓间充质基质细胞(BM-MSC)与慢性下背部疼痛(LBP)患者中的假安慰剂的功效。方法参与者是在2018年4月至2022年12月之间的一项前瞻性,双盲,对照研究中随机分配的,以接受假注射或在验证内注射2000万个同种异体BM-MSC中。第一个共同主要终点是通过改善视觉模拟量表(VAS)至少20%和20 mm的响应者的速率,或者在基线和12个月之间的OSWESTRY残疾指数(ODI)为20%。二级结构共同主要终点是通过基线和第12个月之间的定量MRI T2测量的盘流体含量评估的。次要终点包括疼痛VAS,ODI,短形式(SF)-36和所有时间点上临床上最小的临床差异(1、3、6、12和24个月)。我们确定了与基线至6个月之间同种异细胞注入相关的免疫反应。记录了严重的不良事件(SAE)。结果114例被随机分组(n = 58,BM-MSC组; n = 56,假安慰剂组)。在12个月时,未达到主要结果(在安慰剂组中,BM-MSC组为69%; P = 0.77)。组在所有次要结果上没有差异。没有与干预有关的SAE。得出的结论虽然我们的研究并未结论证明同种异体BM-MSC对LBP的功效,但该程序是安全的。MSC治疗LBP的长期结局仍在研究中。试验登记编号Eudract 2017-002092-25/Clinicaltrials。Gov:NCT03737461。
ANA屏幕定量ELISA分析套件
全身性自身免疫性疾病,例如全身性红斑狼疮,硬皮病,类风湿关节炎,sjögren综合征,皮肤肌炎,混合结缔组织疾病的特征是出现各种自身抗体的外观,这些自身抗体针对细胞核的组成部分。尽管尚未完全揭示某些自动抗体的显着性和病理相关性,但自动抗体的检测被广泛确定,并且在诊断系统性自身免疫性疾病中起着重要作用。anascreen允许在一个样品中检测到一个样品中的核和细胞质抗原的总自身抗体,作为诊断全身自身免疫性疾病的摘要参数。完整的HeLa核与重组蛋白和纯化的天然抗原的抗原结合可确保对ANA检测的最大敏感性和特异性。
Auxilin 是一种新的先天性心脏传导阻滞易感基因,可直接影响胎儿心脏功能
摘要 目的 新生儿红斑狼疮 (NLE) 可能在母体自身抗体经胎盘传播后发生,其心脏表现(先天性心脏传导阻滞,CHB)包括房室传导阻滞、心房和心室心律失常以及心肌病。抗 Ro/SSA 抗体与红斑狼疮的关联已得到充分证实,但尽管存在母体自身抗体,但复发率仅为 12%–16%,这表明 CHB 的发展需要其他因素。在此,我们确定了导致 CHB 风险的胎儿遗传变异,并阐明了它们对心脏功能的影响。方法 在至少有一例 CHB 病例的家族中进行了全基因组关联研究。通过微阵列、RNA 测序和 PCR 分析基因表达,通过蛋白质印迹、免疫组织化学、免疫荧光和流式细胞术分析蛋白质表达。分析了原代心肌细胞和多能干细胞诱导细胞的钙调节和连接。通过多普勒/超声心动图分析了胎儿心脏的性能。结果我们确定 DNAJC6 是一种新的胎儿易感基因,DNAJC6 心脏表达降低与疾病风险基因型相关。我们进一步证明,缺乏辅助蛋白(由 DNAJC6 编码的蛋白质)的胎儿心肌细胞在培养中具有异常的连接和 Ca 2+ 稳态,以及 Ca v 1.3 钙通道的细胞表面表达降低。辅助蛋白缺乏的胎儿小鼠的多普勒超声心动图显示子宫内心脏 NLE 异常,包括心律失常、心房和心室异位以及房室时间间隔延长。结论我们的研究确定了辅助蛋白是NLE调节心脏功能的第一个遗传易感因素,为CHB的筛查和治疗策略的发展开辟了新的途径。
羟氯喹眼部毒性案例研究。
我们开发 RMA 方法的动机是基于一个实际例子,即当前需要从文献中快速获得证据共识。羟氯喹自 1950 年代 [ 6 ] 开始问世,用于治疗疟疾、红斑狼疮和类风湿性关节炎。最近,羟氯喹被强调为一种支持冠状病毒病 (COVID-19) 患者的潜在干预措施。尽管羟氯喹在每种临床条件下的疗效结果不同,但不良事件往往是一致的。在本研究中,我们使用 RMA 来回答有关羟氯喹的特定临床问题以及眼部毒性作为副作用的程度。这是一个重要的临床问题;然而,我们无法找到合适的结果聚合方法。
性别和性别对免疫和自身免疫性的影响
对某些生物学性别的某些疾病的偏爱是众所周知的,这种性偏斜的某些生物学原因越来越明显。多年来对自身免疫性患者的临床观察,在诸如Covid19之类的感染期间,表明生物学对疾病进展至关重要,并且通常是最终结果。在此简短评论中,基本和临床观察结果都有助于我们了解生物学如何影响免疫疾病。在自身免疫性疾病的情况下,早期动物数据和临床观察表明,雌激素和睾丸激素等性类固醇在疾病的临床表现中起着重要作用(1)。疾病全身性红斑狼疮(SLE)是研究广泛的临床状况之一(2)。自身免疫性疾病可能是由一系列因素引起的:遗传易感性,表观遗传调节(miRNA,DNA甲基化和组蛋白修饰),导致抗原模仿或其他某些其他原因激活免疫系统的原因。
2024指南
可遇到另外的细胞减少症(中性粒细胞减少症比血小板减少症的频率更高),婴儿的短暂性血小板病。2除了患有GATA1突变的病例。3强烈暗示DBA综合征;但是不够具体,无法进行诊断。仅在专业实验室中进行4个研究测试;在模棱两可或非信息遗传学的情况下有用。 5通常在成年人中呈现。 6这些IBMF通常表现出多型细胞减少症,并且经常出现其他影响多器官系统的疾病特异性异常。 这种区别特征可以帮助将这些条件与DBA综合征区分开,该疾病最初以孤立的红细胞发育不全表现出来。 缩写:BM;骨髓; EADA,红细胞腺苷脱氨酶; HBF,胎儿血红蛋白; SLE,全身性红斑狼疮; prca,纯红细胞性植物; CLL,慢性淋巴细胞性白血病; LGL,大颗粒状淋巴细胞性白血病; CT,计算机断层扫描; MRI,磁共振成像; IBMF,继承的骨髓衰竭综合征; FA,Fanconi贫血; SDS,Shwachman钻石综合征; DC,Dyskeratosis Congenita。仅在专业实验室中进行4个研究测试;在模棱两可或非信息遗传学的情况下有用。5通常在成年人中呈现。6这些IBMF通常表现出多型细胞减少症,并且经常出现其他影响多器官系统的疾病特异性异常。这种区别特征可以帮助将这些条件与DBA综合征区分开,该疾病最初以孤立的红细胞发育不全表现出来。缩写:BM;骨髓; EADA,红细胞腺苷脱氨酶; HBF,胎儿血红蛋白; SLE,全身性红斑狼疮; prca,纯红细胞性植物; CLL,慢性淋巴细胞性白血病; LGL,大颗粒状淋巴细胞性白血病; CT,计算机断层扫描; MRI,磁共振成像; IBMF,继承的骨髓衰竭综合征; FA,Fanconi贫血; SDS,Shwachman钻石综合征; DC,Dyskeratosis Congenita。
氯和羟氯喹
氯喹和羟氯喹也已被指出为covid-19。两者都在预防和治疗疟疾和自身免疫性疾病(例如慢性多性关节炎) - 类风湿关节炎以及少年特发性关节炎和红斑狼疮。及其基于这种自身免疫性活性,它已经开始考虑其在治疗冠状病毒感染1中的使用,也已在SARS流行病和Zika 2病毒中使用。在SARS-COV-19 1上,这些分子在各种方面作用,例如预防病毒进入细胞,防止其复制,并最终作用于负责这种疾病加重的无性反应。在批准的指示中使用这两种药物有广泛的经验,因此众所周知其安全性。实际上,所有欧洲人都参观疟疾的地方性地理区域,以氯喹进行数十年的预防,并在返回后持续2个月。目前使用羟氯喹,因为它在自身免疫性疾病中具有较大的应用。
患者的人口统计学,病毒学和临床特征
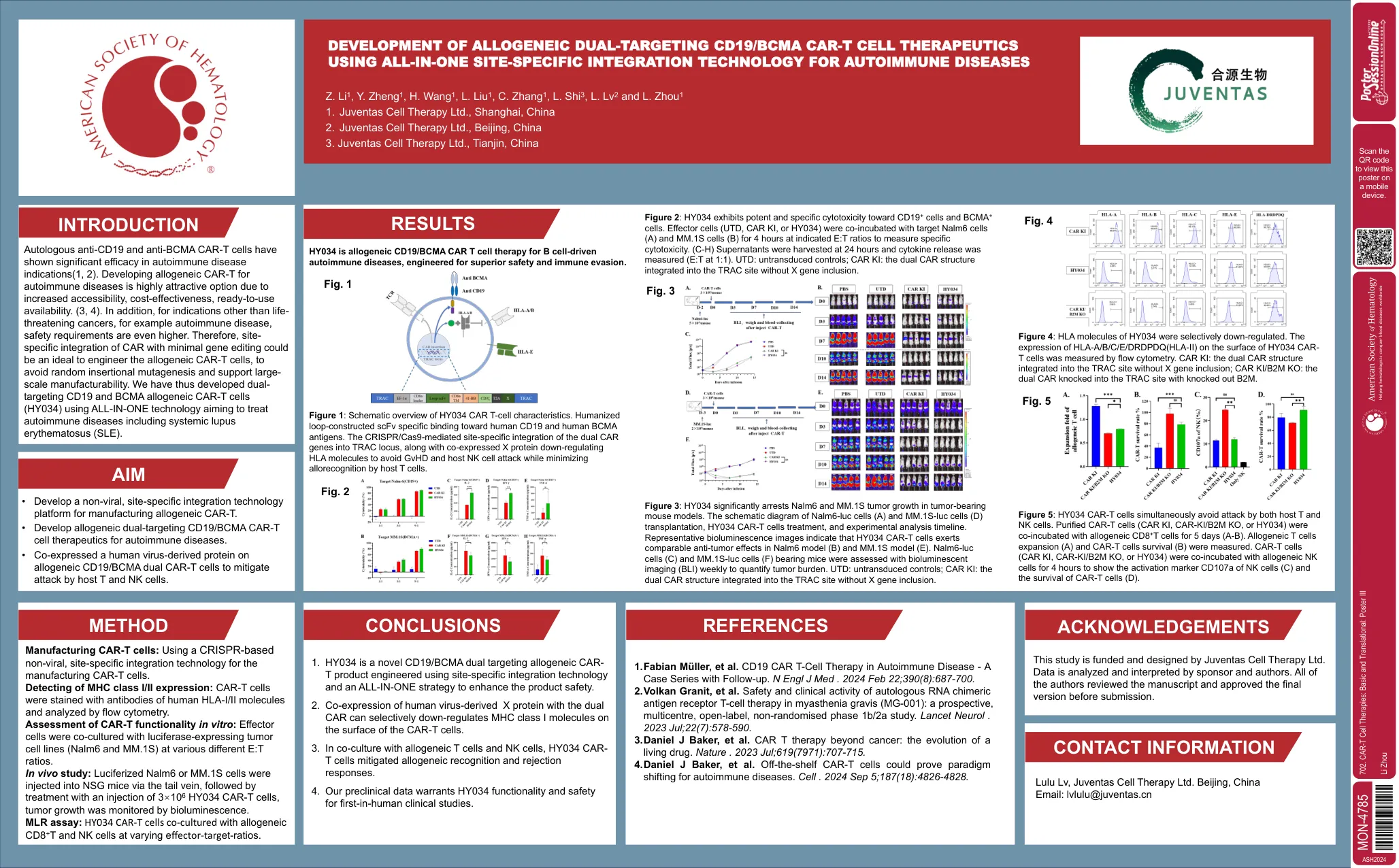
自体抗CD19和抗BCMA CAR-T细胞在自身免疫性疾病适应症中表现出显着的功效(1,2)。为自身免疫性疾病开发同种异体CAR-T,由于可访问性,成本效益,现成的可用性提高,因此非常有吸引力的选择。(3,4)。此外,对于危害生命的癌症以外的适应症,例如自身免疫性疾病,安全要求甚至更高。因此,使用最小基因编辑的CAR特定于位置集成可能是设计同种异体CAR-T细胞的理想选择,以避免随机的插入诱变并支持大规模的生产性。因此,我们使用旨在治疗包括全身性红斑狼疮(SLE)在内的自身免疫性疾病的旨在治疗自身免疫性疾病的旨在治疗自身免疫性疾病的双重靶向CD19和BCMA同种异体CAR-T细胞(HY034)。
lupkynis(voclosporin)
lupkynis是一种口服钙调蛋白抑制剂(CNI)免疫抑制剂,在结构上与环孢素A结构相似。它在2021年获得了FDA的批准,用于治疗活性狼疮肾炎(LN),并结合背景免疫抑制治疗。ln是全身性红斑狼疮(SLE)的并发症,可以发展为终结阶段肾脏疾病(ESRD)。蛋白尿通常是LN的第一个迹象,这是通过尿蛋白肌酐比率(UPCR)升高的。通过肾脏活检证实诊断,该肾脏活检揭示了疾病的分类,并用于指导治疗。给药基于估计的肾小球过滤率(EGFR),大多数患者可能处于剂量范围的高端。高血压是一种常见的副作用,建议进行血压监测。lupkynis(voclosporin)在满足以下标准时将考虑覆盖:
chikungunya疫苗:2023年更新
系统红斑狼疮(SLE)是一种影响多个器官的慢性自身免疫性疾病,持续性疾病活动与发病率和死亡率的增加有关。免疫细胞功能的损害和对自我抗原的免疫耐受性丧失是触发炎症并驱动SLE发病机理的重要决定因素。树突状细胞(DC)是最有效的抗原细胞,它是先天性和适应性侵蚀系统之间的关键联系。SLE发育和发病机理与DC的稳态和功能的异常调节有关,因此,DC靶向的疗法对于治疗SLE和自身免疫性疾病的治疗变得非常重要。本综述着重于DC在促进SLE发病机理中的重要性,并进一步讨论了SLE治疗中DCS的临床潜力。对DC在SLE中作用的见解将为SLE患者提供治疗策略的改善。