XiaoMi-AI文件搜索系统
World File Search SystemTL 13-112,在大鼠血浆中使用LC-MS/MS Workflow
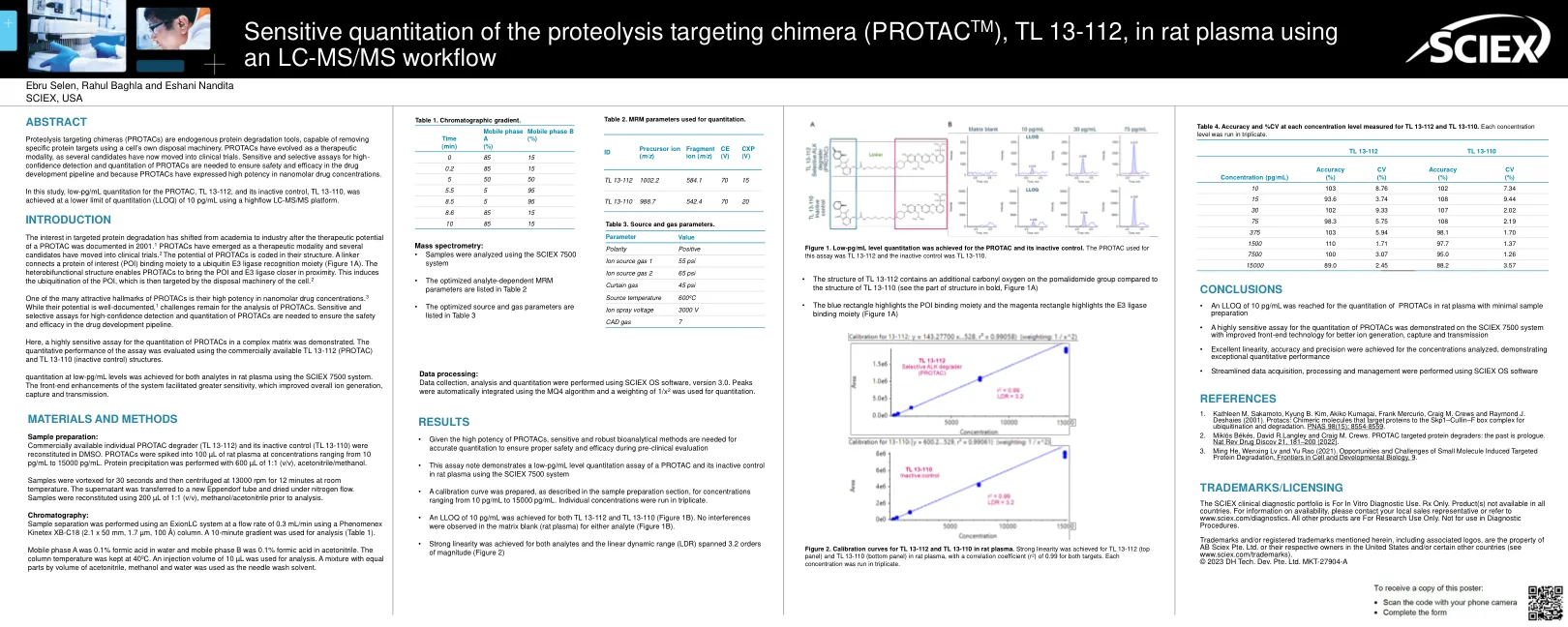
在2001年记录了Protac的治疗潜力后,对靶向蛋白质降解的兴趣已从学术界转变为工业。1个Protac已成为一种治疗方式,几个候选者已进入临床试验。2 Protac的潜力在其结构中编码。接头将感兴趣的蛋白质(POI)结合部分连接到泛素E3连接酶识别部分(图1A)。异常结构使Protac可以使POI和E3连接酶更接近。这引起了POI的泛素化,然后由细胞的处置机制靶向。2
BTK和CIAP1蛋白质降解器三元复合物的快照和合奏
杂功能嵌合降解器是一类配体,它们募集靶蛋白到E3泛素连接酶以驱动化合物依赖性蛋白质降解。对作用机理至关重要的是靶,降解器和E3连接酶之间形成三元复合物,以促进泛素化和随后的降解。然而,存在对三元复合物结构的有限见解,包括几乎没有对最广泛选择的E3,凋亡1的细胞抑制剂的研究(CIAP1)。我们的结果揭示了独特的三元复合结构的见解,并表明增加的三元复合稳定性/刚度不一定总是与提高的降解效率相关。
通过双链DNA片段的单链DNA寡桥构建SGRNA-CAS9表达载体
功能活性(粘性终端连接):20μl含有0.5 µL快速T4 DNA连接酶,12μgHindiii消化的lambda DNA和1x T4 DNA连接酶在37°C下孵育37°C,过夜,由Agarose gelorophoresis确定的片段,在> 95%的片段中,> 95%的片段。重新消化的连接产物,50μl反应,其中含有6μg连接的片段,40个单位Hindiii和1x的Nebuffer 2在37°C下孵育2小时,导致未检测到的未检测到的未发现的片段,因为琼脂糖凝胶电基果实确定。
患者案例讨论与Celmods治疗Paul ...
BMSC,骨髓间充质干细胞; Celmod,Cereblon E3连接酶调节药物; CRBN,Cereblon; CRL4,Cullin 4环泛素连接酶; Cul4,基于Cullin-Ring的E3泛素 - 蛋白连接酶; DDB1,损伤特异性DNA结合蛋白1; Dex,地塞米松; IFN,干扰素; il,白介素; IMID,免疫调节药物; NCAM,神经细胞粘附分子; NK,自然杀手; ROC1,Cullins 1的调节剂; TCR,T细胞受体; TGF,转化生长因子; UB,泛素; VCAM,血管细胞粘附分子; VEGF,血管内皮生长因子。1。Lonial S等。柳叶刀血肿。2022; 9(11):E822-E832; 2。Richardson PG等。 n Engl J Med。 2023; doi:10.1056/nejmoa2303194。 的数字来自:(左)Sato T等。 前细胞开发生物。 2021; 9:629326; (右)D'Souza C等。 前疫苗。 2021; 12:632399。 2Richardson PG等。n Engl J Med。2023; doi:10.1056/nejmoa2303194。的数字来自:(左)Sato T等。前细胞开发生物。2021; 9:629326; (右)D'Souza C等。前疫苗。2021; 12:632399。2
识别新型降解剂和抗性机制...
选择性雌激素受体降解剂 回文重复序列 SERM 选择性雌激素受体 CRL Cullin-RING 连接酶调节剂 CSN COP9 信号体 sgRNA 单向导 RNA DCAF DDB1 和 CUL4 相关因子 SMI 小分子抑制剂 DDB1 DNA 损伤结合蛋白 1 SOCS/BC 细胞因子信号抑制剂/DNMT 从头甲基转移酶 elongin-BC DUB 去泛素化酶 SR 底物受体 E1 泛素活化酶 STK 丝氨酸/苏氨酸激酶 E2 泛素结合酶 TPD 靶向蛋白降解 E3 泛素连接酶 UPS 泛素-蛋白酶体系统
在靶向蛋白质降解器的硅硅设计中
作为治疗方法的靶向蛋白质降解已经看到了惊人的发展和巨大的投资[1]。蛋白水解 - 靶向嵌合体(protac)和诱导靶向蛋白质降解的相关分子具有很大的价值,主要是因为与常规目标占用驱动抑制剂相比,对于给药,安全性,有效性,选择性和调节“不可用的”目标[2] [2]。这些异常小分子具有三个化学特征:与靶蛋白的部分结合,另一种与E3泛素连接酶结合,以及与这两个元素结合的接头[3]。除了protac,还有某些称为分子胶地的非晶状体小分子蛋白蛋白二聚体,它们还结合了泛素E3连接酶和募集蛋白质以降解,类似于带有靶向蛋白质降解的Protacs [4]。
泛素介导的蛋白水解:通过破坏的生物调节
总结泛素蛋白水解系统在一系列基本的细胞过程中起重要作用。是细胞周期的调节,免疫反应和炎症反应的调节,信号转导途径的控制,发育和分化。这些复杂过程通过单个或子集的蛋白质的特异性降解来控制。deg含量涉及两个连续的步骤,共轭泛素的多种部分以及26S蛋白酶体对标记蛋白的降解。一个重要的问题涉及基于系统特异性的机制的身份。底物识别受一个大型家族泛素连接酶的控制,该连接酶可以认识底物,结合它们并催化/促进它们与泛素的相互作用。生物评估22:442±451,2000。β2000 John Wiley&Sons,Inc。
连接酶介导的具有双面 5-羧基尿嘧啶核碱基的 CuII 响应变构 DNA 酶的合成
基于互补氢键碱基配对的核酸高度复杂的分子识别能力导致了 DNA 纳米技术研究领域的迅猛发展。1 通过控制 DNA 杂交和结构以响应诸如 DNA/RNA 结合、pH 变化和光照射等刺激,已经创建了大量 DNA 纳米设备、传感器和分子机器。2 金属离子也可用作外部刺激来调节 DNA 结构和功能,特别是通过利用金属介导的非自然碱基配对。3 通过与桥接金属离子络合,两个相反的配体型核碱基类似物之间形成金属介导的人工碱基对。金属介导的碱基配对通常可以稳定 DNA 双链,从而以金属依赖的方式控制 DNA 杂交。为了通过金属络合有效地切换 DNA 功能,我们最近建立了一种新的概念,即双面 5-修饰嘧啶核碱基的金属介导碱基对切换。 4 – 7 双面碱基,如 5-羟基尿嘧啶 ( U OH ) 4,5 和 5-羧基尿嘧啶 ( caU ) 6 被设计成在金属介导的自碱基对 (例如, U OH – Gd III – U OH ) 中形成
植物PAXX具有XLF样函数,并刺激了ku -dna连接酶IV/XRCC4复合物的DNA末端
非同源末端连接(NHEJ)在修复DNA双链断裂中起主要作用,并且是基因组稳定性和编辑的关键。最小的核心NHEJ蛋白,即Ku70,Ku80,DNA连接酶IV和XRCC4,但其他因素在不同的真核生物组中有所不同。在植物中,唯一已知的NHEJ蛋白是核心因素,而植物NHEJ的分子机制仍然不清楚。在这里,我们报告了先前未知的PAXX植物直系同源物,其晶体结构显示出与人类“ PAXX”相似的折叠。然而,通过与KU70/80和XRCC4相互作用,植物PAXX具有与人XLF相似的分子函数。这表明植物PAXX结合了哺乳动物PAXX和XLF的作用,并且这些功能在进化过程中合并为单个蛋白质。这与PAXX和XLF在哺乳动物中的重新效力一致。