XiaoMi-AI文件搜索系统
World File Search System抗癌药物的靶向递送方法
过去 30 年中,随着我们对致癌过程、细胞生物学和肿瘤微环境的认识不断加深,成功的癌症治疗方法的数量显著增加 [ 1 , 2 ]。然而,尽管在临床前和临床研究方面投入了持续的努力,但许多癌症仍然致命。提高癌症患者生存率的方法之一是靶向递送抗癌药物。生物医学和生物技术的进步导致了有效药物载体的发现和开发,如脂质体、树枝状聚合物以及金和磁性纳米粒子 [ 3 – 6 ]。这些新型制剂与传统制剂的主要区别在于,它们是否适合开发将药物靶向递送到特定组织、细胞甚至细胞内细胞器的技术。靶向给药的本质在于药物容器(载体)的表面带有经过修饰的药物或分子,这些药物或分子具有可被靶细胞受体识别的功能基团。叶酸修饰是一个典型的例子,因为它能被肿瘤细胞主动吸收[7-9]。抗体和适体是识别靶细胞表面的通用分子[10-12]。得益于基础生物医学研究的进步,细胞的抗原特征变得越来越详细,使我们能够根据细胞表面特征区分不同细胞。口服或肠胃外给药的药物分布在整个身体,只有一小部分到达目标区域。因此,靶向给药方法可以减少剂量
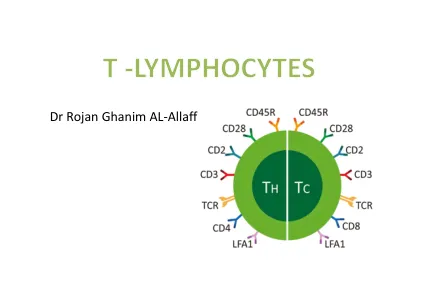
Rojan Ghanim Al -Allaff博士
T淋巴细胞参与了免疫反应和细胞介导的免疫的调节,并帮助B细胞产生抗体。成熟的T细胞表达抗原特异性T细胞受体(TCR)。每个成熟的T细胞都表示与TCR相关的CD3分子。此外,成熟的T细胞通常显示两个辅助分子之一CD4或CD8。TCR/CD3复合物识别靶细胞上与主要组织相容性复合物(MHC)分子相关的抗原(例如病毒感染的细胞)。
人类感觉状神经元培养
人类诱导的多能干细胞(IPSC)(Takahashi和Yamanaka,2006)及其分化为特定靶细胞(例如感觉神经元(ISN)(Chambers等,2009))已发展为有效的疾病模型和药物测试方法。 方法论程序的标准化对于将技术变异性降低到最小至少至关重要,并确保可靠性和可重复性(Lampert等,2020; Volpato和Webber,2020)。 迄今为止,有两个方案可用于区分IS,即基于小分子抑制(Chambers等,2012)和转录因子的过表达(Blanchard等,2015)。 应用小分子方案的应用还导致形态学差异很高的非ISN细胞产生,并且在区分之间计数很高(Schwartzentruber等,2018)。 这种细胞异质性挑战了正确的数据分配和解释。人类诱导的多能干细胞(IPSC)(Takahashi和Yamanaka,2006)及其分化为特定靶细胞(例如感觉神经元(ISN)(Chambers等,2009))已发展为有效的疾病模型和药物测试方法。方法论程序的标准化对于将技术变异性降低到最小至少至关重要,并确保可靠性和可重复性(Lampert等,2020; Volpato和Webber,2020)。迄今为止,有两个方案可用于区分IS,即基于小分子抑制(Chambers等,2012)和转录因子的过表达(Blanchard等,2015)。应用小分子方案的应用还导致形态学差异很高的非ISN细胞产生,并且在区分之间计数很高(Schwartzentruber等,2018)。这种细胞异质性挑战了正确的数据分配和解释。
Yescarta:INN-axicabtagene ciloleucel
作用方式概述:Axicabtagene ciloleucel 是一种自体治疗,通过逆转录病毒转导编码抗 CD19 CAR 的构建体,收获患者自身的 T 细胞并在体外进行基因改造。由于 axicabtagene ciloleucel 是一种基于自体细胞的产品,因此它没有明确的化学性质。用于生产 axicabtagene ciloleucel 的抗 CD19 CAR 构建体包含 3 个区域:1) 源自 FMC63 鼠杂交瘤的抗人 CD19 scFv;2) 人 CD28 的部分胞外结构域和完整的跨膜和胞内信号传导结构域;3) 人 CD3-ζ 分子的细胞质部分,包括其胞内信号传导结构域。 CAR 与 CD19 + 靶细胞结合后,CD3ζ 结构域激活下游信号级联,导致 T 细胞活化、增殖并获得效应功能(例如细胞毒性)。CD28 的胞内信号结构域提供共刺激信号,与主要 CD3ζ 信号协同作用以增强 T 细胞功能,包括 IL2 产生 { Finney 1998 }。这些信号共同刺激 CAR T 细胞增殖并直接杀死表达 CD19 的靶细胞。此外,活化的 T 细胞会分泌细胞因子、趋化因子和其他分子,这些分子可以募集和激活额外的抗肿瘤免疫细胞 { Restifo 2012 }。图 I.1 部分显示了描述 axicabtagene ciloleucel 构建体和产品作用方式的示意图。
针对调整受体FN14的人类融合构建体的治疗疗效和安全性,并包含改良的颗粒b
抽象背景抗体 - 药物结合物是多种疾病的特殊且有用的治疗工具,特别是用于癌症治疗。我们先前表明,丝氨酸蛋白酶颗粒B(GRB),效应分子或T和B细胞与结合结构域的融合允许将细胞毒性有效载荷控制到靶细胞中。这些构建体的产生诱导了高分子聚集体的形成,并可能影响蛋白质的疗效和安全性。方法我们的实验室设计了一种新的FN14靶向融合构建体指定的GRB(C210A)-FC-IT4,其中包含改进的GRB有效载荷,以改善蛋白质生产和保留的生物学活性。我们评估了构建体的酶活性,以及体外的细胞毒性和内在化对靶细胞。我们还评估了体内药代动力学,功效和毒理学参数。结果GRB(C210A)-FC-IT4蛋白在针对FN14阳性人类癌细胞系进行测试时,在纳摩尔范围内表现出高亲和力和选择性细胞毒性。迅速内化到靶细胞,激活caspase级联反应并引起线粒体膜去极化。在小鼠中的药代动力学研究表明,GRB(C210A)-FC-IT4显示出具有快速初始清除率(T1/2α= 0.36小时)的血浆中的双指数清除率(T1/2α= 0.36小时),然后延长了末期末期 - 末期半寿命(T 1/2β= 35小时)。与单独使用媒介物治疗的对照组相比,对确定的皮下A549肺肿瘤建立的小鼠的治疗表现出令人印象深刻的长期肿瘤。带有MDA-MB-231的小鼠用媒介物或GRB(C210A)-FC-IT4构建体(QODX5)处理的MDA-MB-231原位肿瘤异种移植物显示出肿瘤的消退和长期(> 80天)抑制肿瘤生长。小鼠的GRB(C210A)-FC-IT4(100 mg/kg总剂量)的耐受性良好,导致肺癌患者衍生的异种移植模型的肿瘤负担显着减轻。毒性研究表明,治疗小鼠中天冬氨酸转移酶,丙氨酸转移酶或乳酸脱氢酶没有统计学上的显着变化。对经过治疗的小鼠的组织的组织病理学分析尚未证明任何与药物有关的变化。
老年人血液癌的多目标药物
由于抗癌疗法的心血管毒性增加,患有心血管合并症的老年人的血液学恶性肿瘤很难治疗。这组患者平衡效率和耐受性的困难通常会导致临床医生暂停或减少药物的剂量,从而促进疾病的复发。作为靶细胞,对心脏和血管祖细胞的鉴定可能允许开发新的心血管保护策略,以防止抗癌药物免受抗癌药物的影响。在本评论中,由于某些非常有效的靶疗法,我们将重点关注心血管毒性,这些靶向疗法的治疗方法最大,治疗与老年人 - 酪氨酸激酶抑制剂和蛋白酶体抑制剂相关的血液恶性肿瘤。
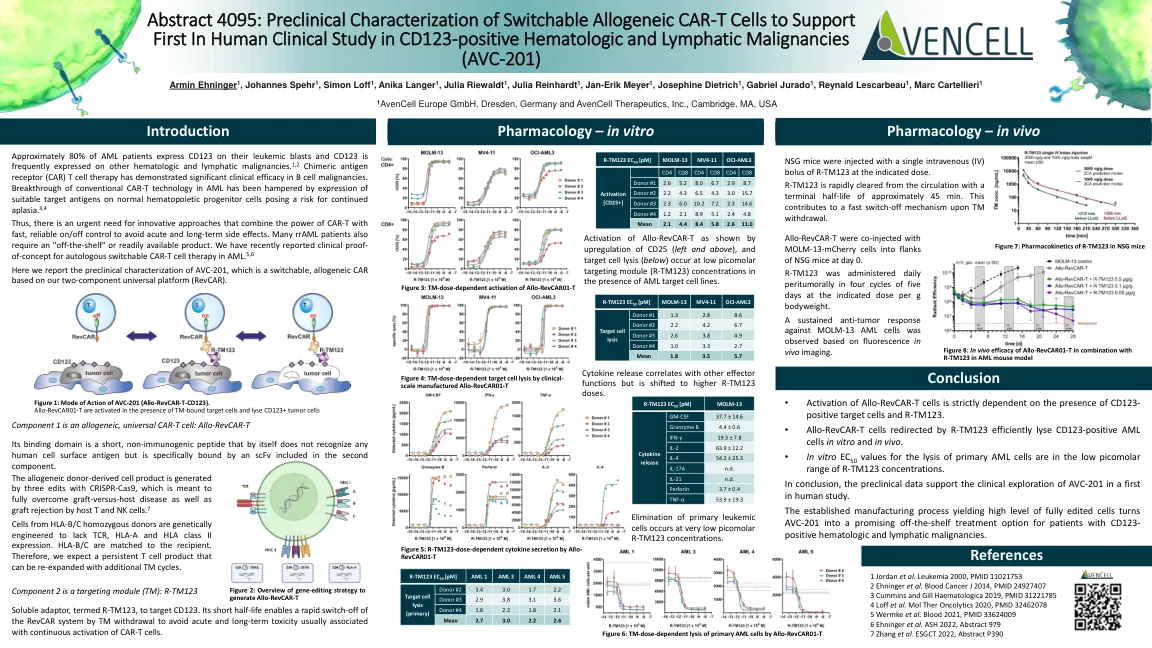
可转换同种异体 CAR-T 的临床前表征...
• Allo-RevCAR-T 细胞的激活严格依赖于 CD123 阳性靶细胞和 R-TM123 的存在。 • 由 R-TM123 重定向的 Allo-RevCAR-T 细胞可在体内和体外有效裂解 CD123 阳性 AML 细胞。 • 体外裂解原代 AML 细胞的 EC 50 值处于 R-TM123 浓度的低皮摩尔范围内。总之,临床前数据支持在首次人体研究中对 AVC-201 进行临床探索。成熟的制造工艺可产生高水平的完全编辑细胞,使 AVC-201 成为 CD123 阳性血液系统和淋巴系统恶性肿瘤患者有前途的现成治疗选择。