XiaoMi-AI文件搜索系统
World File Search SystemVenetoclax
增强的TP53重新激活破坏了MYC转录程序,并克服了急性髓样白血病中的Venetoclax耐药性
肿瘤抑制剂TP53经常在癌症中以突变的方式灭活,并通过抑制其阴性调节剂来重新激活。我们在这里cotarget MDM2和核出口XPO1至p53的最大转录活性。MDM2/XPO1抑制积累了核p53,并引起其转录靶标25至60倍。TP53调节MYC,MDM2/XPO1抑制作用破坏了C- MYC调节的转录组,从而导致急性髓样白血病(AML)的凋亡的协同诱导。出乎意料的是,耐Venetoclax的AML表达高水平的C-MYC,并且容易受到MDM2/ XPO1抑制体内的抑制作用。然而,MDM2/XPO1抑制后持续存在的AML细胞表现出静止和应激反应 - 相关表型。venetoclax克服了这种抗性,如单细胞质量旋转术所示。MDM2,XPO1和BCl2的三重抑制作用非常有效,对抗Venetoclax的AML体内。我们的结果提出了一种新型的,高度可翻译的治疗方法,利用p53重新激活以过度反应,反应适应压力的静脉抗体耐药性。
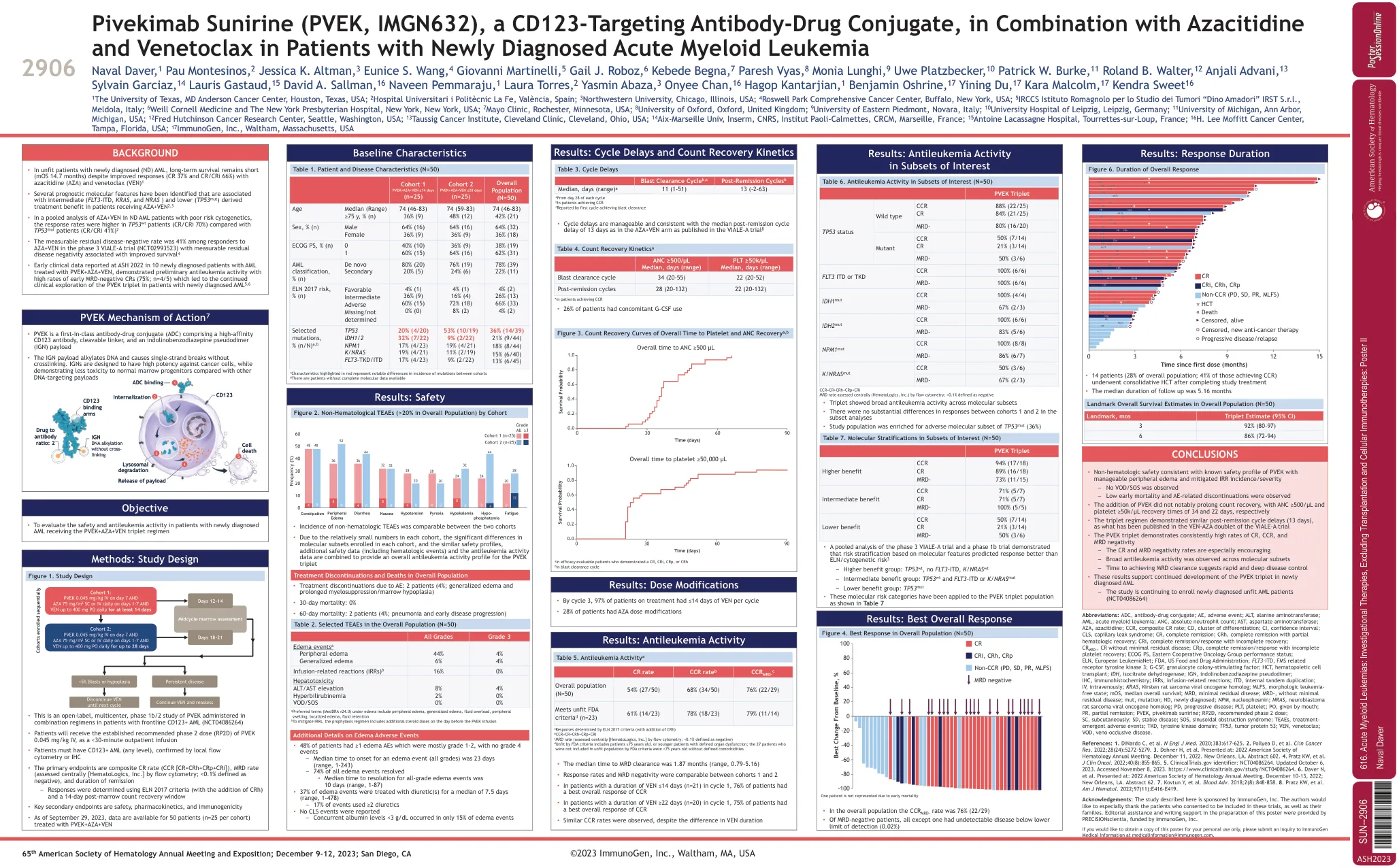
pivekimab sunirine(PVEK,IMGN632),一种CD123靶向抗体 - 药物结合物,与新近D
1美国德克萨斯州休斯敦的德克萨斯大学安德森癌症中心; 2医院Universitari iPolitècnicLaFe,西班牙瓦恩西亚; 3西北大学,美国伊利诺伊州芝加哥; 4罗斯威尔公园综合癌症中心,美国纽约,美国; 5 Irccs iStituto romagnolo per lo Studio dei tumori“ Dino Amadori” Irst S.R.L.,意大利梅尔多拉; 6 Weill Cornell Medicine和美国纽约的纽约长老会医院; 7美国明尼苏达州罗切斯特的梅奥诊所; 8英国牛津大学牛津大学; 9东皮埃蒙特大学,意大利诺瓦拉; 10莱比锡大学医院,德国莱比锡;密歇根大学11号,美国密歇根州安阿伯; 12号弗雷德·哈钦森癌症研究中心,美国华盛顿州西雅图; 13美国俄亥俄州克利夫兰克利夫兰诊所Taussig癌症研究所; 14 AIX-MARSELILL UNIV,INSERM,CNRS,PAOLI-CALMETTES,CRCM,MARSEILLE,法国; 15法国Tourrettes-Sur-Loup的Antoine Lacassagne医院; 16 H. Lee Moffitt癌症中心,美国佛罗里达州坦帕; 17美国马萨诸塞州沃尔瑟姆Immunogen,Inc。
标题:基于急性髓样白血病(AML)的基于Venetoclax(VEN)的抗药性和克隆进化的遗传见解
新获得的muts(中位数1,范围1-6)(图1A)。在20/30分中,获得的MUTS的VAF≥10%。新的mut是转录调节剂(n = 16),信号基因(n = 9)或两者(n = 5)。在TF处,最常见的MUT是FLT3(n = 7; 6 flt3-itd; 1 flt3 n676k),runx1(n = 5),tet2(n = 4),nf1(n = 4)和ptpn11
venetoclax加定解替滨作为老年急性粒细胞性白血病(VEN-DEC GITMO)患者的同种异体造血干细胞移植的桥梁:多中心,单臂,2期试验
方法在意大利的20个Gruppo Italiano Trapianto Midollo Osseo(Gitmo)中心进行了这个多中心,单臂2期试验。患者,新诊断为急性髓样白血病为中间或高风险,ECOG性能状态少于2,并且被认为适合同种HSCT。患者接受口服Venetoclax,为期3天的升高:第1天的100毫克,第2天,从第一周期的第3天开始每天400毫克,然后每个周期的每28天(总共2至4天)(总共2至4天)。div>静脉注射。在第一周期,患者至少被送往医院,至少24小时,而随后的周期可以在外科治疗。在等待同种异体HSCT或第二周期后没有响应或部分响应的人时,还允许另外两个周期。主要终点是在第一次完全缓解期间进行同种异体HSCT的患者的比例,对所有接受研究药物至少一剂的患者进行了评估。这项研究已在ClinicalTrials.gov(NCT04476199,正在进行)和Eudract(2020–002297–26)中注册。
临床试验和观察固定疗程伊布替尼联合维奈克拉用于慢性淋巴细胞白血病 (CLL) 的一线治疗:CAPTIVATE FD 队列的主要分析
1 彼得麦卡勒姆癌症中心,墨尔本,维多利亚州,澳大利亚;2 圣文森特医院,墨尔本,维多利亚州,澳大利亚;3 墨尔本大学,墨尔本,维多利亚州,澳大利亚;4 威尔康奈尔医学院,纽约,纽约州;5 希望之城国家医学中心,杜阿尔特,加利福尼亚州;6 摩尔斯癌症中心,加州大学圣地亚哥分校,加利福尼亚州圣地亚哥;7 莱文癌症研究所,北卡罗来纳州夏洛特;8 莫纳什大学,克莱顿,维多利亚州,澳大利亚;9 威尔莫特癌症研究所,罗彻斯特大学医学中心,纽约州罗彻斯特;10 ASST Grande Ospedale Metropolitano Niguarda,意大利米兰;11 帕多瓦大学,意大利帕多瓦;12 罗格斯大学新泽西州癌症研究所,新泽西州新不伦瑞克;13 米德尔摩尔医院,新西兰奥克兰;14 弗林德斯大学与医学中心,南澳大利亚州贝德福德公园,澳大利亚; 15 Hospital de la Santa Creu i Sant Pau,巴塞罗那自治大学,巴塞罗那,西班牙; 16 Pharmacyclos LLC,艾伯维旗下公司,加利福尼亚州桑尼维尔; 17 德克萨斯大学 MD 安德森癌症中心白血病科,德克萨斯州休斯顿; 18 圣拉斐尔生命健康大学,米兰,意大利;和 19 IRCCS Ospedale San Raffaele,意大利米兰
校准的释放IL15表达二价CD33和/或FLT3逻辑门电路电路CAR-NK细胞疗法(来自Senti-202基因电路)in venetoclax
背景:Venetoclax(VEN)作为联合疗法提高了急性髓样白血病(AML)患者的反应率和总体存活率。然而,一旦AML复发,预后就有5.3个月的中位数生存期(Brandwein,2020)。虽然嵌合抗原受体(CAR)细胞疗法已彻底改变了B-细胞恶性肿瘤的治疗局势,但这种AML疗法的开发一直在挑战,部分原因是该疾病的异质性。当前,单个AML靶标的很少在AML亚群中始终表达。此外,这些AML靶标的表达不仅限于肿瘤细胞群,通常会导致对健康细胞群体的肿瘤毒性。Senti-202使用或不使用逻辑门控以及校准的IL-15细胞因子来克服这些挑战。
与新诊断的披风细胞淋巴瘤患者中Venetoclax,Lenalidomide和Rituximab的结合可诱导高反应率和MRD不可检测性
S.斋月5,E。Zucca6,T。Instant 7,Q.。S.斋月5,E。Zucca6,T。Instant 7,Q.。
MALT1蛋白酶抑制克服BTK抑制剂的耐药性,并在B细胞淋巴瘤和白血病模型中与Venetoclax显示协同活性
结果:机械研究表明,ABBV-MALT1有效抑制了BCR途径的信号转导,并降低了非GCB DLBCL细胞系中NF-K B基因的活化,从而导致细胞周期停滞并减少生存能力。体内,该化合物的口服给药表明在几种B细胞肿瘤模型中,包括对Bruton的酪氨酸激酶(BTK)抑制剂的非GCB DLBCL模型。nf-k b靶基因包括促生物的家族成员bcl-x l和bcl2-a1,有助于调节内在凋亡途径。作为ABBV-MALT1诱导的NF-K B途径的抑制导致这些基因的下调,我们假设相关的肿瘤模型将越来越依赖于生存的家族成员Bcl-2。为了检验该假设,在DLBCL的细胞系和患者衍生的异种移植模型中均进行了ABBV-MALT1和选择性BCL-2抑制剂Venetoclax的组合研究。在此表明,在体内测试的所有模型中,ABBV-MALT1和VENETOCLAX的施用会导致剧烈的抗肿瘤活性。这种疗效也转化为原发性患者CLL细胞的体外,与单独的任何一种药物相比,该组合赋予了更大的凋亡水平。
评论文章 BH3 类似物维奈克拉在急性髓系白血病治疗中的作用日益增强 Elvira Pelosi、Germana Castelli 和 Ugo
摘要。尽管近年来取得了进展,急性髓系白血病 (AML) 仍然是一种预后不良的疾病,尤其是对于无法耐受强化化疗的老年 AML 患者。维奈克拉 (VEN) 是一种强效的 BH3 类似物,靶向抗凋亡蛋白 BCL-2,诱导白血病细胞凋亡,已被证明是一种有希望的治疗方法,适用于不适合诱导化疗的新诊断、复发和难治性 AML 患者。使用维奈克拉和低甲基化剂(阿扎胞苷或地西他滨)或低强度化疗的联合治疗在新诊断患者中显示出不同的反应率,对 NPM1、IDH1-IDH2、TET2 和 RUNX1 突变的患者反应性高,对 FLT3、TP53 和 ASXL1 突变、复杂核型和继发性 AML 的患者反应性低。难治性/复发性疾病患者对基于 Venetoclax 的方案反应较差。然而,在大多数患者中,反应仅持续有限时间,并且经常观察到耐药性的产生。因此,了解耐药机制对于制定新策略和确定合理的药物组合方案至关重要。在这种情况下,两种策略似乎很有希望:(i) 基于 Venetoclax、低甲基化剂(或低剂量化疗)和针对白血病细胞特定基因改变的药物(即 FLT3 突变 AML 中的 FLT3 抑制剂)或改变的信号通路的联合给药的三联疗法;(ii) 基于两种 BH3 模拟物(即 BCL-2 +MCL-1 模拟物)和低甲基化剂的给药的联合疗法。关键词:BH3;急性髓系白血病。引文:Pelosi E.、Castelli G.、Testa U. BH3 类似物 Venetoclax 在急性髓系白血病治疗中的作用日益增强。Mediterr J Hematol Infect Dis 2022,14(1): e2022080,DOI:http://dx.doi.org/10.4084/MJHID.2022.080 出版日期:2022 年 11 月 1 日 收到日期:2022 年 9 月 17 日 接受日期:2022 年 10 月 17 日 这是一篇根据知识共享署名许可条款分发的开放获取文章 (https://creativecommons.org/licenses/by-nc/4.0),允许在任何媒体中不受限制地使用、分发和复制,前提是对原始作品进行适当的引用。联系人:Ugo Testa。意大利罗马高级卫生研究院肿瘤学系。电子邮箱:ugo.testa@iss.it 简介。细胞凋亡是健康和疾病中的一个重要生物过程,受 BCL-2 家族蛋白的调控。
KME-0584,一种高度有效的IRAK1/irak4/panflt3抑制剂,是低甲基化剂和耐Venetoclax抗性AML/MDS
NF-κB报告基因测定。根据THP-1-蓝色NF-κB细胞和Quanti-Blue试剂制造方案(Invivogen)进行。菌落成型单元(CFU)。主要的AML患者样品是从发现生命科学(DLS)获得的,并在甲基纤维素测定中进行了测试。生化和基于细胞的激酶抑制测定。激酶抑制数据和基于细胞的激酶测定是使用RBCHotSpot®激酶和Nanobret®分析获得的,分别在Rectionbio(Malvern,PA)上进行。结合动力学测定。使用KineticFinder®TR-FRET分析在酶logic上进行。异种移植。生存分析在用Molm14 Flt3-ITD(D835Y)细胞的NSG-SGM3小鼠中进行。药代动力学筛查和离子通道面板。测试是在Pharmaron进行的。rnaseq。THP-1细胞在液体培养中进行24小时。 提取总RNA,并以每个样品的30m读取进行RNASEQ。 统计分析。 使用GraphPad Prism绘制了所有数据,并使用t检验确定统计显着性。THP-1细胞在液体培养中进行24小时。总RNA,并以每个样品的30m读取进行RNASEQ。统计分析。使用GraphPad Prism绘制了所有数据,并使用t检验确定统计显着性。