XiaoMi-AI文件搜索系统
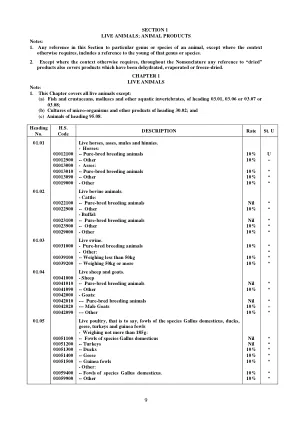
World File Search System第 1 部分 活体动物;动物产品 注释
沙丁鱼(Sardina pilchardus、Sardinops spp.)、小沙丁鱼(Sardinella spp.)、鲂鱼或鲱鱼(Sprattus sprattus)、鲭鱼(Scomber scombrus、Scomber australasicus、Scomber japonicus)、印度鲭鱼(Rastrelliger spp.)、鲭鱼(Scomberomorus spp.)、鲭鱼和竹荚鱼(Trachurus spp.)。鲹鱼、鲹鱼(Caranx spp.)、海鲡(Rachycentron canadum)、银鲳(Pampus spp.)、秋刀鱼(Cololabis saira)spp.鲭鱼(Decapterus spp.)、毛鳞鱼(malloutus villosus)、剑鱼(Xiphias gladius)、卡瓦卡瓦鱼(euthynnus affinis)、鲣鱼(Sarda spp.)、马林鱼、旗鱼、旗鱼(Istiophoridae),但不包括子目 0302.91 至 0302.99 的可食用鱼内脏:
保护美国动物健康-动物疾病预防和...
为紧急情况做准备与预防紧急情况同样重要。这就是为什么 APHIS 与各级利益相关者合作,以确保美国准备好应对当今畜牧业面临的最严重的动物健康威胁。通过国家动物疾病防范和应对计划,APHIS 与各州、部落、生产者组织、大学和其他机构合作,开展项目,以增强地方、区域和国家预防、准备和应对动物疾病爆发的能力。这项工作对于强大的美国保障体系、安全的食品供应和美国动物的持续健康至关重要。自 2019 年以来,APHIS 已提供超过 4000 万美元来支持 180 多个项目。这些项目包括:
纸的类型(文章
摘要:主要的视觉皮层(V1)是研究最多的大脑区域之一,并被人类和非人类灵长类动物中的专门和层压层的第4层征收。然而,旨在统一啮齿动物和灵长类动物的V1皮层层和边界定义的研究非常有限。本文试图识别和统一分子标记和连接模式,这些分子标记和连接模式可以始终如一地将V1的相应皮层和跨哺乳动物物种和年龄之间的骨质联系起来。V1至少具有至少两个额外的独特层(L3B2和L3C)和两个第4层(L4A和L4B)的子层。在所有检查的物种中,V1的第4和3B层从(背侧)侧向基因核接收强烈的输入,而V1大多被次级视觉皮层包围,除了V1直接缩小prostriata区域的一个位置。灵长类动物V1的边界也可以在胎龄中清楚地鉴定出使用基因标记。在啮齿动物中,识别V1的新型后外侧延伸,该延伸表达了V1标记基因并从侧向基因核中接收强输入。该V1延伸被标记为文献和脑图中的后肾上腺皮质和内侧次生皮层。啮齿动物和灵长类动物V1的第6层起源于皮质胸膜伸向对侧向遗传,背侧和网状丘脑核的侧面,以及与地形组织的后期脉络膜结构。最后,直接的geniculo-extrastriate(尤其是强大的geniculo-prostriata)预测可能是V1病变后盲目的主要因素。与啮齿动物,灵长类动物和人类相比,V1至少具有两个独特的中层层,而其他层则在物种之间相当,并且显示保守的分子标记物以及与视觉丘脑的相似连接,并且仅具有微妙的差异。
实验动物
摘要:电穿孔动物基因敲除系统技术(TAKE)是一种简单有效的方法,利用成簇的规律间隔短回文重复序列(CRISPR)/CRISPR 相关蛋白 9(Cas9)系统生成转基因小鼠。为了增强电穿孔在小鼠基因编辑中的多功能性,针对玻璃化冷冻小鼠胚胎优化了电条件,并将其应用于广泛使用的近交系(C57BL/6NCr、BALB/cCrSlc、FVB/NJcl 和 C3H/HeJJcl)的新鲜胚胎。电脉冲设置(穿孔脉冲:电压,150 V;脉冲宽度,1.0 ms;脉冲间隔,50 ms;脉冲数,+4;转移脉冲:电压,20 V;脉冲宽度,50 ms;脉冲间隔,50 ms;脉冲数,±5)对于玻璃化冷冻加温的小鼠胚胎是最佳的,其可以有效地将 gRNA/Cas9 复合物递送到受精卵中而无需透明带变薄过程并编辑目标位点。这些电条件在广泛使用的近交系小鼠中有效地产生了转基因小鼠。此外,使用间隙为 5 mm 的电极进行电穿孔可以在 5 分钟内引入超过 100 个胚胎,而无需特殊的预处理和复杂的技术技能,例如显微注射,并且在产生的后代中表现出较高的胚胎发育率和基因组编辑效率,从而快速高效地产生基因组编辑小鼠。本研究中使用的电条件用途广泛,可以更轻松高效地生成转基因小鼠,有助于了解人类疾病和基因功能。关键词:CRISPR/Cas9、电穿孔、冻融胚胎、基因组编辑
实验动物
摘要:自发性hhy小鼠出现脑积水和皮层下异位,且已鉴定出Ccdc85c基因突变。为了比较Ccdc85c在不同物种中的作用,我们建立了Ccdc85c KO大鼠并研究了其病理表型。Ccdc85c KO大鼠是通过转录激活因子样效应核酸酶(TALEN)的基因组工程改造而来的。KO大鼠的Ccdc85c基因约350 bp缺失,缺乏CCDC85C蛋白表达。KO大鼠表现出非阻塞性脑积水、皮层下异位和颅内出血。KO大鼠具有许多与hhy小鼠相似的病理特征。这些结果表明CCDC85C在大鼠大脑发育中起着重要作用,且CCDC85C在大鼠和小鼠大脑中的作用相似。关键词: Ccdc85c, 脑积水, 大鼠, 皮层下异位
小分子GAT1508激活了脑特异性GIRK1/2通道异构体,并促进了啮齿动物中有条件的恐惧灭绝
G蛋白 - 内向矫正的K(Girk)通道是G I/O-蛋白质 - 信号系统的靶标,可抑制细胞的兴奋性细胞。Girk通道作为同型(GIRK2和GIRK4)或具有非功能同源亚基(GIRK1和GIRK3)的异驱动器存在。尽管它们与多个条件有关,但缺乏区分不同少女通道亚型的选择性girk药物阻碍了对其精确的生理相关性和治疗性潜力的研究。在这里,我们报告了大脑GIRK1/2通道的高度特异性,有效且有效的激活因子。使用化学筛选和电生理测定法,我们发现该激活剂,溴硫氰基取代的小分子GAT1508是针对脑表达的GIRK1/2通道的特异性的,而不是心脏GIRK1/4通道。计算模型预测了通过实验性诱变实验验证的GAT1508结合位点,提供了有关基于尿素的化合物如何与通道激活所需的遥远GIRK1残基的见解。此外,我们还提供了计算和经验证据,表明GAT1508是通道 - 磷脂酰肌醇4,5-双磷酸磷酸盐的变构调节剂。通过脑部滑动电生理学,我们表明,亚阈值GAT1508浓度直接刺激基底外侧杏仁核(BLA)和potentiate baclofen诱导的电流中的Girk电流。值得注意的是,GAT1508在啮齿动物中有效地熄灭了条件恐惧,缺乏心脏和行为副作用,这表明其在创伤后应激失调的药物治疗中的潜力。总而言之,我们的发现表明小痣 -
一种跨不同啮齿动物物种进行基因编辑的 AAV-CRISPR/Cas9 策略:以神经催产素受体为目标作为概念验证
神经科学的一个主要问题是,动物临床前研究的结果很难转化为临床结果。比较神经科学可以通过研究多个物种来克服这一障碍,以区分物种特异性和神经回路功能的一般机制。神经回路的定向操纵通常依赖于基因解剖,而这种技术的使用仅限于少数模型物种,限制了它在比较研究中的应用。然而,基因组学的不断进步使得越来越多的物种可以进行基因解剖。为了展示比较基因编辑方法的潜力,我们开发了一种病毒介导的 CRISPR/Cas9 策略,预计该策略将靶向 80 多种啮齿动物的催产素受体 (Oxtr) 基因。该策略专门降低了所有评估物种 (n = 6) 的 OXTR 水平,而不会引起严重的神经元毒性。因此,我们表明基于 CRISPR/Cas9 的工具可以同时在多个物种中发挥作用。因此,我们希望鼓励比较基因编辑并提高神经科学研究的可转化性。
产前饮食限制啮齿动物前额皮质中胰岛素与 Netrin-1/DCC 引导线索通路调节之间的关系
1 加拿大魁北克省蒙特利尔麦吉尔大学神经科学综合项目; 2 加拿大魁北克省蒙特利尔麦吉尔大学 Ludmer 神经信息学和心理健康中心; 3 加拿大魁北克省蒙特利尔麦吉尔大学道格拉斯心理健康大学研究所; 4 美国新泽西州新不伦瑞克罗格斯大学细胞生物学和神经科学系; 5 加拿大魁北克省蒙特利尔麦吉尔大学精神病学系; 6 巴西阿雷格里港南里奥格兰德联邦大学医学院儿童和青少年健康研究生课程; 7 巴西阿雷格里港南里奥格兰德联邦大学基础健康科学研究所神经科学研究生课程; 8 巴西阿雷格里港南里奥格兰德联邦大学医学院精神病学和行为科学研究生课程和 9 加拿大魁北克省蒙特利尔麦吉尔大学神经病学和神经外科系