XiaoMi-AI文件搜索系统
World File Search SystemMIP/VFC 推出 Priorix 和 Vaxneuvance
• 0.5 毫升预充式注射器 • 使用前剧烈摇晃 • 肌肉注射 • 在 2、4、6 和 12-15 个月大时分 4 剂给药 • 12-15 个月剂量需要在注射第 3 剂后至少 2 个月给药。 • 将原包装存放在 36°F 至 46°F(2°C 至 8°C)的冰箱中
印度血清研究所私人有限公司 MenAfriVac 5 微克...
产品特性总结 1 药品名称 MenAfriVac 脑膜炎球菌 A 结合疫苗(冻干) 5 mcg 2 定性和定量组成 [脑膜炎球菌 A 多糖与破伤风类毒素载体蛋白结合] 每剂量 0.5 mL 含: 脑膜炎球菌 A 多糖 5 mcg 破伤风类毒素(载体蛋白)5 至 16.5 mcg 用稀释剂重构脑膜炎球菌 A 结合疫苗 剂量:0.5 mL 肌肉注射 有关辅料的完整列表,请参见第 6.1 节。稀释剂:每支安瓿含有稀释剂,佐剂为磷酸铝 (Al +++ )(每人单剂量 Al +++ 的含量不超过 1.25 毫克),防腐剂为硫柳汞 (0.01%)。稀释剂为白色略微不透明的均匀悬浮液,装于 5 毫升安瓿中。 3 剂型 注射剂,注射用粉剂 4 临床特点 4.1 治疗适应症 3 至 24 个月大的幼儿主动免疫,以预防 A 组脑膜炎奈瑟球菌引起的侵袭性脑膜炎球菌病。它不能预防其他形式的侵袭性疾病,包括由其他脑膜炎球菌群(如 B、C、W135、Y、X 组)、b 型流感嗜血杆菌、肺炎链球菌等引起的化脓性脑膜炎。它也不能预防由其他生物(如病毒、真菌、分枝杆菌等)引起的脑膜炎。4.2 剂量和给药方法对于 3 至 9 个月大的儿童,MenAfriVac 5 mcg 应分 2 剂给药,间隔至少 3 个月。9 至 24 个月大的儿童只需接种一剂。该疫苗仅供肌肉注射。MenAfriVac 5 mcg(脑膜炎球菌 A 结合疫苗 5 微克)应通过深部肌肉注射给药,最好注射到三角肌或大腿前外侧。疫苗不得皮下或静脉注射,不得与其他疫苗混合在同一注射器中。若同时注射,应使用不同的注射部位。
COVID-19 疫苗公告 9
标记注射部位。图中浅色三角形表示三角肌肌肉注射部位。建议注射部位位于三角形中间。用拇指和食指绷紧皮肤,不要将皮肤揉成一团。以 90° 角快速插入针头。缓慢注射。快速拔出针头,用棉绒或纱布轻轻按压几秒钟
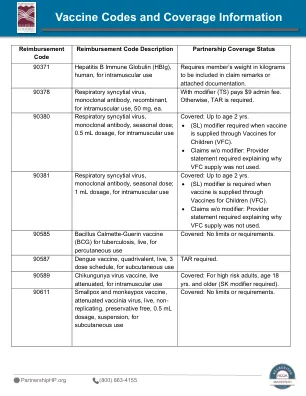
疫苗代码和覆盖范围信息
覆盖范围: • 年龄 <19 岁:当疫苗通过儿童疫苗 (VFC) 提供时,需要 (SL) 修饰符。 • 不带修饰符的索赔:需要提供供应商声明,解释为何未使用 VFC 供应。 90697 白喉、破伤风类毒素、无细胞百日咳疫苗、灭活脊髓灰质炎病毒疫苗、乙型流感嗜血杆菌 PRP-OMP 结合疫苗和乙肝疫苗 (DTaP-IPV-Hib-HepB),用于肌肉注射
最终记分卡 团队编号 ______ 牛加工......
• 如果第一次尝试时注射不正确,则无法重新注射产品 • 肌肉注射而非皮下注射 • 注射在颈后,注射位置太高、太低或太靠前 • 注射疫苗的针头与抽取疫苗的针头相同 • 疫苗未正确水化 • 注射器未在梭菌疫苗和呼吸道疫苗之间切换 可能扣分(每次扣 1 分)
用于癌症联合治疗的有机和无机纳米药物
Abraxane 紫杉醇 白蛋白 NP 美国 (2005) 静脉注射 癌症 Doxil 阿霉素脂质体 美国 (1995) 静脉注射 癌症 Feraheme N/A 聚合物涂层氧化铁 NP 美国 (2009) 静脉注射 贫血 Feridex IV N/A 葡聚糖涂层氧化铁 NP 美国 (1996) 静脉注射 MRI 造影剂 Genexol PM 紫杉醇 聚合物胶束 韩国 (2007) 静脉注射 癌症 Marqibo 长春新碱脂质体 美国 (2012) 静脉注射 白血病 Mepact Mifamurtide 脂质体 欧洲 (2009) 静脉注射 骨肉瘤 SPIKEVAX mRNA 脂质 NP 美国 (2022) 肌肉注射 新冠疫苗 COMIRNATY mRNA 脂质 NP 美国 (2021) 肌肉注射 新冠疫苗 Nano Therm N/A 氧化铁NP 欧洲 (2010) 肿瘤内癌症 Onivyde 伊立替康脂质体 美国 (2015) 静脉内癌症 ONPATTRO siRNA 脂质 NP 美国 (2018) 静脉内多发性神经病变 VISUDYNE Vertepor n 脂质体 美国 (2000) 静脉内黄斑变性
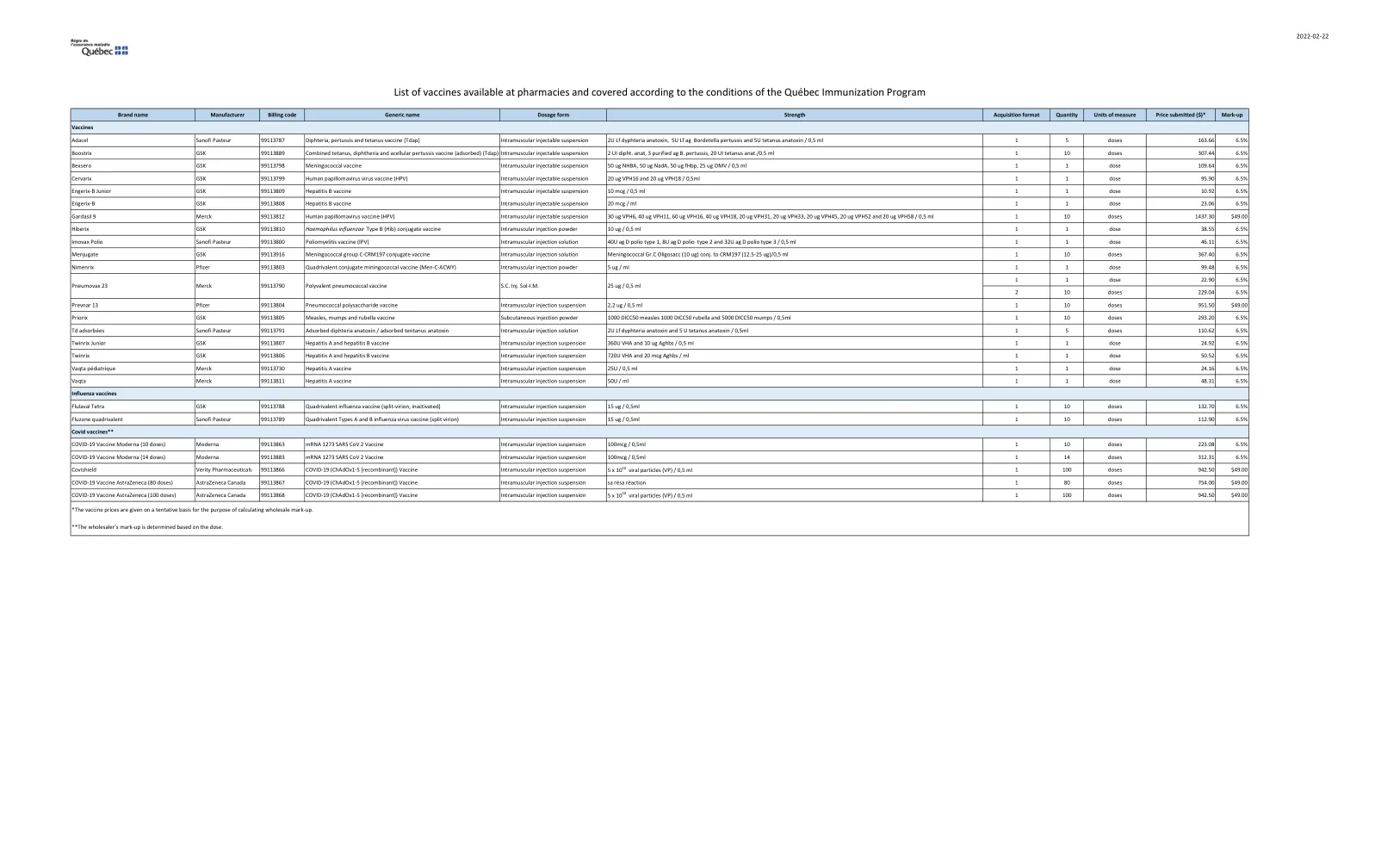
药房有售且符合魁北克免疫计划条款的疫苗清单
Gardasil 9 Merck 99113812 人乳头瘤病毒疫苗 (HPV) 肌肉注射悬浮液 30 ug VPH6、40 ug VPH11、60 ug VPH16、40 ug VPH18、20 ug VPH31、20 ug VPH33、20 ug VPH45、20 ug VPH52 和 20 ug VPH58 / 0.5 ml 1 10 剂 1437.30 49.00 美元
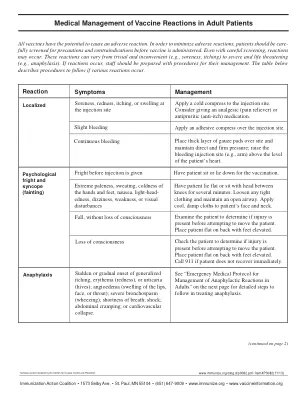
成年患者疫苗反应的医学管理
a. 第一线治疗:肌肉注射 1:1000 稀释的肾上腺素水溶液,0.01 mL/kg/剂量(成人剂量范围为 0.3 mL 至 0.5 mL,最大单剂量为 0.5 mL)。 b. 第二线治疗:对于荨麻疹或瘙痒,您也可以口服或肌肉注射苯海拉明;标准剂量为 1-2 mg/kg,最大单剂量可达 50 mg。 4. 密切监测患者直至急救人员到达。如有必要,进行心肺复苏术 (CPR),并保持呼吸道通畅。除非患者呼吸困难,否则让其保持仰卧姿势(平躺)。如果呼吸困难,可以抬高患者的头部,前提是血压足以防止失去意识。如果血压低,抬高双腿。每 5 分钟监测一次血压和脉搏。 5. 如果急救人员尚未到达且症状仍然存在,则根据患者的反应,每 5-15 分钟重复注射一次肾上腺素,最多注射 3 次。 6. 记录所有生命体征、给患者注射的药物,包括时间、剂量、反应、给患者注射药物的医务人员姓名以及其他相关临床信息。 7. 通知患者的初级保健医生。
马匹疫苗接种
• 狂犬病:我们好奇的马可能会在马厩或牧场接触野生动物。狂犬病毒通过唾液传播,在威斯康星州最常见的是蝙蝠和臭鼬。其他哺乳动物也可能携带狂犬病毒。这种疫苗可以很好地预防致命疾病。一旦感染,症状出现的时间各不相同,可能长达数月。症状可能包括绞痛、动作不协调、唾液分泌过多、抑郁、自残或攻击性。一旦出现症状,它们会迅速发展直至死亡。疑似患有狂犬病的马会被人道地安乐死,并在死后进行检测。这种疫苗每年肌肉注射一次。不需要加强疫苗接种。• 莱姆病:伯氏疏螺旋体威斯康星州大量黑腿蜱或“鹿”蜱携带导致莱姆病的细菌。目前市场上没有用于预防马莱姆病的疫苗。研究表明,使用犬疫苗可以保护马群免受莱姆病的侵害。症状可能包括轻度跛行、关节痛、皮肤/肌肉压痛、不适和一般行为不当。这种疾病的长期影响尚不清楚。这种疫苗每 6 个月进行一次肌肉注射。首次接种时,需要在初始剂量后 4-6 周注射第二剂加强剂。
VaxiRab N - 狂犬病疫苗,人免疫球蛋白
3. 剂型和规格 剂型:冻干疫苗,用随附的注射用无菌水溶解,IP 注射,用于肌肉注射或皮内注射。 规格:灭活狂犬病毒(Pitman Moore 株)-效力 ≥ 2.5 IU 4. 临床特点 4.1 治疗指征 狂犬病主动免疫: (a) 暴露前预防(预防性,暴露前):在可能感染狂犬病之前进行免疫,特别是对于兽医、兽医学学生、动物饲养者、猎人、林业工人、动物处理者、屠夫、狂犬病研究实验室人员等,或在访问狂犬病流行区(狂犬病感染区)之前。 (b) 暴露后预防(暴露后):接触患有狂犬病或疑似患有狂犬病的动物后,或接触接种狂犬病的尸体后的治疗 4.2 剂量和给药方法 将稀释剂(1 ml 注射用无菌水 IP)加入冻干疫苗中。在重新配制之前和之后,应目视检查疫苗是否有任何异物颗粒和/或外观变化。如果疫苗的外观发生任何变化,则不得使用疫苗。用无色透明稀释剂重新配制冻干粉后,会产生透明溶液。 A) 暴露前疫苗接种:暴露前疫苗接种适用于高风险人群(实验室人员、兽医、屠宰场工人、在疫区工作的警察、动物贩卖者、动物饲养员、检疫站工作人员、动物学家以及疫区的猎场看守人、猎人、护林员、林业工人等)。暴露前疫苗接种也适用于在疫区停留时间较长(数月)并因此经常接触潜在狂犬病动物(狗、猫、狐狸、蝙蝠或其他有狂犬病风险的动物)的人员(包括儿童)。肌肉注射途径暴露前基本免疫包括在第 0、7 和 28 天(或第 21 天)进行三次肌肉注射,每次注射一剂(1 毫升),注射到三角肌,或幼儿的大腿前外侧,但绝不注射到臀部。最后一次接种后 2-3 周检查血清转化情况。对于疑似免疫抑制(药物或疾病)的人和具有高职业暴露风险的人,常规检查是必要的。对于具有高职业风险的人,应每 6 个月检查一次中和抗体滴度;对于所有其他具有持续风险的人,应每年测定一次滴度。如果滴度不足(≤ 0.5 lU/mL),则应进一步给予加强剂量,直至疫苗接种成功。B) 未完成或未接种疫苗的人的暴露后措施:• 伤口处理作为急救,应使用肥皂和水或清洁剂彻底清洁伤口。在某些情况下可能需要破伤风加强针和抗生素治疗。• 使用 VaxiRab N ® 肌肉注射途径主动接种疫苗在第 0、3、7、14 和 28 天,将 1 ml 剂量肌肉注射到三角肌或幼儿大腿前外侧,但切勿注射到臀部,共 5 次。(世卫组织 2005 年技术报告系列,第 931 号)应通过测量第 14 天的滴度来检查高危免疫功能低下人群中疫苗接种(≥ 0.5 lU/mI)的成功率。滴度低于 0.5 IU/ml 的患者应尽快同时再注射两剂疫苗。应进一步检查抗体滴度,并根据需要注射更多剂量的疫苗。