机构名称:
¥ 12.0
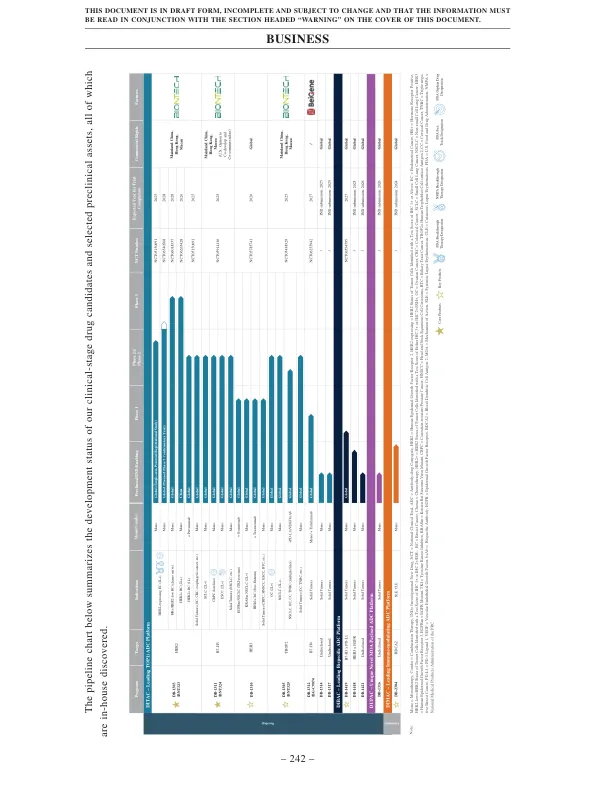
我们力争走在 ADC 技术和开发战略的前沿。我们拥有 12 种内部发现的 ADC 候选药物,这证明了我们在 ADC 创新方面的实力,包括:(i) 六种临床阶段 ADC,具有广泛适应症的潜力,且具有未满足的医疗需求,根据 Frost & Sullivan 的数据,每种药物在整体或主要适应症开发进度方面均位居全球临床最先进的行列;(ii) 两种下一代双特异性 ADC(“BsADC”)和一种自身免疫 ADC,预计将于 2024 年至 2026 年进入临床阶段;以及 (iii) 多种其他临床前 ADC。我们的三种临床阶段产品,包括核心产品 DB-1303/BNT323 和 DB-1311/BNT324 以及关键产品 DB-1305/BNT325,已获得美国食品药品监督管理局(“ FDA ”)的快速通道认证,DB-1303 已获得 FDA 和国家药品监督管理局(“ NMPA ”)针对某些适应症的突破性治疗认证。DB-1303 是一种后期临床阶段 HER2 ADC 候选药物,目前有两项正在进行的注册试验和一项潜在的注册研究,第一项适应症(表达 HER2 的子宫内膜癌(“ EC ”)预计最早将于 2025 年向 FDA 提交加速批准申请。
模数转换器