XiaoMi-AI文件搜索系统
World File Search SystemTempus 遗传性癌症检测
2 Horton C、Hoang L、Grzybowski J 等人。扩大配对 DNA 和 RNA 测序的范围:来自遗传性癌症队列的 450,000 名连续个体的结果。口头报告于:美国人类遗传学会年会;2024 年 11 月 6-8 日;科罗拉多州丹佛市。
遗传性癌症测试申请表2025.01.07
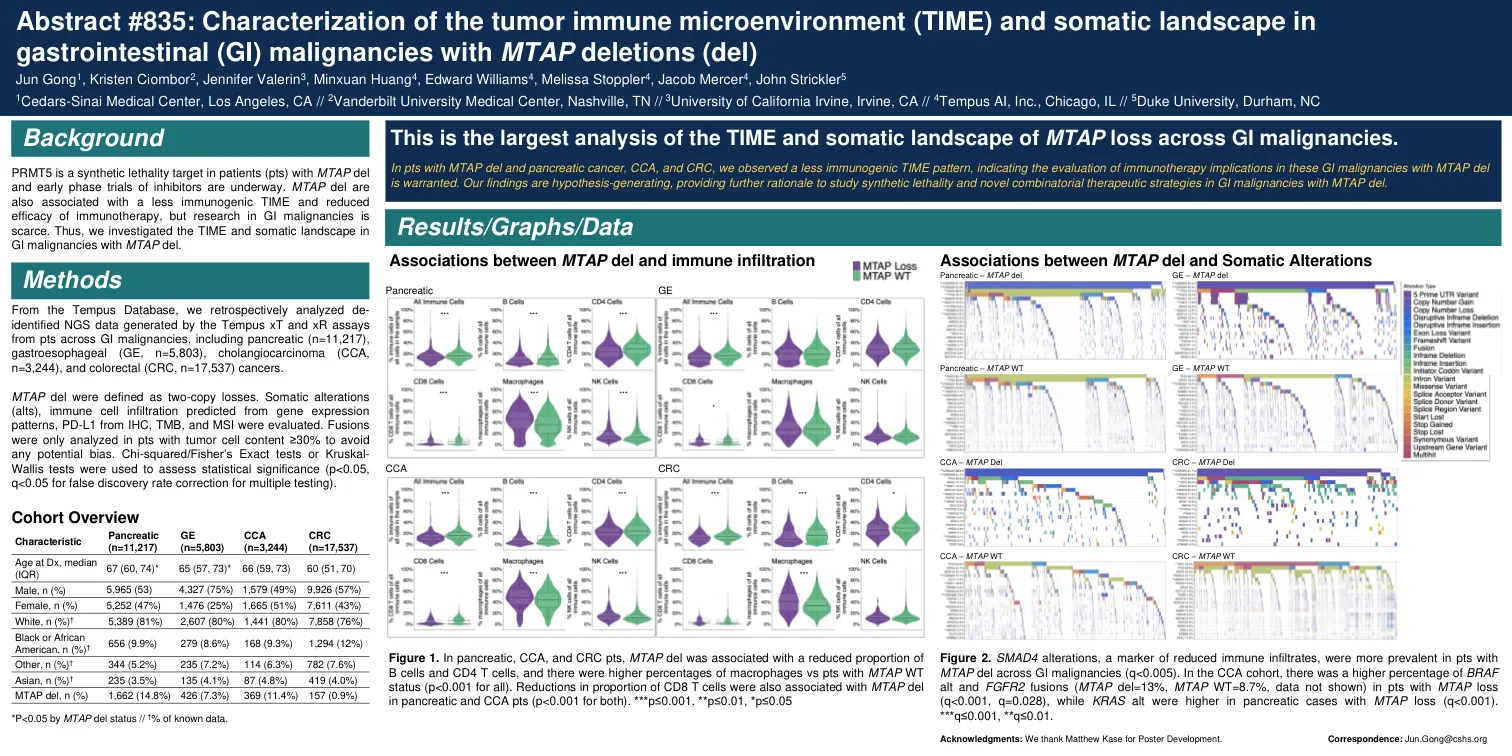
mtap del定义为两拷贝损失。体细胞改变(ALTS),从IHC,TMB和MSI的基因表达模式,PD-L1预测的免疫细胞浸润。融合,以避免任何潜在的偏见。卡方/Fisher的精确测试或Kruskal-Wallis检验用于评估统计显着性(p <0.05,Q <0.05,用于用于多次测试的错误发现率校正)。
通过protac样诱导剂的侵蚀性癌症
(未通过同行评审认证)是作者/资助者。保留所有权利。未经许可就不允许重复使用。此预印本版本的版权持有人于2024年12月29日发布。 https://doi.org/10.1101/2024.12.28.630572 doi:Biorxiv Preprint
肝细胞癌核中原发性癌症的流行病学概况......
乌贝兰迪亚-MG 一家参考医院中枢神经系统基底神经节原发性癌症的流行病学概况 摘要 在本研究中,我们提出一项建议,以描述 2000 年 1 月至 2017 年 12 月期间在乌贝兰迪亚联邦大学临床医院 (HC-UFU) 诊断出的中枢神经系统 (CNS) 癌症患者的临床和流行病学概况,以及同一时期在巴西的情况。我们将对医院癌症登记系统 (SisRHC) 中登记的病例进行评估;以及根据文献书目审查对收集到的这些数据进行分析,通过预定的研究数据库,按照研究人员建立和描述的分析标准进行。 关键词:癌症、中枢神经系统、流行病学。
遗传性癌症及癌症诊断后的基因检测
遗传性癌症具有家族遗传性。当保护我们免受癌症侵害的基因发生改变而无法发挥作用时,就会发生这种现象。这种改变被称为致病变异、可能致病变异、有害变异,有时也被称为“突变”。致病变异会增加罹患某些类型癌症的风险。但是,并非每个携带致病变异的人都会患上癌症。
基因检测:遗传性癌症易感性
重要信息 – 请在使用本政策前阅读 这些服务可能包含在所有 Medica 计划中,也可能不包含在内。 保险范围受适用联邦或州法律的要求约束。 有关其他具体保险信息,请参阅会员的计划文件。 如果政策要求与会员的计划文件存在差异,则将使用会员的计划文件来确定保险范围。 对于 Medicare、Medicaid 和其他政府计划,除非这些计划需要不同的保险范围,否则将适用本政策。 会员可以拨打会员身份证上列出的电话号码联系 Medica 客户服务部,以更具体地讨论他们的福利。 提供商如果对此 Medica 保险政策有疑问,可以拨打免费电话 1-800-458-5512 联系 Medica 提供商服务中心。 Medica 保险政策不是医疗建议。 会员应咨询适当的医疗保健提供商,以获得所需的医疗建议、护理和治疗。 概述
遗传性癌症申请
通过签署此同意书,我同意对我的医疗保健提供者要求的所有基因检测承担全部和完全的财务责任。对于保险账单,我特此授权 Baylor Genetics 代表我向我的健康保险计划开具账单,并进一步授权 Baylor Genetics 向我的保险公司披露开具账单所合理需要的任何信息。此外,我指定 Baylor Genetics 作为我的指定代表,负责对我的保险公司拒绝提供福利的行为提出上诉。我不可撤销地将相关付款分配给 Baylor Genetics,并指示该款项直接支付给 Baylor Genetics。我理解我的自付费用可能与 Baylor Genetics 在福利核查调查中向我指示的估计金额不同。我同意对我的健康保险计划发布的福利说明中所示的所有金额承担财务责任。如果我的保险公司直接向我支付 Baylor Genetics 代表我提供的未付费服务的费用,我同意在保险支票上签字并在收到支票后三十 (30) 天内将该支票转交给 Baylor Genetics,作为 Baylor Genetics 服务索赔的付款。如果我没有健康保险,我同意支付我的医疗保健提供者订购的、Baylor Genetics 向我开具的基因检测的全部费用。
研究肿瘤学杂志革命性癌症护理
癌症研究进入了一个令人兴奋的新时代,裁员的发现和技术改变了我们理解,检测和治疗疾病的方式。虽然癌症仍然是医学上最巨大的挑战之一,但基因组学,免疫疗法,早期检测和人工智能的进步为更具个人化,有效和侵入性较小的疗法铺平了道路。在这里,我们探讨了癌症研究中最有希望的发展,这些发展可能会重塑肿瘤学的未来。癌症研究中最深刻的转变之一就是朝着精确医学的发展。癌症不是一种疾病,而是由多种基因突变引起的疾病的集合。传统的“一定程度的”方法,即广泛使用了化学疗法和放射治疗(例如化学疗法和放射线),它被旨在针对促进癌症生长的特定遗传学的疗法所取代。多亏了基因组测序的进步,研究人员现在可以识别患者癌细胞中的突变,并开发出专门针对这些遗传变化的治疗方法。这导致了靶向疗法的发展,这些疗法旨在阻止负责癌细胞增殖的蛋白质或信号通路。
利用免疫组织化学和免疫荧光法评估 c-KIT 在涎腺腺样囊性癌中的作用
利比亚的黎波里。摘要背景:腺样囊性癌是涎腺最常见的恶性肿瘤之一,具有侵袭性、复发、远处器官转移和相对放射抗性的特点,使得局部控制难以实现。目的:这项研究的目的是阐明 c-KIT 在基因和蛋白质水平上在涎腺腺样囊性癌发病机制中的作用。材料和方法:通过实时免疫组织化学 (IHC) 和聚合酶链反应 (PCR) 测定总共 52 例涎腺腺样囊性癌标本中的 c-KIT 蛋白表达和基因水平。结果:在所有研究病例中均观察到 c-KIT 抗体的免疫反应性,而通过 DNA 测序检测 c-KIT 基因突变的 13 例病例尽管免疫组织化学呈阳性,但未检测到基因突变。结论:尽管唾液腺腺样囊性癌中 c-KIT 免疫阳性率较高,但基因突变的缺失导致靶向治疗无效。2024 年 11 月 27 日收到;2024 年 12 月 4 日修订;2024 年 12 月 6 日接受 © 作者 2024。在 www.questjournas.org 上以开放获取方式发布
B7-H4:腺样囊性癌的潜在治疗靶点
腺样囊性癌 (ACC) 是一种罕见的分泌腺恶性肿瘤,具有双重生物学和临床行为。虽然大多数患者最初表现为局部晚期疾病,但 50-60% 的病例会出现远处转移,而这种疾病的治疗选择有限 [1]。我们的团队之前曾根据蛋白质组学和临床数据报告过两种主要的 ACC 分子亚型 [2]。ACC-I 是最具侵袭性的 ACC 类型,其特征是实体组织学、NOTCH1 突变富集、早期发生转移(包括转移到内脏器官)和预后不良(中位总生存期 (mOS) = 3.4 年)。而 ACC-II 更为普遍(占病例的 66%),其特征是非实体组织学(筛状和/或管状)、p63 和受体酪氨酸激酶上调、主要发生肺转移和总体缓慢病程(mOS = 23 年)。这些差异强调了 ACC 的内在异质性以及个性化治疗的必要性,以改善该疾病患者的临床结果。