XiaoMi-AI文件搜索系统
World File Search SystemIMVAMUNE(猴痘/天花)疫苗适用于患有...的人
作者:Elissa M Abrams MD MPH、Kyla J Hildebrand MD MSsCH、Andrew O'Keefe MD MPH 和 Jennifer LP Protudjer PhD IMVAMUNE 是第三代减毒活非复制型正痘病毒疫苗,最初为预防天花而开发,最近获批用于 18 岁及以上成人猴痘感染的暴露前和暴露后预防。1 虽然尚未获准在 18 岁以下儿童和青少年中使用,但国家免疫咨询委员会酌情建议此类人群使用 IMVAMUNE,因为这可能会增加严重感染的风险。1 IMVAMUNE 含有微量潜在药物过敏原(氨丁三醇、庆大霉素、环丙沙星)和食物过敏原(鸡蛋)。在本文中,我们旨在解决对这些过敏原或疫苗本身可能或已确认过敏的人群中使用 IMVAMUNE 的问题。
学院/行政/服务部门: - 萨里大学
该职位面向热情、创新的博士后研究员,研究方向为疫苗学和病毒学,特别是痘病毒和人类先天免疫。这是一个多学科项目,涉及疫苗开发和测试、病毒学、先天免疫和分子生物学,因此欢迎拥有这些领域博士学位的候选人,只要他们能够证明自己在病毒学、先天免疫和/或疫苗学方面有成就和热情。该项目将在萨里大学一个成熟的研究小组进行,由卡洛斯·马鲁克·德莫特斯博士(分子病毒学讲师)指导,他是一位在宾夕法尼亚大学(美国)、伦敦帝国理工学院(英国)和剑桥大学(英国)接受过培训的研究员,在大型 DNA 病毒和免疫逃避方面拥有 10 年的经验。候选人应积极主动,具有人际沟通技巧,并具有出色的组织和时间管理技能。
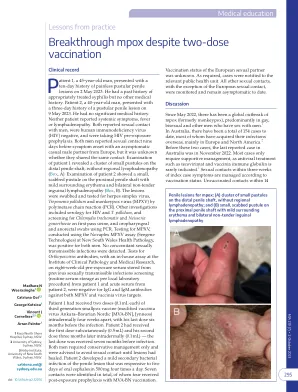
尽管接种了两剂疫苗,但仍出现突破性感染
患者 1 是一名 45 岁的男性,于 2023 年 5 月 2 日出现无痛性脓疱性阴茎病变 10 天。他有适当治疗的梅毒病史,但没有其他病史。患者 2 是一名 40 岁的男性,于 2023 年 5 月 9 日出现脓疱性阴茎病变 3 天。他没有重大病史。两名患者均未报告全身症状、发烧或淋巴结肿大。两人均报告与男性发生性接触,人类免疫缺陷病毒 (HIV) 呈阴性,并正在服用 HIV 暴露前预防措施。两名男性均报告在症状出现前九天与来自欧洲的无症状临时男性伴侣发生过性接触,但未知他们是否有同一次接触。对患者 1 的检查发现远端阴茎轴上有一簇小脓疱,没有局部淋巴结肿大(方框,A)。对患者 2 的检查显示,近端阴茎轴上有一个小的结痂脓疱,周围有轻微的红斑,双侧无痛性腹股沟淋巴结肿大(方框,B)。对病变进行拭子检查,并用聚合酶链反应(PCR)检测单纯疱疹病毒、梅毒螺旋体和猴痘病毒 (MPXV)。其他检查包括艾滋病毒和梅毒螺旋体血清学检查,以及使用 PCR 对初次尿液和口咽和肛门直肠拭子进行沙眼衣原体和淋病奈瑟菌筛查。在新南威尔士州卫生病理学部门使用 Novaplex MPXV 检测(Seegene Technologies)对两名男性进行了 MPXV 检测,结果均为阳性。未检测到同时存在的性传播感染。在临床病理学和医学研究所的内部检测中,对患者 1 的先前性传播感染筛查中储存的八周前暴露前血清(根据当地实验室程序进行常规血清储存)和患者 2 的急性血清进行了正痘病毒抗体测试,结果显示针对 MPXV 和痘苗病毒靶标的 IgG 和 IgM 抗体均为阴性。
AAV 介导的基因治疗:推进心血管疾病治疗
基因治疗彻底改变了医学领域,为常见病和罕见病患者带来了新的希望。近 30 年来,腺相关病毒 (AAV) 在多个临床试验中显示出显著的治疗益处,主要是由于其独特的复制缺陷和对人类无致病性。在心血管疾病 (CVD) 领域,与非病毒载体、慢病毒、痘病毒和腺病毒载体相比,AAV 具有安全性高、免疫原性低、外源基因可持续稳定表达等优势,使 AAV 成为治疗多种遗传病和遗传性疾病最有希望的候选药物之一。在本综述中,我们评估了目前关于基于 AAV 的 CVD 基因治疗相关的免疫反应、转运途径和作用机制的信息,并进一步探索潜在的优化策略,以提高 AAV 转导的效率,从而提高 CVD 治疗的安全性和效率。总之,AAV介导的基因治疗在心血管系统领域具有巨大的发展潜力。
Mpox 疫苗接种,民主共和国......
猴痘是由猴痘病毒 (MPXV) 引起的,是一种人畜共患传染病,流行于刚果民主共和国 (DRC) ( 1 – 3 )。2022 年,MPXV 进化枝 IIb 在全球迅速传播,导致确诊感染人数超过 91,000 人,促使世界卫生组织宣布该病为国际关注的突发公共卫生事件 ( 4 )。在刚果民主共和国,2021 年至 2023 年的发病病例增加了四倍;2023 年 1 月至 2024 年 7 月期间,报告了 28,000 例疑似病例,邻国布隆迪、卢旺达、肯尼亚和乌干达也记录了新的病例 ( 5 )。2024 年 8 月,瑞典报告了一例与旅行相关的进化枝 Ib 病例 ( 6 )。为应对 2024 年不断增加的 mpox 负担,非洲疾病控制和预防中心宣布了非洲大陆安全公共卫生紧急事件 ( 7 ),世界卫生组织宣布了国际关注的公共卫生紧急事件 ( 4 )。尽管已向许多高中级医院部署了改良的安卡拉-巴伐利亚北欧痘苗 (https://www. bavarian-nordic.com),但
JYNNEOS™ Mpox 疫苗现可通过 VFC 获得
目前,尚无关于同时接种 JYNNEOS™ 疫苗和其他疫苗的数据。由于 JYNNEOS™ 不可复制,因此通常可以不考虑其他疫苗的接种时间而进行接种。这包括尽可能在不同的解剖部位同时接种 JYNNEOS™ 和其他疫苗(包括流感疫苗),以简化潜在局部反应的识别。考虑同时接种 MenACWY 或其他推荐疫苗和 JYNNEOS™。无论先接种哪种疫苗,接种任何 COVID-19 疫苗(即 Moderna、Novavax 或 Pfizer-BioNTech)和 JYNNEOS™ 疫苗之间没有最低间隔要求。建议接种两种疫苗的人(尤其是青少年或年轻成年男性)可能考虑在接种疫苗之间等待 4 周。此等待期是由于接种 ACAM2000 正痘病毒疫苗和 COVID-19 疫苗后观察到的心肌炎和心包炎风险,以及接种 JYNNEOS™ 疫苗后假设的心肌炎和心包炎风险。但是,如果患者因 COVID-19 疾病而面临 mpox 或严重疾病的风险增加,则不应延迟接种 JYNNEOS™ 和 COVID-19 疫苗。多次注射的最佳做法包括:
猴痘疫苗
所有剂量都应在给药后 24 小时内记录在 NDIIS 中。NDHHS 提供的剂量应输入到 NDIIS 中,使用公众作为资金来源和其他符合 VFC 状态的州。• 疫苗名称:天花/猴痘• 品牌:Jynneos™• MVX:BN• CVX:206• 销售单位 NDC(11 位数字):50632-0001-03• 销售单位 NDC(10 位数字):50632-001-03• 使用单位 NDC(11 位数字):50632-0001-01• 使用单位 NDC(10 位数字):50632-001-01 CPT 代码已创建当前程序术语 (CPT) 代码,以简化目前在美国市场上可用的正痘病毒和猴痘检测和免疫接种的报告。查看此 AMA 网页,其中概述了代码并为提供商提供了进一步的指导。• 90611:天花和猴痘疫苗,减毒痘苗病毒,活的,非复制型,不含防腐剂,0.5 毫升剂量,悬浮液,用于皮下使用特殊注意事项
优化用于检测绵羊的聚合酶链反应
SPV的抽象准确和快速诊断对于控制利比亚疾病的快速传播至关重要。本研究旨在优化和开发利比亚阿尔扎维耶市绵羊农场绵羊病毒鉴定的PCR分析。总共收集了120个口头拭子样品,如下:临床怀疑的绵羊痘(n = 67),临床怀疑具有传染性的外生体(n = 18)和健康的绵羊(n = 35)。对收集的样品进行DNA提取,然后进行针对p32基因的聚合酶链反应,该反应用特定的引物。所有67个临床怀疑的绵羊痘样品的SPV呈阳性,并产生预期的扩增子大小为390 bp。所有临床上怀疑的传染性胚膜(CE)样品和健康样品均为阴性。当前基于p32基因的PCR分析的结果表现出良好的敏感性和特异性,可用于分子诊断绵羊痘病毒疾病。关键字。绵羊痘病毒,p32 Gene,PCR,Alzawiyah City,Libya。引言绵羊病是绵羊中最严重,最感染的病毒疾病[1]。在临床上,Sheepox病毒(SPV)可以通过发烧,厌食症,抑郁症,肺部病变发展,无羊毛区域的痘病变的出现以及表面淋巴结肿胀来识别。[2]。SPV是严重的绵羊皮肤病。SPV属于Poxviridae家族的Capripoxvirus(CAPV)属。该属的成员,还包括引起皮肤肿块和山羊痘的病毒,感染绵羊,山羊和牛,并引起经济上重要的疾病(LSDV)[3,4]。绵羊痘病毒是动物的最重要的蛇毒,在OIE的A组疾病中列出[5]。由于对绵羊的羊毛和皮革损害,牛奶产量降低,堕胎率降低,体重增加和高死亡率降低,可能会造成严重的生产损失[6-8]。即使在许多国家中消除了这种疾病,但仍有从北非,中东,西亚,印度和中国在内的世界各地据报道[8,9]。在利比亚,该疾病通常具有enzootic外观。它威胁着农业部门的发展,造成了与羔羊死亡率有关的经济损失,成人的繁殖和生产下降[10]。SPV的诊断通常基于高度特征的临床体征,病毒的分离,中和 - 中和血清学测定[11,12]和聚合酶链反应(PCR)分析[13,11]。用于识别SPV的常规病毒学和血清学测定是耗时,费力的,大多数的特异性低[14]。但是,包括PCR分析在内的分子方法是潜在的工具,可以用作传统实验室技术检测SPV的替代或互补测试。被证明是可靠,敏感,快速和特定的方法,这些方法通常用于世界上许多病毒的检测和表征,包括卡皮托病毒[15,16,12]。[17]。这项研究的目的是创建一种快速,敏感的方法,用于在短时间内检测现场样本中的SPV,从而实用和高效。此外,对于识别SPV的识别,需要进行快速,特异性和敏感测试,因为在现场样品中及时检测SPV对于成功的SPV控制至关重要,并且降低了可能由流行病引起的潜在严重经济损害。方法样本该研究是在利比亚黎波里的利比亚生物技术研究中心(BTRC)的基因工程系进行的。当前的研究总共收集了120件口腔拭子,从可疑的绵羊痘病例中获得了67件,从可疑的绵羊传染性ecthyma(CE)中获得了18例,以及各种羊群中的健康绵羊(阴性对照)的35例。在2013年5月至2014年4月之间,标本是从利比亚阿尔扎维亚市的绵羊群中收集的。使用由英国的公司Isohelix提供的颊拭子管进行了口服拭子样品。随后将这些样品运输到基因工程
新西兰数据表 1. 产品名称
2. 定性和定量组成 JYNNEOS 是一种活疫苗,由改良的安卡拉-巴伐利亚北欧痘苗 (MVA-BN) 菌株产生,这是一种减毒的、非复制性正痘病毒。MVA-BN 在悬浮于不含直接动物来源物质的无血清培养基中的原代鸡胚成纤维细胞 (CEF) 中生长,从 CEF 细胞中收获,通过包括苯并酶消化在内的几个切向流过滤 (TFF) 步骤纯化和浓缩。每 0.5 mL 剂量配制成含有 0.5 x 10 8 至 3.95 x 10 8 个感染单位的 MVA-BN 活病毒,溶于 10 mM Tris(氨基丁三醇)、140 mM 氯化钠,pH 值为 7.7。每 0.5 mL 剂量可能含有残留的宿主细胞 DNA(≤ 20 mcg)、鸡蛋白(≤ 500 mcg)、Benzonase(≤ 0.0025 mcg)、庆大霉素(≤ 0.400 mcg)和环丙沙星(≤ 0.005 mcg)(见 4.3 节)。有关辅料的完整列表,请参阅 6.1 节。
Jynneos USA 审查备忘录 08092022
审查备忘录日期:2022 年 8 月 9 日 收件人:文件 发件人:Peter Marks,医学博士,哲学博士(CBER/OD) 申请人名称:国家过敏和传染病研究所 (NIAID) EUA 申请编号:28801 产品:JYNNEOS(天花和猴痘疫苗,活,非复制型) 主题:评估通过皮内 (ID) 给药途径使用两剂(每剂 0.1 毫升,含 2 x 10 7 TCID 50 MVA-BN)JYNNEOS 用于预防 18 岁及以上被确定为感染猴痘风险较高的个人的猴痘病,以及通过皮下 (SC) 给药途径使用两剂(每剂 0.5 毫升,含 1 x 10 8 TCID 50 MVA-BN)JYNNEOS 用于预防 18 岁以下个人的猴痘病被确定为患有猴痘感染高风险 本备忘录提供了 JYNNEOS(天花和猴痘活疫苗,非复制型)紧急使用授权 (EUA) 的摘要、审查和建议,以授权进行以下管理:(i) 两剂(每剂 0.1 mL 含 2 x 10 7 TCID 50 的 MVA-BN,以下简称 0.1 mL)JYNNEOS,间隔 4 周通过皮内 (ID) 途径给药,给药对象为被确定为患有猴痘感染高风险的 18 岁及以上个人;以及 (ii) 两剂(每剂 0.5 mL 含 1 x 10 8 TCID 50 的 MVA-BN,以下简称 0.5 mL)JYNNEOS,间隔 4 周通过皮下 (SC) 途径给药,给药对象为被确定为患有猴痘感染高风险的 18 岁以下个人。执行摘要 猴痘是一种与天花有关的正痘病毒。第一例人类猴痘病例记录于 1970 年,过去几十年来,猴痘与零星爆发有关,通常发生在访问过非洲大陆的国际旅行者身上。在目前的疫情中,迄今为止主要影响男男性行为者及其亲密接触者,该疾病通常表现为生殖器区域的疼痛性病变,可能需要两到三周才能完全愈合。 JYNNEOS 是美国 FDA 许可的疫苗,获准用于预防 18 岁及以上被确定为感染天花或猴痘风险较高的个人的猴痘和天花病。它是一种活病毒疫苗,由改良的安卡拉-巴伐利亚北欧痘苗 (MVA-BN) 菌株生产,这是一种减毒的、非复制性正痘病毒,