XiaoMi-AI文件搜索系统
World File Search System靶向NRF2及其下游过程
转录因子 NRF2 协调大量细胞保护和代谢基因的表达,以响应各种压力输入,恢复细胞稳态。健康组织中 NRF2 的瞬时激活长期以来被认为是一种细胞防御机制,对于防止致癌物引发癌症至关重要。然而,癌细胞经常劫持 NRF2 的保护能力来维持氧化还原平衡并满足其增殖的代谢需求。此外,癌细胞中 NRF2 的异常激活会导致对常用化疗药物和放射疗法的耐药性。在过去十年中,许多研究小组试图阻断肿瘤中的 NRF2 活性,以抵消癌细胞的生存和增殖优势并逆转对治疗的耐药性。在这篇综述中,我们重点介绍了 NRF2 在癌症进展中的作用,并讨论了过去和现在禁用肿瘤中 NRF2 信号传导的方法。
脑科学 - 神经退行性疾病中的星形胶质细胞
“神经退行性疾病”通常是指诸如阿尔茨海默氏病,亨廷顿氏病,各种共济失调和大量罕见的遗传疾病等疾病,这些疾病会导致神经元的逐渐丧失,认知和运动功能的丧失以及某些情况下,死亡。然而,神经退行性的迹象在癫痫和抑郁等疾病中也很明显。尽管“神经变性”一词显然意味着神经元的生存能力丧失,但现在普遍承认星形胶质细胞与这种过程密切相关。星形胶质细胞通过各种方式帮助神经元的弹性。一些研究表明,它们实际上可能是某些条件下病理机制的一部分。我们试图在所有病理状态中的星形胶质细胞与神经元之间的相互作用进行研究。星形胶质细胞保护神经元免受损害的机制,与小胶质细胞在处理退化神经元方面的合作以及疾病中星形胶质细胞的可塑性是本卷中潜在的主题。
我们niriotic流体衍生的细胞外囊泡显着改善了人类
关键字:细胞外囊泡,神经再生,细胞间交流,PC12细胞引入神经系统疾病具有挑战性治疗,因为中枢神经系统(CNS)的再生潜力差。在过去的几十年中,细胞疗法已成为再生医学的前线。但是,临床试验的糟糕证据要求科学家的极端重点来制定适当的方案和方法[1]。例如,神经营养因子的表达可以通过基因治疗作为一种补充方法增强治疗作用,但不幸的是,可能会导致与遗传变化相关的可能风险。干细胞旁分泌作用的证据是组织再生的突破[2]。在2005年,Gnecchi等人。表明,间充质干细胞(MSC)培养基通过缺氧下心脏细胞的AKT1过表达表明细胞保护作用,以及心肌梗塞大小的减小,并增强了体外和体外和体内的心室功能, *相应的作者 *相应的作者。电子邮件:saeidifar@merc.ac.ir
电池单元与...
(v),印度海得拉巴Medchal District。摘要:电动汽车(EVS)需要一个车载电池充电器单元和电池管理系统(BMS)单元,以平衡每个电池电池的电压水平。因此,提出的电路在一个方面使用了两个函数,因此消除了具有两个自传单元降低复杂性和降低组件计数的需求。电池均衡,旨在使内部电池的充电状态保持相同水平,对于最大化整个电池组的容量并使单元远离过度充电和过度放电损坏至关重要。在本文中,基于对双向转换器的分析,我们提出了一个模糊控制器来适应均衡电流。选择模糊控制器的输入作为充电状态,电荷的平均状态和总内部电阻的差异。通过多数指数(例如均衡速度,效率和细胞保护)评估所提出的均衡器的整体性能。拟议的电路作为反式转换器运行,并在电池充电期间实现功率因数校正。
核糖细胞器创伤处是由于功能丧失LMNA突变而引起的心肌病发病机理的
摘要在过去25年中,在LMNA基因中具有突变的各种实验模型中已经报道了核包膜(NE)扰动。尽管LMNA突变的NE扰动是横纹肌肉损伤的基本特征的假说,已获得广泛的接受,但由NE损伤引起的分子序列造成的分子序列以及它们如何基于疾病发病机理,例如心肌病(LMNA心脏疾病)仍然很差。最近,我们通过在成人心脏中采用心肌细胞 - 特异性LMNA缺失来阐明这种结果。,我们在心脏功能恶化之前观察到广泛的NE扰动,并在核周空间中旁边损害。高尔基体受到了特别的影响,导致细胞保护应激反应可能会因高尔基体的进行性恶化而破坏。在这篇综述中,我们讨论了LMNA心肌病的病因,并将核周的“井肌创伤”作为NE损伤和疾病发病机理之间的联系。
关注健康和疾病的NRF2信号通路
氧化应激,已知会增加多种代谢和慢性异常或癌症发展的风险,被定义为活性氧(ROS)的产生与抗氧化剂抵消氧化剂有害作用的能力之间的不平衡。为了调节氧化/还原(氧化还原)平衡,存在许多抗氧化剂和非酶抗氧化剂。自由基激活转录因子以促进抗氧化剂的产生和线粒体生物发生。这些转移因子之一,核因子2相关因子2(NRF2)是抗氧化剂和抗炎反应的主要调节剂。的确,NRF2通过启动涉及抗氧化剂和细胞保护反应的数百个基因的转录来促进氧化还原平衡。更好地了解氧化应激的分子靶标及其与NRF2信号通路的相互作用将增强其预防性或治疗性在健康和疾病中的相关性。对于本期特刊,邀请研究人员提交原始文章或审查有关动物模型或人类氧化应激的不同方面的文章。主题包括着重于慢性疾病或预防NRF2信号通路的生物学和生理效应。
评论文章理解白介素11作为疾病基因和治疗靶标的
白介素11(IL11)是IL6细胞因子家族的难以捉摸的成员。最初被认为是造血和细胞保护因素,但最新的数据表明,IL11对于造血和有毒而言是多余的。在这篇综述中,导致IL11生物学的原始误解的原因(现在是可以理解的),特别关注了在小鼠和人类中使用重组人IL11的使用。在组织损伤之后,作为进化古代稳态反应的一部分,IL11从受损的哺乳动物细胞中通过JAK/STAT3,ERK/P90RSK,LKB1/MTOR和GSK3β/SNAI1在自分泌和旁分泌中分泌。这激活了上皮,基质和内皮细胞的间充质转变程序,以引起炎症,纤维化和停滞的内源性组织修复,从而导致器官衰竭。描述了IL11信号传导在细胞和器官特异性病理学中的作用,讨论了有关IL11生物学的大型未知数,并审查了将IL11信号作为一种方法的靶向靶向。
热肿瘤:MEX-3家族蛋白的法规
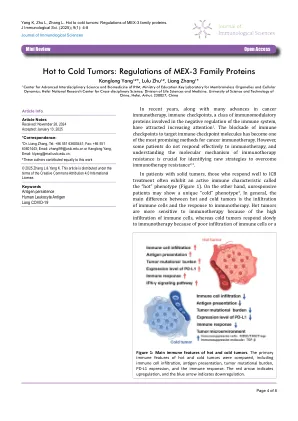
肿瘤细胞免疫逃生的机制许多机制,一些研究将其定义为“ 3C”模型6,即伪装,它使肿瘤细胞无法通过免疫细胞识别。胁迫,直接或间接干扰免疫细胞;和细胞保护作用,这是对肿瘤细胞免受免疫细胞毒性的保护。这些机制主要包括肿瘤抗原表达或表现中的缺陷:肿瘤细胞可能会失去或改变其表面抗原的表达,从而使T细胞无法识别和攻击它们;免疫抑制细胞的募集:各种免疫抑制细胞(例如调节性T细胞,髓样抑制细胞等)可以募集到肿瘤微环境中,这可以直接抑制效应T细胞的功能。和细胞因子分泌:肿瘤细胞可以分泌一些免疫抑制性细胞因子(例如IL-10,TGF-β等)抑制免疫反应并促进肿瘤的生长;肿瘤微环境的变化:肿瘤细胞可以改变微环境,使其更有利于肿瘤生长并抑制抗肿瘤免疫反应。这些机制经常重叠,从而使肿瘤有效地逃避了免疫系统监测。
黑色素瘤中的 HSP90 抑制剂
摘要 HSP90(热休克蛋白 90)是一种 ATP 依赖性分子伴侣,参与数百种蛋白质的正确折叠和成熟。HSP90 在癌症(包括黑色素瘤)中大量表达。HSP90 客户蛋白是控制黑色素瘤发展、进展和治疗反应的几种信号通路的关键癌蛋白。许多具有不同化学结构和 HSP90 内结合位点的天然和合成化合物已被鉴定为选择性 HSP90 抑制剂。大多数 HSP90 靶向药物会影响 HSP90 的 N 端 ATPase 活性。与 N 端抑制剂相比,与 HSP90 中部和 C 端结构域相互作用的药物不会诱导 HSP70 依赖性细胞保护反应。在临床前研究和临床试验中,几种 HSP90 抑制剂针对黑色素瘤进行了测试,证明这些药物可以被视为单一或补充治疗策略。本综述总结了目前关于 HSP90 蛋白在癌症中的作用的知识,重点是黑色素瘤,并概述了被视为黑色素瘤治疗潜在疗法的结构不同的 HSP90 抑制剂。
抑制ULK1/2和KRASG12C控制肿瘤生长... 供体衍生的多重白血病抗原特异性T细胞疗法,以防止所有患者移植后复发 与年龄相关的丁酸酯产生细菌的时间下降在3×TG-AD小鼠的神经病理学和记忆缺陷的发作和进展中起关键的致病作用 naltrexone-bupropion组合不影响可卡因自我 胰腺内导管内乳头肿瘤的空间转录组将NKX6-2鉴定为胃分化和顽固生物潜能的驱动力 昼夜节律作为发育期间和整个衰老期间大脑健康的调节剂 小鼠心脏发育的三维微观成像从早期植入后到晚期阶段 使用现场虚拟培训课程改善学校卫生工作者的糖尿病管理
KRAS的摘要突变激活通常发生在肺癌发生中,并且随着美国食品和药物管理局最近批准KRAS G12C的共价抑制剂,例如Sotorasib或Adagrasib,KRAS癌蛋白是非小细胞肺癌(NSCLC)的重要药理靶标。但是,并非所有KRAS G12C驱动的NSCLC都对这些抑制剂做出反应,并且那些反应反应的患者的耐药性出现可能是迅速而多效的。因此,基于共价抑制KRAS G12C的支柱,正在努力开发有效的组合疗法。在这里,我们报告说,KRAS G12C信号传导的抑制会增加KRAS G12C表达肺癌细胞的自噬。此外,DCC -3116(一种选择性ULK1/2抑制剂)的组合以及sotorasib显示了对人Kras G12C驱动的肺癌细胞增殖的合作/协同抑制体内体外和肿瘤对照中的抑制作用。此外,在KRAS G12C驱动的NSCLC的基因工程小鼠模型中,抑制KRAS G12C或ULK1/2的抑制会减轻肿瘤负担并增加小鼠的存活率。因此,这些数据表明ULK1/2介导的自噬是对肺癌中KRAS G12C抑制的药理作用的细胞保护胁迫反应。