XiaoMi-AI文件搜索系统
World File Search System慢性β3肾上腺素能治疗可改善神经血管耦合反应,减轻血脑屏障泄漏和神经炎症,并增强老年小鼠的认知
1神经外科部,俄克拉荷马州俄克拉荷马州俄克拉荷马州俄克拉荷马州俄克拉荷马州俄克拉荷马州俄克拉荷马州俄克拉何马州俄克斯学和健康大脑中心俄克拉荷马州健康科学中心,俄克拉荷马州健康科学中心,俄克拉荷马州健康科学中心,俄克拉荷马州俄克拉荷马州典范中心,美国俄克拉荷马州73104,俄克拉荷马州俄克拉荷马州俄克拉荷马州哥伦比亚省校园和美国俄克拉荷马州典范中心,美国73104,美国俄克拉荷马州校友73104美国俄克拉荷马城俄克拉荷马州健康科学中心,美国4号,美国4 43104,俄克拉荷马州立大学兽医学院,兽医学院,俄克拉荷马州斯蒂尔沃特市,俄克拉荷马州73104,美国5美国,美国俄克拉荷马州卫生科学院,美国俄克拉荷马州卫生部,美国俄克拉荷马州卫生部,俄克拉荷马州卫生部,美国俄克拉荷马州,卫生部美国俄克拉荷马城中心,美国俄克拉荷马州73104,美国7 Geroscience的国际培训计划,基础和转化医学博士学位/公共卫生系/Semmelweis University,Budapest,Budapest,Hungary
巴瑞替尼和托法替尼的脱靶概况,重点关注……
缩写:Cmax:脑内巴瑞替尼的最大浓度,小鼠实验:在小鼠中实验观察到的,QIVIVE BBB:血脑屏障渗透的定量体外-体内外推,QSAR:定量结构-活性关系。
国家免疫,过去和未来之间
Noemie Cresto,Isabel Forner-Piquer,Asma Baig,Mousumi Chatterjee,Julie Perroy等。脑边界的农药:对血脑屏障,神经炎症和神经系统风险的影响。化学圈,2023,324,pp.138251。10.1016/j.Chemosphere.2023.138251。hal-04428920
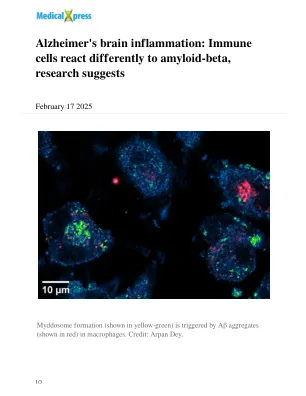
阿尔茨海默氏症的脑部炎症:免疫细胞对淀粉样蛋白β的反应不同,研究表明
“细菌由于血脑屏障而无法进入我们的大脑,”英国剑桥大学的大卫·克莱尔曼(David Klenerman)教授的博士后学院说。“但是小蛋白可能在我们的大脑中像细菌一样起作用,并引起神经炎症,这可能会导致痴呆症。”他补充说。
文献计量与可视化分析
结果:共发现 4230 篇有关病毒和神经炎症的文章和评论,随着时间的推移呈现持续上升趋势。美国是贡献出版物最多的国家。来自 4474 个机构的约 22274 名作者参与了这项研究。约翰霍普金斯大学的出版物和引用量最高。该领域发表文章最多的前三位作者分别是 Power, C.、Lane, TE 和 Buch, S。《神经炎症杂志》是研究人员最权威的选择。该领域的主要研究重点包括多发性硬化症、帕金森病、血脑屏障、COVID-19、阿尔茨海默病、基因治疗。近年来,压力成为热门关键词,特别是抑郁症、人类免疫缺陷病毒相关神经认知障碍、血脑屏障、肠道微生物群相关方向,预示着研究重点可能会发生转变。
标题:征求FDA的紧急请愿:加快亨特综合症患者DNL310的访问日期:7/29/2024
denali Therapeutics正在进行一项持续的DNL310(NCT04251026)的I/II期试验,这是一种旨在治疗猎人综合征的外围和中枢神经系统表现的酶替代疗法。该试验的初始数据证明了DNL310的安全性。DNL310(NCT05371613)的II/III期试验始于2022年,目前正在进行中。在这项试验中,6岁以下的患者被随机分配,以盲目的方式接受DNL310或IDURSULFase(Elaprase)2年。ELAPRASE是FDA批准的酶替代疗法,用于治疗猎人综合征已有15年以上。小脑膜不会穿过血脑屏障,因此不处理猎人综合征的中枢神经系统表现。dnl310是I2融合到Denali专有酶的运输载体,该酶经过精心设计,可通过受体介导的大脑跨脑胞菌病穿越血脑屏障。
了解使用脂质体向大脑输送药物...
摘要。血脑屏障 (BBB) 可能会限制脑部药物输送,而基于脂质体的药物输送策略则可增强脑部药物输送。由于人类大脑的通路有限,许多研究都是在实验动物身上进行的。尽管这些研究提供了有趣的数据,但仍有改进的空间,以便提供机制见解,了解特定 BBB 运输和脑内分布过程的速率和程度,这些过程共同控制着 CNS 靶向输送的游离药物。本综述简要总结了 BBB 运输和当前基于脂质体的克服 BBB 运输限制的策略,重点是如何确定共同决定游离药物脑浓度时间过程的各个机制,包括药物本身和脂质体给药后。重点介绍了使用微透析的动物研究,这些研究提供了血浆和脑中未结合药物的时间过程信息,因为这些研究提供了了解 BBB 药物运输所需的机制信息,以及该药物的脂质体制剂对 BBB 运输的影响。总体而言,这些研究表明,以脂质体制剂形式给药的药物在大脑中的分布取决于药物性质和脂质体制剂特征。一般而言,有证据表明,脂质体绕过了血脑屏障中的主动转运体(无论是流入转运体还是流出转运体)。结论是,脂质体制剂可能会给血脑屏障的转运带来有趣的变化。需要进行更多的机制研究来了解脂质体药物向大脑输送的相关机制,从而为使用动物数据预测人类的药物输送提供更好的基础。
光遗传学激活星形胶质细胞可降低血液
摘要:光遗传学已被用于调节星形胶质细胞活性并调节脑损伤后的神经元功能。活化的星形胶质细胞调节血脑屏障功能,从而参与脑修复。然而,光遗传学激活的星形胶质细胞对缺血性中风屏障功能变化的影响和分子机制仍不清楚。在本研究中,成年雄性 GFAP-ChR2-EYFP 转基因 Sprague-Dawley 大鼠在光血栓性中风后 24、36、48 和 60 小时接受光遗传学刺激以激活同侧皮质星形胶质细胞。使用免疫染色、蛋白质印迹、RT-qPCR 和 shRNA 干扰探索活化的星形胶质细胞对屏障完整性的影响及其潜在机制。进行神经行为测试以评估治疗效果。结果表明,光遗传学激活星形胶质细胞后,IgG 漏出、紧密连接蛋白间隙形成和基质金属肽酶 2 表达均减少( p <0.05)。此外,与对照组相比,光刺激星形胶质细胞可保护中风大鼠的神经元免于凋亡并改善神经行为结果( p <0.05)。值得注意的是,大鼠缺血性中风后光遗传学激活的星形胶质细胞中白细胞介素 10 的表达显著增加。抑制星形胶质细胞中的白细胞介素 10 会削弱光遗传学激活的星形胶质细胞的保护作用( p <0.05)。我们首次发现来自光遗传学激活的星形胶质细胞的白细胞介素 10 通过降低基质金属肽酶 2 的活性和减弱神经元凋亡来保护血脑屏障的完整性,这为缺血性中风急性期提供了一种新的治疗方法和靶点。关键词:星形胶质细胞、血脑屏障、白细胞介素 10、光遗传学、中风 引言 星形胶质细胞可以被动支持神经元的发育和存活,或主动调节突触传递和血脑屏障 (BBB) 的完整性 [1]。星形胶质细胞活化是缺血性中风的一个重要特征。活化的星形胶质细胞通过释放炎症因子(如 IL-6、TNF-α、IL-1α、IL-1β、干扰素 γ (IFNγ) 和自由基)发挥有害作用 [2]。它还可以通过释放
肺癌患者 58 个月的生活质量很高......
由于血脑屏障的特性,药物无法顺利转运至中枢神经系统,脑部曾被认为是转移性NSCLC的避难所[3]。尽管由于血脑屏障的影响[3],化疗并未用于治疗脑转移,但靶向药物和免疫检查点抑制剂已显示出明显获益[4]。对于无吸烟史的晚期NSCLC患者,若分子检测为表皮生长因子受体(EGFR)阳性,则建议首先进行靶向治疗[5]。随着靶向启动子基因的发现和相关药物研究,多发转移的晚期NSCLC患者的治疗也取得了可喜的进展[6-8]。如何优化利用现有的靶向药物,是NSCLC个体化治疗中满足中枢神经系统临床需求的重要途径[9]。我们在此介绍一位脑、骨、肺多发转移的NSCLC患者,经过适当的分子靶向治疗组合,存活时间超过5年,且生活质量非常好。这是迄今为止脑、骨、肺多发转移的NSCLC患者中存活时间最长的。