XiaoMi-AI文件搜索系统
World File Search System研究强调了治疗耐药性癌症的新靶点和潜在疗法
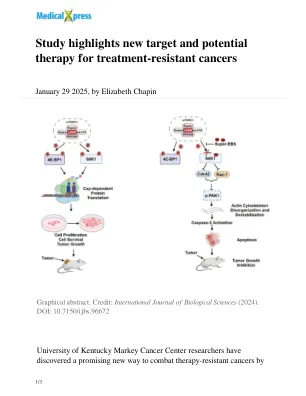
癌细胞通常会通过改变其特性(一种称为细胞可塑性的过程)来对治疗产生耐药性。研究发现,随着癌症产生这种耐药性,它们会变得更加依赖磷酸化的 S6K1,从而使它们更容易受到新治疗方法的攻击。这项研究为未来研究 Super-EBS 和相关化合物以开发针对治疗耐药性癌症的靶向疗法打开了大门。
经人类遗传学验证的功能丧失突变靶点
KHK 是果糖代谢的限速酶之一,对 NAFLD/NASH、T2D 和其他果糖介导的代谢疾病具有治疗意义,目前有两种药物处于 II 期临床阶段(ALN-KHK 和 PF-06835919)。CIDEB 在维持全身脂质稳态和能量代谢方面起着重要作用,阻断 CIDEB 表达可能有助于预防或治疗 NASH 和相关疾病,但目前尚无用于此目的的药物处于临床试验阶段,尽管 Regeneron 已与 Alnylam 合作开发一种沉默 CIDEB 基因的 siRNA 治疗候选药物。
GluK2 是耐药性颞叶癫痫基因治疗的靶点
目的:颞叶癫痫 (TLE) 的特征是边缘系统(尤其是海马)中反复发作癫痫。在 TLE 中,从齿状回颗粒细胞 (DGC) 中反复出现的苔藓纤维在 DGC 之间形成异常的致癫痫网络,该网络通过异位表达的含 GluK2/GluK5 的海人酸受体 (KAR) 起作用。TLE 患者通常对抗癫痫药物有抵抗力,并患有严重的合并症;因此,迫切需要新的治疗方法。之前,我们已经证明 GluK2 基因敲除小鼠可以免受癫痫发作的影响。本研究旨在提供证据,证明使用基因疗法下调海马中的 KAR 可以减少 TLE 中的慢性癫痫放电。方法:我们将分子生物学和电生理学结合到啮齿类 TLE 模型和从耐药性 TLE 患者手术切除的海马切片中。结果:在这里,我们确认了使用非选择性 KAR 拮抗剂抑制 KAR 的转化潜力,该拮抗剂显着减弱了 TLE 患者来源的海马切片中的发作间期样癫痫样放电 (IED)。表达抗 grik2 miRNA 的腺相关病毒 (AAV) 血清型 9 载体被设计为特异性下调 GluK2 表达。将 AAV9-抗 grik2 miRNA 直接递送到 TLE 小鼠的海马中可显着减少癫痫发作活动。TLE 患者海马切片的转导降低了 GluK2 蛋白的水平,最重要的是,显着减少了 IED。解释:我们抑制异常 GluK2 表达的基因沉默策略可抑制小鼠 TLE 模型中的慢性癫痫发作以及来自 TLE 患者的培养切片中的 IED。这些结果为针对耐药性 TLE 患者的 GluK2 KAR 基因治疗方法提供了概念验证。ANN NEUROL 2023;00:1 – 17
广泛的突变靶点解释了快速的表型进化速度
摘要 生物体某一分支中某一性状的快速进化可以用自然选择的持续作用或高突变方差(即在自发突变下发生变化的倾向)来解释。高突变方差的原因仍然难以捉摸。在某些情况下,快速进化取决于一个或几个具有短串联重复序列的基因座的高突变率。在这里,我们报告了隐杆线虫外阴前体细胞中进化最快的细胞命运,即 P3.p。我们识别并验证了 P3.p 高突变方差的因果突变。我们发现这些位置不表现出任何高突变率的特征,分散在整个基因组中,相应的基因属于不同的生物途径。我们的数据表明,广泛的突变靶标大小是高突变方差和相应的快速表型进化率的原因。
癌症和慢性炎症性疾病中的可溶性CD95L,一个新的治疗靶点?
尽管CD95L(也称为FASL)仍被视为诱导感染和转化细胞中凋亡的死亡配体,但大量证据表明,它还可以触发非凋亡信号传导途径,其病理生理作用仍被充分阐明。跨膜配体CD95L属于肿瘤坏死因子(TNF)超家族。在金属蛋白酶裂解后,其可溶性形式(S-CD95L)无法触发凋亡程序,而是引起信号通路,促进了促进某些炎症性疾病(如自身免疫性疾病和癌症)的侵略性。我们建议评估累积金属蛋白酶切割的CD95L的各种病理,并分析该可溶性配体是否在病理进展中起重要作用。基于tnf tnf -argeting Therapeutics,我们设想靶向CD95L的可溶性形式可能代表了本文所示的病理学中非常有吸引力的治疗选择。
验证细胞表面蛋白酶作为癌症治疗的药物靶点:我们知道什么?我们要做什么?
摘要:细胞表面蛋白酶(也称为外蛋白酶)是跨膜和膜结合酶,参与各种生理和病理过程。几个成员,最显著的是二肽基肽酶 4 (DPP4/CD26) 及其相关家族成员成纤维细胞活化蛋白 (FAP)、氨基肽酶 N (APN/CD13)、解整合素和金属蛋白酶 17 (ADAM17/TACE) 以及基质金属蛋白酶 (MMP) MMP2 和 MMP9,通常在癌症中过度表达并与肿瘤功能障碍有关。由于这些外蛋白酶具有多方面的作用,已被证实是癌症的治疗靶点。已经开发出许多抑制剂来靶向这些酶,试图控制它们的酶活性。尽管这些化合物的临床试验在大多数情况下没有显示出预期的结果,但外蛋白酶抑制剂领域正在不断发展。本综述总结了目前关于该主题的知识,并重点介绍了最近开发的更有效、更有选择性的靶向外蛋白酶的药物,其中包括小分子量抑制剂、肽缀合物、前药或单克隆抗体 (mAb) 及其衍生物。这些有希望的途径有可能为癌症治疗提供新的治疗策略。
机器学习预测肥胖相关肠道菌群:确定假链双歧杆菌作为潜在治疗靶点
超重和肥胖是全球重大的公共卫生挑战,带来了巨大的临床困难(Laine 和 Wee,2023 年)。肥胖是各种广泛性疾病的主要前兆,包括 2 型糖尿病、高血压、非酒精性脂肪肝、癌症和阻塞性睡眠呼吸暂停综合征(Tsai 和 Bessesen,2019 年;Quek 等人,2023 年)。尽管为治疗、缓解和预防做出了许多努力,但全球肥胖的患病率和严重程度仍在持续上升(Heindel 等人,2024 年)。从病因上讲,肥胖是一种复杂的疾病,主要由遗传和环境因素的相互作用驱动(Laine 和 Wee,2023 年)。因此,有效的肥胖治疗需要采用多学科方法(Velazquez 和 Apovian,2018 年),凸显了对创新预防和治疗策略的迫切需求。
T 细胞受体 (TCR) 信号传导的细胞内负调节剂作为潜在的抗肿瘤免疫治疗靶点
摘要 免疫治疗策略旨在通过主要针对 T 细胞来调动针对肿瘤细胞的免疫防御。共抑制受体或免疫检查点 (ICP)(例如 PD-1 和 CTLA4)可以限制 T 细胞受体 (TCR) 信号在 T 细胞中的传播。基于抗体的免疫检查点阻断(免疫检查点抑制剂,ICI)可以逃避 ICP 对 TCR 信号的抑制。ICI 疗法已显著影响癌症患者的预后和生存。然而,许多患者对这些治疗仍然有抵抗力。因此,需要替代的癌症免疫治疗方法。除了膜相关抑制分子外,越来越多的细胞内分子也可能起到下调由 TCR 参与触发的信号级联的作用。这些分子被称为细胞内免疫检查点 (iICP)。阻断这些细胞内负信号分子的表达或活性是增强 T 细胞介导的抗肿瘤反应的一个新领域。这个领域正在迅速扩大。事实上,已经发现了 30 多种不同的潜在 iICP。在过去 5 年中,已经注册了多项针对 T 细胞中 iICP 的 I/II 期临床试验。在本研究中,我们总结了最近的临床前和临床数据,证明针对 T 细胞 iICP 的免疫疗法可以介导实体瘤(包括(膜相关)免疫检查点抑制剂难治性癌症)的消退。最后,我们讨论了如何靶向和控制这些 iICP。因此,iICP 抑制是一种有前途的策略,为未来的癌症免疫疗法开辟了新途径。
治愈HBV感染的最终治疗靶点
关键点54•HBV感染导致在感染细胞的核中建立了病毒cccDNA微型55的池,这是导致病毒持久性的。56•当前的HBV建议疗法有效地实现病毒抑制57改善患者的生活质量;但是,他们无法消除病毒58微型浓度小体,因此可以治愈CHB。59•当前治疗研究的下一个可实现目标是实现有限治疗后的60治疗,从而导致循环中的HBSAG抑制。61•针对直接CCCDNA靶向的疗法,要么为其降解,主HBV蛋白中的致命62突变或转录沉默正在积极地被探索63。64•对CCCDNA生物学的全面了解对于寻找潜在的可药65靶标并实现HBV靶向疗法仍然至关重要。66•临床前研究中有希望的直接CCCDNA靶向方法,目的是减少或沉默病毒的微型浓度储层,以克服交付,68个安全性和可行性问题。69 70 71 72 73 74 75 76 77 77 79 79 80 81 82 83 84 85 86 87 87 88 89 90 91 91 92 92 93 94
tau蛋白作为癌症的治疗靶点?专注于胶质母细胞瘤
摘要:尽管经过广泛研究了几十年,但微管相关的蛋白质Tau尚未揭示其秘密。长期以来,tau以其促进微管组装的能力而闻名。TAU的一个鲜为人知的特征是它与癌症相关蛋白激酶结合的能力,这表明TAU在调节与肿瘤发生相关的微管非依赖性细胞途径中的可能作用。有意为癌症找到新的治疗靶标,似乎必须检查Tau与这些激酶及其后果的相互作用。本综述旨在收集支持Tau与癌症之间关系的文献数据,特别着重于胶质母细胞瘤肿瘤,其中Tau的病理学意义在很大程度上没有探索。,我们将从机械的角度将这一主题视为tau在致癌过程中的关键作用。然后,我们将讨论TAU参与胶质母细胞瘤中关键途径失调的参与。最后,我们将概述靶向tau蛋白治疗胶质母细胞瘤的有希望的策略。