XiaoMi-AI文件搜索系统
World File Search System标志146皮肤黑色素瘤2023 Update
不可能完全消除这些来源的任何可能的偏见,甚至不可能确定地量化偏见程度。标志要求所有参与指南开发工作的人应每年宣布直接或间接的所有财务和学术利益,只要他们积极与组织积极合作。通过明确说明贡献者受到的影响,标志承认偏见的风险,并使指南用户或审阅者可以自己评估自己的结论和指南建议是基于对证据的偏见解释的可能性。
口腔黑色素瘤犬的靶向免疫:兽医
摘要 背景 黑色素瘤是人类最致命的皮肤癌。传统疗法疗效有限,而且考虑到免疫检查点抑制剂仅在一小部分患者中产生持久的临床反应,总体反应仍然不令人满意。这促使我们开发了一种以肿瘤抗原硫酸软骨素蛋白聚糖 (CSPG)4 为靶点的疫苗接种策略。 方法 为了克服宿主对自身抗原 CSPG4 的无反应性,我们利用了 CSPG4 序列在系统发育进化中的保守性,因此我们使用了一种基于嵌合 DNA 分子的疫苗,该分子包含 CSPG4 的人类 (Hu) 和狗 (Do) 部分 (HuDo-CSPG4)。我们已经在一项前瞻性、非随机兽医临床试验中测试了它的安全性和免疫原性(主要目标)以及治疗效果(次要结果),该试验招募了 80 只客户所拥有的、已通过手术切除的、CSPG4 阳性、II-IV 期口腔黑色素瘤的狗。结果接种疫苗的狗产生了抗 Do-CSPG4 和 Hu-CSPG4 免疫反应。有趣的是,接种疫苗的狗的抗体滴度与总体生存率显着相关。我们的数据表明,与仅接受常规疗法治疗的对照组相比,HuDo-CSPG4 疫苗接种可能有助于提高接种疫苗的狗的生存率。结论 HuDo-CSPG4 佐剂疫苗接种对患有口腔黑色素瘤的狗是安全且具有免疫原性的,并可能对疾病过程产生有益影响。由于自然发生的犬肿瘤作为癌症免疫治疗反应的预测模型的强大作用,这些数据可能为将这种方法转化为治疗 CSPG4 阳性黑色素瘤亚型的人类患者奠定基础。
对治疗黑色素瘤的当前和管道药物的综述
摘要:恶性黑色素瘤是皮肤癌最具侵略性的形式。标准治疗方案包括手术,放射治疗,全身化疗,靶向治疗和免疫疗法。结合这些方式通常会产生更好的反应。手术适用于局部病例,有时涉及淋巴结清扫和活检,以评估疾病的传播。raviation治疗有时可以用作独立治疗或手术切除后。全身化疗虽然较低,但被用作组合治疗的一部分,或者在其他方法失败时使用。发展对系统性化学疗法和相关副作用的耐药性促使对新方法进行了进一步的研究和临床试验。在晚期黑色素瘤的情况下,可能需要一种全面的方法,结合了靶向疗法和免疫疗法,这些疗法表现出显着的抗肿瘤活性。 有针对性的疗法,包括针对BRAF,MEK,C-KIT和NRA的抑制剂,旨在阻断负责肿瘤生长的特定分子。 这些疗法表现出希望,特别是在相应突变的患者中。 组合疗法,包括BRAF和MEK抑制剂,已证明可以提高无进展的生存。但是,对抵抗和皮肤毒性的担忧突出了对密切监测的需求。 免疫疗法,利用肿瘤淋巴细胞和CAR T细胞,增强了免疫反应。 正在进行的试验继续探索CAR T细胞疗法对晚期黑色素瘤的功效。在晚期黑色素瘤的情况下,可能需要一种全面的方法,结合了靶向疗法和免疫疗法,这些疗法表现出显着的抗肿瘤活性。有针对性的疗法,包括针对BRAF,MEK,C-KIT和NRA的抑制剂,旨在阻断负责肿瘤生长的特定分子。这些疗法表现出希望,特别是在相应突变的患者中。组合疗法,包括BRAF和MEK抑制剂,已证明可以提高无进展的生存。但是,对抵抗和皮肤毒性的担忧突出了对密切监测的需求。免疫疗法,利用肿瘤淋巴细胞和CAR T细胞,增强了免疫反应。正在进行的试验继续探索CAR T细胞疗法对晚期黑色素瘤的功效。Lifileucel是一种由FDA批准的肿瘤浸润淋巴细胞疗法,已显示出晚期黑色素瘤的反应率提高了。靶向CTLA-4和PD-1的检查点抑制剂具有增强的结果。急诊IL-2疗法增强了树突状细胞,增强了抗癌免疫力。 溶瘤病毒疗法,已批准用于晚期黑色素瘤,增强了联合方法中的治疗功效。 免疫疗法具有明显的晚期黑色素瘤疗法,但其成功却有所不同,促使人们发现新药和影响结果的因素。 本综述提供了对当前黑色素瘤治疗和最近治疗进展的见解。急诊IL-2疗法增强了树突状细胞,增强了抗癌免疫力。溶瘤病毒疗法,已批准用于晚期黑色素瘤,增强了联合方法中的治疗功效。免疫疗法具有明显的晚期黑色素瘤疗法,但其成功却有所不同,促使人们发现新药和影响结果的因素。本综述提供了对当前黑色素瘤治疗和最近治疗进展的见解。
黑色素瘤的新疗法:当前趋势、发展...
黑色素瘤是一种侵袭性皮肤癌,全球发病率和死亡率不断上升。多年来,治疗策略仅限于手术、放疗和化疗。免疫学和癌症生物学的最新进展导致了免疫检查点抑制剂 (ICI) 和靶向疗法等新型疗法的发现和开发,这些疗法彻底改变了转移性黑色素瘤患者的临床护理。尽管最近 ICI 取得了成功,但许多黑色素瘤患者并没有从 ICI 疗法中获得长期益处,这凸显了对具有新靶点(如淋巴细胞激活基因 3 (LAG-3))的替代疗法的需求。在这篇综述中,我们探讨了正在早期临床试验中测试的新型治疗剂和新型组合。我们讨论了较有前途的新型工具,例如纳米技术,以开发充当药物载体和/或光吸收剂的纳米系统,从而可能改善治疗结果。最后,我们还强调了诸如耐药后管理等挑战
p53 家族对黑色素瘤靶向治疗的耐药性
摘要:转移性黑色素瘤是最具侵袭性的肿瘤之一,其频繁突变会影响 MAPK 通路的组成部分,主要是蛋白激酶 BRAF。尽管对 BRAF 抑制剂的初始反应很有希望,但黑色素瘤会因耐药性的产生而进展。除了频繁重新激活 MAPK 或激活 PI3K/AKT 信号通路外,最近还有研究表明 p53 通路会导致对靶向 MAPK 抑制剂治疗的获得性耐药。经典肿瘤抑制因子 p53 在黑色素瘤中通过多种机制失活。TP53 基因和其他两个家族成员 TP63 和 TP73 编码多种蛋白质亚型,这些亚型在肿瘤发生过程中表现出不同的功能。p53 家族亚型可以通过使用替代启动子和/或在 C 端和 N 端剪接来产生。各种 p53 家族亚型在黑色素瘤细胞系和肿瘤样本中都有表达,其中几种亚型已被证实在黑色素瘤中具有特定功能,影响增殖、存活、转移潜能、侵袭、迁移和治疗反应。特别令人感兴趣的是 p53 家族亚型表达增加,并直接参与黑色素瘤细胞对 MAPK 抑制剂的获得性耐药性,这意味着调节它们的表达或靶向它们的功能通路可能是克服黑色素瘤对 MAPK 抑制剂耐药性的潜在治疗策略。
绘制肢端黑色素瘤的单细胞景观图和……
编辑评价 从历史上看,肢端黑色素瘤的研究一直被忽视,因为在欧洲血统的个人中,肢端黑色素瘤占所有黑色素瘤病例的比例很低,这导致该领域存在重要的知识空白,并阻碍了控制该疾病的有效疗法的开发。因此,针对黑色素瘤研究中这一未满足需求的研究非常重要。在这里,何和合作者通过单细胞 RNA 测序分析了六名肢端黑色素瘤患者的八个样本。他们描述了这些肿瘤中的肿瘤微环境,包括对肿瘤微环境中不同细胞类型之间相互作用的描述和潜在的生物标志物。这项研究将有助于我们了解这种类型癌症的免疫浸润,并且是更好地理解这些细胞相互作用如何影响肢端黑色素瘤的发展、进展和治疗反应的重要一步。
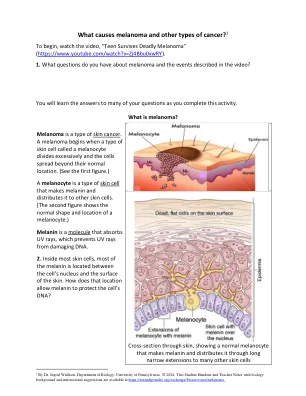
是什么引起黑色素瘤和其他类型的癌症?1
C.如果免疫细胞和手术没有消除所有黑色素瘤细胞,那么存活的黑色素瘤细胞可以在肺,肝或其他器官中建立转移性黑色素瘤。转移性黑色素瘤可以通过干扰其所在的器官的功能,并使用如此多的营养来杀死一个人,以至于人体其余部分的健康细胞无法获得足够的营养。4a。视频中的第一位青少年的第一位医生删除了她脸上的黑色素瘤。但是,他警告她,黑色素瘤可以在五年内杀死她。去除脸上的黑色素瘤后,黑色素瘤细胞在她体内可以在哪里?4B。黑色素瘤最终如何导致她的死亡?为了防止黑色素瘤可能杀死这名少年,她的第二位医生去除了淋巴结(如果它们含有黑色素瘤细胞)。他还开了药物,以帮助她的免疫细胞更有效地识别和破坏黑色素瘤细胞。
lncRNA在肿瘤微环境及黑色素瘤免疫治疗中的作用
黑色素瘤是恶性程度最高、转移性最强的肿瘤之一,免疫治疗和靶向治疗对黑色素瘤有一定的治疗作用,但相当一部分患者在治疗后仍然产生耐药性。最近的研究表明,长链非编码RNA(lncRNA)是公认的癌症调控因子,可以调控细胞增殖、转移、上皮间质转化(EMT)进展和免疫微环境等多种细胞过程。lncRNA在恶性肿瘤中的作用备受关注,而lncRNA与黑色素瘤的关系还有待进一步研究。本文综述了与黑色素瘤发生发展密切相关的抑癌和致癌lncRNA,总结lncRNA在免疫微环境、免疫治疗和靶向治疗中的作用,为临床治疗提供新的靶点和治疗方法。
肢端黑色素瘤的分子特征
摘要................................................................................................................ix
与黑色素瘤免疫治疗相关的皮肤事件:综述
免疫系统在黑色素瘤病程中的作用已得到充分证实。免疫检查点抑制剂在增强免疫系统对抗癌细胞方面显示出良好的前景,并且比过去使用的化疗有更高的反应率 [ 1 , 2 ]。肿瘤细胞通过表达免疫检查点通路的配体来灭活免疫监视过程。免疫检查点抑制剂 (ICI) 是针对两种免疫检查点通路的单克隆抗体:(1) 细胞毒性 T 淋巴细胞抗原 4 (CTLA-4),由活化的 T 细胞表达,在免疫反应期间向 T 细胞活化传递抑制信号,以及 (2) 程序性死亡-1 蛋白 (PD-1),促进淋巴结中 T 细胞凋亡并减少调节性 T 细胞凋亡。T 细胞的这种激活也可能是影响不同器官和系统的免疫相关不良反应 (AE) 发生的原因;尤其是接受 ICI 治疗的患者中,多达 30%–50% 的患者报告出现皮肤相关不良反应 [ 3 ]。在此,我们回顾了 ICI 引起的主要色素沉着变化:白癜风的出现、萨顿现象、黑变病以及头发和指甲毒性。