XiaoMi-AI文件搜索系统
World File Search Systemr e v i w综述了在婴儿和儿童的特应性皮炎治疗中
摘要:特应性皮炎(AD)是一种常见的核和慢性炎症性皮肤病,对患者的生活质量产生了重大影响。它的特征是干性,发痒和湿疹样皮疹。在幼儿中更为普遍,并且与其他各种过敏疾病有关。传统药物治疗对治疗AD的幼儿有一定的局限性。但是,生物制剂在年轻患者的医疗治疗中具有良好的临床应用前景。dupilumab是一种完全人类的单克隆抗体,特异性结合了IL-4Rα亚基,抑制IL-4和IL-13信号传导,并阻止2型炎症反应的发生。它对治疗中度至重度AD的婴儿和儿童具有良好的影响。本综述探讨了杜皮鲁马布在婴儿和儿童中AD治疗的安全性和功效,以及早期干预对AD进展的影响,目的是为使用Dupilumab用于治疗AD的年轻患者的临床实践。关键词:特应性皮炎,杜皮鲁马布,婴儿,儿童,治疗
延迟型高敏性胃肠道症状是由食物口服免疫疗法诱导的,并通过杜皮鲁马布有效治疗的:病例报告
这是根据Creative Commons Attribution-Noncormercial-Noderivs许可条款的开放访问文章,该许可允许在任何媒介中使用和分发,只要正确地提到了原始工作,该使用是非商业用途,并且没有进行修改或改编。©2023作者。由欧洲过敏和临床免疫学学院出版的儿科过敏和免疫学和约翰·威利(John Wiley&Sons Ltd)。
EASI p‐EASI:使用血清生物标志物组合预测接受 dupilumab 治疗的特应性皮炎患者的病情严重程度
1. Flohr C. 特应性皮炎临床试验诊断标准和结果测量:仍然一团糟。J Invest Dermatol。2011;131(3):557-559。2. Thijs J、Krastev T、Weidinger S 等人。特应性皮炎的生物标志物:系统评价和荟萃分析。Curr Opin Allergy Clin Immunol。2015;15(5):453-460。3. Thijs JL、Drylewicz J、Fiechter R 等人。EASI p-EASI:利用血清生物标志物组合为特应性皮炎患者的疾病严重程度提供客观测量工具。J Allergy Clin Immunol。2017;140(6):1703-1705。 4. Walker C、Kagi MK、Ingold P 等。特应性皮炎:外周血 T 细胞活化、嗜酸性粒细胞增多症和血清因子与临床严重程度的相关性。临床实验过敏。1993;23(2):145-153。5. Nograles KE、Zaba LC、Guttman-Yassky E 等。Th17 细胞因子白细胞介素 (IL)-17 和 IL-22 调节不同的炎症和角质形成细胞反应途径。英国皮肤病学杂志。2008;159(5):1092-1102。6. Thijs JL、Drylewicz J、Bruijnzeel-Koomen C 等。 EASI p-EASI:预测接受环孢素 A 治疗的特应性皮炎患者的病情严重程度。过敏。2019;74(3):613-617。7. Paller AS、Kabashima K、Bieber T。特应性皮炎的治疗渠道:干旱的结束?过敏临床免疫学杂志。2017;140(3):633-643。8. Ariens LF、van der Schaft J、Bakker DS 等人。Dupilumab 对大量难治性成人特应性皮炎患者非常有效:来自 BioDay 登记处的首批临床和生物标志物结果。过敏 2019;75(1):116-126。 9. Furue M, Sugiyama H, Tsukamoto K, Ohtake N, Tamaki K. 特应性皮炎患者血清可溶性 IL-2 受体 (sIL-2R) 和嗜酸性粒细胞阳离子蛋白 (ECP) 水平。J Dermatol Sci 。1994;7(2):89-95。10. Guttman-Yassky E, Bissonnette R, Ungar B 等人。Dupilumab 可逐步改善特应性皮炎患者的全身和皮肤异常。J Allergy Clin Immunol 。2019;143(1):155-172。
EASI p‐EASI:使用血清生物标志物组合预测接受 dupilumab 治疗的特应性皮炎患者的病情严重程度
1. Flohr C. 特应性皮炎临床试验诊断标准和结果测量:仍然一团糟。J Invest Dermatol。2011;131(3):557-559。2. Thijs J、Krastev T、Weidinger S 等人。特应性皮炎的生物标志物:系统评价和荟萃分析。Curr Opin Allergy Clin Immunol。2015;15(5):453-460。3. Thijs JL、Drylewicz J、Fiechter R 等人。EASI p-EASI:利用血清生物标志物组合为特应性皮炎患者的疾病严重程度提供客观测量工具。J Allergy Clin Immunol。2017;140(6):1703-1705。 4. Walker C、Kagi MK、Ingold P 等。特应性皮炎:外周血 T 细胞活化、嗜酸性粒细胞增多症和血清因子与临床严重程度的相关性。临床实验过敏。1993;23(2):145-153。5. Nograles KE、Zaba LC、Guttman-Yassky E 等。Th17 细胞因子白细胞介素 (IL)-17 和 IL-22 调节不同的炎症和角质形成细胞反应途径。英国皮肤病学杂志。2008;159(5):1092-1102。6. Thijs JL、Drylewicz J、Bruijnzeel-Koomen C 等。 EASI p-EASI:预测接受环孢素 A 治疗的特应性皮炎患者的病情严重程度。过敏。2019;74(3):613-617。7. Paller AS、Kabashima K、Bieber T。特应性皮炎的治疗渠道:干旱的结束?过敏临床免疫学杂志。2017;140(3):633-643。8. Ariens LF、van der Schaft J、Bakker DS 等人。Dupilumab 对大量难治性成人特应性皮炎患者非常有效:来自 BioDay 登记处的首批临床和生物标志物结果。过敏 2019;75(1):116-126。 9. Furue M, Sugiyama H, Tsukamoto K, Ohtake N, Tamaki K. 特应性皮炎患者血清可溶性 IL-2 受体 (sIL-2R) 和嗜酸性粒细胞阳离子蛋白 (ECP) 水平。J Dermatol Sci 。1994;7(2):89-95。10. Guttman-Yassky E, Bissonnette R, Ungar B 等人。Dupilumab 可逐步改善特应性皮炎患者的全身和皮肤异常。J Allergy Clin Immunol 。2019;143(1):155-172。
审查 Dupilumab 和 Tralokinumab 治疗肿瘤患者特应性皮炎和瘙痒性皮肤病的有效性和安全性:
简介:癌症患者越来越多地被确诊患有特应性皮炎 (AD) 和瘙痒性皮肤病。在有癌症病史或同时患有癌症的患者中,这些疾病的治疗面临着独特的挑战,因为传统的全身疗法可能因其免疫抑制作用而带来风险。近年来,dupilumab 和 tralokinumab 等生物制剂已成为治疗 AD 的有希望的药物,它们可以针对性地调节免疫反应,并且全身副作用可能更少。本文旨在回顾 dupilumab 和 tralokinumab 在治疗癌症幸存者的 AD 和瘙痒症方面的安全性和有效性的现有证据,并探讨这一独特患者群体的潜在益处和注意事项。方法:对截至 2024 年 12 月 15 日的 PubMed、Ovid、Scopus、Embase 和 Cochrane Library 数据库中的当前医学文献进行了全面分析。在进行此叙述性综述时,采用了与临床试验和现实研究相关的医学主题词 (MeSH) 术语和医学术语,重点关注药物 dupilumab 和 tralokinumab。讨论:患有活动性或既往癌症的患者通常被排除在新药的临床试验之外,这使得评估这些患者的癌症进展或复发风险变得复杂。dupilumab 和 tralokinumab 等生物药物在肿瘤患者中的潜在使用标志着治疗湿疹和瘙痒等疾病的重大突破,这些疾病在该患者群体中很常见。虽然对于患有活动性癌症或有恶性肿瘤病史的患者,没有明确的使用 dupilumab 和 tralokinumab 的禁忌症,但对于在这些情况下使用它们没有明确的指导。在皮肤科医生和肿瘤科医生的合作推动下,现实世界的数据不断涌现,支持 dupilumab 和 tralokinumab 在治疗癌症患者 AD 方面的有效性和安全性。尽管如此,仍需要进行更大规模、更长随访期和专门的药物警戒计划的研究来证实这些发现。关键词:特应性皮炎、dupilumab、tralokinumab、肿瘤患者
针对 2 型炎症治疗大疱性...
大疱性类天疱疮 (BP) 是一种自身免疫性起泡性疾病,常发生于患有瘙痒和紧张性大疱的老年患者。虽然标准治疗包括类固醇、类固醇减量剂和抗炎疗法,但临床医生越来越多地使用非说明书的新型生物制剂治疗难治性病例。我们最近报道了一例使用 dupilumab 成功治疗 BP 的病例,dupilumab 是一种单克隆白细胞介素 4 受体 α (IL-4Rα) 抗体,可通过双重抑制 IL-4 和 IL-13 信号传导来调节 2 型炎症。在这里,我们讨论了 dupilumab 和某些其他生物制剂在治疗 BP 方面的报告疗效如何表明 2 型炎症是 BP 发病机制的重要驱动因素。此外,dupilumab 成功治疗其他瘙痒性皮肤病患者的报告强调了 2 型炎症(特别是通过 IL-4R 信号传导)在慢性瘙痒中的重要性。这些生物疗法的快速发展为炎症性皮肤病的研究和治疗提供了新的机遇。
您问:我正在分析新生物学的用法和...
皮肤病学部门具有以下药物:•Abrocibinqo(Cibinqo) - 0•Barcarciinib(Olumilmit)(Olumilmit) - 25•Dupipumab(34•Alizumab(Xolair)(Xolair)-26•Ulodtraumab(ulodtraumab(Adtranib(Adtranib(Adtranib(Adtranib)(Adtranib(Adtranib))) 0
巴瑞替尼对中度至重度过敏性皮炎的预算影响...
每种治疗的监测要求均基于产品 PI。该模型未纳入任何根据 dupilumab PI 进行的 dupilumab 常规监测 [15]。每种监测资源的成本均基于医疗保险和医疗补助服务中心 (CMS) 医师收费表和 CMS 实验室收费表的国家支付率 [16-17]。总监测成本按年计算;对于接受治疗超过 12 个月的患者,监测资源使用情况和成本假设与 6-12 个月时间范围内的相同。该模型假设治疗第一年的监测资源使用情况更高,因此第一年的年度监测成本高于后续年份(表 3)。
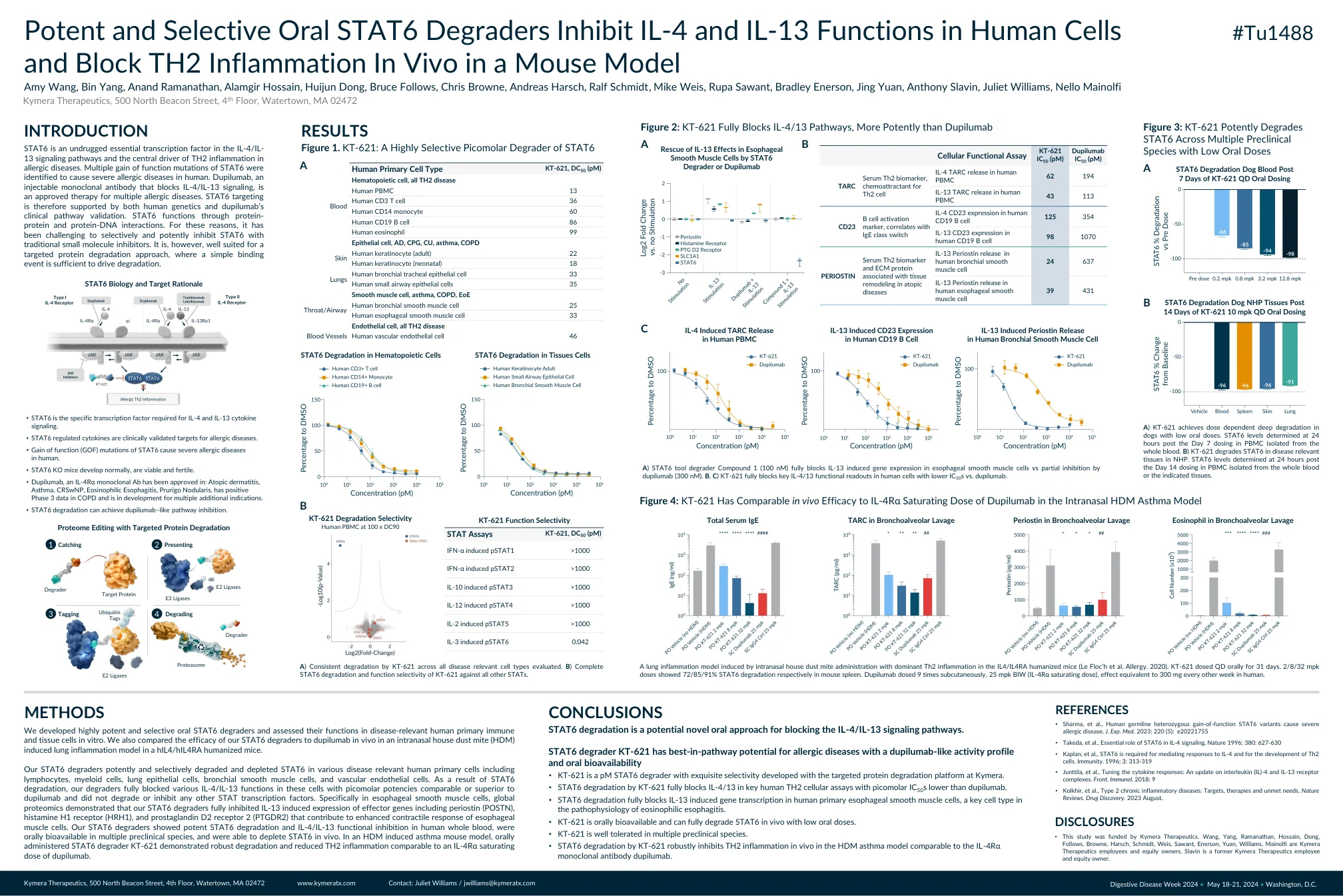
有效的和选择性的口服STAT6降解器抑制人类细胞中的IL-4和IL-13功能,并阻止小鼠模型中的Th2炎症
STAT6是IL-4/IL-13信号通路中的未触发的基本转录因子,并且是过敏性疾病中Th2炎症的中心驱动因素。确定了STAT6功能突变的多重增益,以引起人类严重的过敏性疾病。dupilumab是阻断IL-4/IL-13信号传导的一种可注射的单克隆抗体,是多种过敏性疾病的批准疗法。STAT6靶向受人类遗传学和Dupilumab的临床途径验证的支持。STAT6通过蛋白质蛋白质和蛋白-DNA相互作用发挥作用。由于这些原因,通过传统的小分子抑制剂有选择和有效地抑制STAT6的挑战。非常适合靶向蛋白质降解方法,在该方法中,简单的结合事件足以驱动降解。