XiaoMi-AI文件搜索系统
World File Search System从目标结构和动力学到药物筛查。 -Iris
**首先通过人类细胞中的细胞内NMR筛选蛋白质的药物筛选。化学位移扰动揭示了药物的结合和铅化合物与胞质蛋白Ca II的活性位点的结合。剂量和时间依赖性分析表明,整个膜的配体扩散是缓慢的步骤,与批准药物的效力密切相关。
人类胰腺癌类器官中的药物筛选和基因组编辑可确定药物-基因相互作用和标外治疗候选药物
作者贡献 CKH 和 GS 设计了研究并撰写了论文,其他所有作者也参与其中。CKH 进行了实验并分析了数据,GS 负责监督研究的整体执行。DT、VL、AG 在建立、培养、扩增和测试 PDAC 类器官系方面提供了技术援助。PS 进行并分析了实验并准备了图表。THB、DK、CUS 设计并执行了自动化药物筛选并为分析做出了贡献。CP、DL、KE、AS 提供了病理学/肿瘤学专业知识。LV、FR 建立了野生型胰腺类器官系。LG、DJS、NCT、HK 提供了生物信息学专业知识并为分析做出了贡献。SK、MDM、MKJ 提供了转移性 PDAC 类器官系的数据。JB、JS 为体内研究的设计、实验和分析做出了贡献。
神经类器官
摘要 神经退行性疾病 (NDD) 是一组以神经细胞退化为特征的疾病,包括阿尔茨海默病、帕金森病和亨廷顿病。当前的研究依赖于动物模型和二维细胞培养,限制了疾病的准确复制。然而,源自干细胞的 3D 神经类器官为 NDD 研究提供了令人兴奋的前景。神经类器官与正在发育的人类大脑非常相似,已成为疾病建模和药物筛选的宝贵工具。它们可以分化成特定的神经细胞类型并模拟疾病特异性蛋白质聚集。脑类器官改进了药物筛选,评估了药物对神经活动和 BBB 通透性的影响。挑战包括可重复性、血管化和小胶质细胞掺入。尽管如此,神经类器官代表了 NDD 研究的革命性方法,提供了生理相关模型。随着技术的进步,神经类器官在理解和发现神经退行性疾病药物方面具有巨大的前景。关键词:3D 细胞培养、脑类器官、阿尔茨海默病、帕金森病。
NDSL GL 情况说明书 - Navy.mil
建模为政策和工作与生活的改善提供信息 海军药物筛选实验室 - 大湖区 (NDSL-GL) 领导层希望不断提高效率、避免错误并提高实验室标本接收部分的吞吐量。标本量大和筛选过程时间长导致 NDSL-GL 领导层寻求替代方案以减少加班并改善工作与生活的平衡。我们分析了在药物筛选过程中从线性 (1D) 条形码转换为二维 (2D) 条形码以进行样本识别的效果。我们还比较了替代工作时间表的工作效率,特别是标准的 8 小时、每周 5 天与 10 小时、每周 4 天。模拟结果表明,实施 2D 条形码系统可能会显著提高标本的吞吐量,这得到了证实,并减少了加班的需求。模型结果显示生产率没有下降,或略有提高,这让 NDSL-GL 领导层有信心引入替代工作时间表。模型结果还用于制定替代工作时间表的政策,根据他们的气候调查结果,“工作与生活的平衡度大大提高。” 了解更多信息:www.med.navy.mil/Navy-Marine-Corps-Public-Health-Center/Population-Health/Health-Analysis/
临床前嗜铬细胞瘤和副神经节瘤模型_细胞系、动物模型和人类原代培养模型
尽管数十年的研究证明建立人类嗜铬细胞瘤和副神经节瘤 (PPGL) 细胞系尤为困难,但目前还有其他可靠的临床前 PPGL 模型可用。本综述总结了这些模型,以及我们最近使用患者来源的 PPGL 原代培养物建立的个性化药物筛选平台。当前可用的 PPGL 模型包括小鼠和大鼠 PPGL 细胞系(其中只有一个细胞系(PC12)可通过细胞库公开访问)和 PPGL 动物模型(其中患者来源的异种移植模型很有前景但建立起来很复杂)。我们已经开发出下一代人类 PPGL 原代培养物实施方案,能够根据肿瘤独特的遗传、生化、免疫组织化学和临床特征进行可靠和个性化的药物筛选,以及对肿瘤药物反应性的个体化分析。总体而言,可靠的 PPGL 模型(包括患者来源的原代培养模型)对于推进 PPGL 领域的临床前研究至关重要。© 2024 作者。由 Elsevier Ltd. 出版。这是一篇根据 CC BY 许可开放获取的文章(http://creativecommons.org/licenses/by/4.0/)。
斑马鱼药物筛选证实厄洛替尼是 T 细胞急性淋巴细胞白血病中 Wnt/β-Catenin 信号和自我更新的抑制剂
图 1:6xTCF/LEF-miniP:GFP 斑马鱼系对 Wnt 信号通路的小分子调节剂产生可量化的反应。(A) Wnt/β-catenin GFP 报告基因 6xTCF/LEF-miniP:dGFP 转基因斑马鱼系的示意图。(B) 受精后 48 小时 (hpf) 的 6xTCF/LEF-miniP:dGFP 斑马鱼幼虫。GFP 荧光表明 Wnt 信号活跃,尾鳍 (虚线框) 用于量化。(C) 用 DMSO、Wnt 通路抑制剂 XAV939 或 Wnt 通路激活剂 BIO 处理 24 小时的 6xTCF/LEF- miniP:dGFP 幼虫中的代表性尾鳍荧光。从左到右的面板显示了明场图像、GFP 荧光和使用 ImageJ 软件对荧光进行标准化阈值处理。图中标出了与 DMSO 相比荧光增加或减少的百分比。比例尺 = 500 μm。
病例报告:Sortina 制药公司使用 Iscaffpharma 公司的患者衍生支架进行癌症药物筛选摘要:Sortina 制药公司基于 PDS 技术
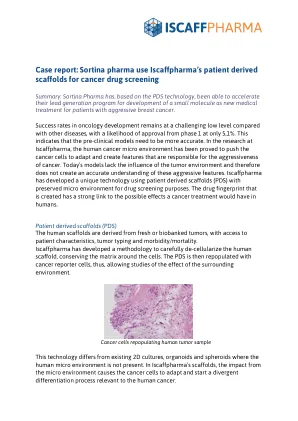
病例报告:Sortina pharma 使用 Iscaffpharma 的患者来源支架进行癌症药物筛选 摘要:Sortina Pharma 基于 PDS 技术,已经能够加速其潜在客户生成计划,以开发一种小分子作为侵袭性乳腺癌患者的新医疗方法。与其他疾病相比,肿瘤学开发的成功率仍然处于具有挑战性的低水平,从第一阶段获得批准的可能性仅为 5.1%。这表明临床前模型需要更准确。在 Iscaffpharma 的研究中,人类癌症微环境已被证明会促使癌细胞适应并产生导致癌症侵袭性的特征。当今的模型缺乏肿瘤环境的影响,因此无法准确了解这些侵袭性特征。Iscaffpharma 开发了一种独特的技术,使用具有保留微环境的患者来源支架 (PDS) 进行药物筛选。创建的药物指纹与癌症治疗对人类的可能影响有着密切的联系。患者来源的支架 (PDS) 人体支架来自新鲜或生物库中的肿瘤,可了解患者特征、肿瘤类型和发病率/死亡率。Iscaffpharma 开发了一种仔细去除人体支架细胞的方法,保留了细胞周围的基质。然后将癌症报告细胞重新植入 PDS,从而可以研究周围环境的影响。
肺癌类器官:临床前研究和精准医疗的模型
肺癌是全球发病率和死亡率较高的恶性肿瘤,5年生存率仅为10%-20%。不同肺癌患者的临床表现、组织学特征、多组学表现和药物敏感性存在显著的异质性,需要制定个性化的治疗策略。目前以病理和基因组多组学检测为主的肺癌精准医疗无法满足临床难治性肺癌患者的需求。肺癌类器官(LCO)来源于肿瘤组织内的肿瘤细胞,通过三维组织培养生成,能够真实地复现体内肿瘤的特征和异质性。系列LCO生物库的建立为高效筛选和鉴定抗肿瘤药物新靶点提供了良好的平台。此外,LCO 还提供了补充决策因素以增强当前的肺癌精准医疗,从而解决了病理引导方法在治疗难治性肺癌方面的局限性。本文全面回顾了 LCO 的构建方法及其在临床前和临床研究中的潜在应用。它强调了 LCO 在生物标志物探索、耐药性调查、靶标识别、临床精准药物筛选以及基于微流控技术的高通量药物筛选策略中的重要性。此外,它还讨论了该领域目前的局限性和未来前景。
正则化函数回归模型可实现转录组范围内癌症药物反应剂量依赖性关联研究
图 1. 用于识别基因与药物之间剂量依赖性关联的两阶段算法。来自药物筛选研究(例如 GDSC)的基因表达和药物反应数据用于拟合我们的剂量变化系数模型,以估计协变量与药物反应之间的剂量变化效应。应用两阶段变量筛选和选择算法对基因-药物关联进行排序。然后可以使用所选基因来预测目标药物的剂量依赖性反应。