XiaoMi-AI文件搜索系统
World File Search SystemSEC(新药研究)会议于 07.10 举行。......
该公司向委员会提交了第三阶段临床试验研究报告。经过详细审议,委员会根据该公司提交的 CSR 建议生产和销售以下适应症:用于治疗患有社区获得性细菌性肺炎 (CABP) 的成年人 (>18 岁)。该公司必须在获得营销授权 (MA) 后 3 个月内提交第四阶段临床试验方案供委员会审查。
IGFBP3 通过调节晚期前列腺癌中的 EGFR 信号传导来促进对 Olaparib 的耐药性
摘要 奥拉帕尼是一种开创性的 PARP 抑制剂 (PARPi),被批准用于治疗存在 DNA 修复缺陷的去势抵抗性前列腺癌 (CRPC) 肿瘤,但已有临床耐药记录。为了研究获得性耐药性,我们通过对 LNCaP 和 C4-2B 细胞系进行长期奥拉帕尼治疗,开发了奥拉帕尼耐药 (OlapR) 细胞系。在这里,我们发现 IGFBP3 在奥拉帕尼耐药的获得性 (OlapR) 和内在性 (Rv1) 模型中高度表达。我们表明 IGFBP3 表达通过激活 EGFR 和 DNA-PKcs 增强 DNA 修复能力,从而促进奥拉帕尼耐药性。IGFBP3 耗竭通过促进 DNA 损伤积累,随后在耐药模型中促进细胞死亡,从而增强奥拉帕尼的疗效。从机制上看,我们表明,沉默 IGFBP3 或 EGFR 表达会降低细胞活力,并使 OlapR 细胞对 Olaparib 治疗重新敏感。通过吉非替尼抑制 EGFR 可抑制 OlapR 细胞的生长并提高 Olaparib 敏感性,从而模拟 IGFBP3 抑制。总之,我们的结果强调 IGFBP3 和 EGFR 是 Olaparib 耐药性的关键介质。
雷诺嗪诱导的代谢重组可改善黑色素瘤对靶向治疗和免疫治疗的反应
黑色素瘤对靶向治疗和免疫治疗的耐药性与代谢重组有关。在这里,我们表明,在长期 BRAF 抑制剂 (BRAFi) 治疗期间,脂肪酸氧化 (FAO) 增加会导致小鼠获得性治疗耐药性。使用美国食品药品管理局和欧洲药品管理局批准的抗心绞痛药物雷诺嗪 (RANO) 靶向 FAO 可延缓获得性 BRAFi 耐药性的肿瘤复发。单细胞 RNA 测序分析表明,RANO 减少了对治疗有抵抗力的 NGFR hi 神经嵴干细胞亚群的丰度。此外,通过重新连接蛋氨酸挽救途径,RANO 通过增加抗原呈递和干扰素信号传导来增强黑色素瘤的免疫原性。RANO 与抗 PD-L1 抗体的结合通过增加抗肿瘤免疫反应大大提高了生存率。总之,我们表明 RANO 通过对 FAO 和蛋氨酸挽救途径的影响提高了靶向黑色素瘤治疗的疗效。重要的是,我们的研究表明 RANO 可以使 BRAFi 抗性肿瘤对免疫疗法敏感。由于 RANO 的副作用非常轻微,它可能成为一种治疗选择,以改进目前用于治疗转移性黑色素瘤的两种主要策略。
100 个自我评估问题
1. 脑肿瘤 2. 急性淋巴细胞白血病 3. 干细胞移植 4. 骨髓增生性疾病、骨髓增生异常性疾病和组织细胞疾病 5. 白细胞疾病 6. 视网膜母细胞瘤、生殖细胞肿瘤和肝母细胞瘤 7. 免疫学和免疫缺陷 8. 神经母细胞瘤和相关肿瘤 9. 肾母细胞瘤和其他肾肿瘤 10. 临床药理学和靶向治疗 11. 血红蛋白病 12. 血液凝固概述和获得性出血性疾病 13. 遗传性出血性疾病 14. 输血医学 15. 血栓性疾病 16. 营养性贫血 17. 肉瘤 18. 急性和慢性粒细胞白血病 19. 生物统计学和流行病学20. 骨髓衰竭21. 癌症倾向22. 先天性和获得性溶血性贫血23. 血小板疾病24. 淋巴瘤25. 肿瘤急症26. 姑息治疗和支持治疗27. 研究伦理和质量改进28. 外周血和骨髓形态学回顾:恶性疾病29. 外周血和骨髓形态学回顾:非恶性血液学30. 生存率31. 血管异常
DigitalCommons@URI - 罗德岛大学
引文/出版商归属 引文/出版商归属 Chen, J., Dai, J., Kang, Z., Yang, T., Zhao, Q., Zhang, X.,...Yang, T. (2020). 一种克服结直肠癌 MEK 抑制原发性和获得性耐药性的组合策略。Experimental Cell Research, 393(1), 112060. https://doi.org/10.1016/j.yexcr.2020.112060 可从以下网址获取:https://doi.org/10.1016/j.yexcr.2020.112060
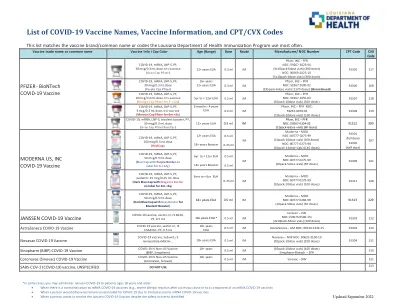
LDH 最常用的 COVID-19 疫苗 2022 年 7 月_Vial Colors.xlsx
*在某些情况下,您可以为 18 岁及以上的患者接种 Janssen COVID-19:• 当存在 mRNA COVID-19 疫苗禁忌症时(例如,在之前接种疫苗后或对 mRNA COVID-19 疫苗的某种成分出现严重过敏反应)• 当一个人由于 mRNA COVID-19 疫苗的可获得性有限而无法接种 COVID-19 疫苗时。• 当一个人尽管发现存在安全问题,但仍想接种 Janssen COVID-19 疫苗时 2022 年 9 月更新
菌血症的危险因素及其对复杂社区获得的尿路感染的临床影响
摘要:菌血症在某些感染中与严重程度有关;但是,它对尿路感染预后(UTI)的影响仍然存在争议。我们的目标是确定细菌血症的危险因素及其对复杂社区获得性尿路感染的住院患者的临床影响。,我们对被复杂社区获得的UTI的医院录取的患者进行了前瞻性观察性研究。比较了有或没有菌血症患者的临床变量和结果,并进行了多变量分析以鉴定菌血症和死亡率的危险因素。在279例社区获得性尿道的患者中,有37.6%的人具有阳性的血液培养。通过多变量分析的菌血症的危险因素是温度≥38℃(p = 0.006,或1.3(95%CI 1.1-1.7))和procalcitonin≥0.5ng/ml(P = 0.005,或8.5(95%CI 2.2-39.4))。院内和30天死亡率分别为9%和13.6%。快速沙发(P = 0.030,或5.4(95%CI 1.2-24.9))和Barthel指数<40%(P = 0.020,或4.8(95%CI 1.3-18.2))与30天的死亡率通过多变量分析有关。然而,菌血症与30天死亡率无关(P = 0.154,或2.7(95%CI 0.7-10.3))。我们的研究发现,高热社区获得的UTI和降低的降钙素是菌血症的危险因素。菌血症患者的结局稍差一些,但死亡率没有显着差异。
了解谱系可塑性是 EGFR 突变型非小细胞肺癌靶向治疗失败的途径
表皮生长因子受体基因 (EGFR) 的体细胞变异会导致激酶信号异常激活,大约 15% 的非小细胞肺癌 (NSCLC) 会出现这种情况。确诊为 EGFR 突变型 NSCLC 的患者对 EGFR 酪氨酸激酶抑制剂 (EGFR TKI) 有良好的初始临床反应,但肿瘤复发很常见并且发展很快。过去十年,人们对 EGFR TKI 获得性耐药机制进行了广泛研究。在理解治疗失败的两种主要途径方面取得了巨大进展:EGFR 基因的其他基因组变异和替代激酶信号激活(所谓的“旁路激活”)。多种旨在克服这些 EGFR TKI 耐药模式的药物已获得 FDA 批准或正在临床开发中。表型转化是一种不太常见且不太清楚的 EGFR TKI 耐药机制,尚待临床解决。在获得性 EGFR TKI 耐药性的情况下,表型转化包括上皮-间质转化 (EMT)、肺腺癌 (LUAD) 向鳞状细胞癌 (SCC) 或小细胞肺癌 (SCLC) 的转化。SCLC 转化或神经内分泌分化与 TP53 和 RB1 信号失活有关。然而,允许谱系转换的确切机制需要进一步研究。最近的报告表明,LUAD 和 SCLC 具有共同的细胞起源,并且在适当的条件下会发生转分化。目前,EGFR 突变型 SCLC 的治疗靶向选择仅限于传统的基因毒性化疗。同样,EMT 相关耐药性的基础尚不清楚。EMT 是一个复杂的过程,其特征是一系列中间状态,上皮和间质因子的表达各不相同。在获得性 EGFR TKI 耐药性的情况下,EMT 经常与旁路激活同时发生,因此很难确定 EMT 对治疗失败的确切贡献。EMT 相关耐药性的可逆性表明其表观遗传起源,并在疾病进展过程中发生其他调整,例如基因改变和旁路激活。本综述将讨论与表型转化相关的 EGFR TKI 耐药性的机制基础,以及在 EGFR 突变型 NSCLC 中解决此类靶向治疗耐药性的挑战和机遇。
引用本文:Kate Dawes、Ashley Carlino、Maayken van den Berg 和 Maggie Killington (2020): 家庭成员之间的不和对孩子的生活产生影响
摘要 目的:调查家庭获得性脑损伤对儿童和成年家庭成员的影响,包括他们对所提供支持的看法、差距和未来干预的建议。研究设计:使用现象学方法的定性探索性研究。方法:从南澳大利亚脑损伤康复服务中心(SABIRS)和南澳大利亚阿德莱德的外部社区脑损伤机构的 12 个家庭中招募了 26 名参与者。16 名 5-18 岁的儿童参加了 10 次半结构化访谈。10 名成年人参加了六次访谈。在转录和成员检查之后,对所有经过开放、轴向和选择性编码的访谈的汇总数据进行主题分析。主要结果:分析揭示了四个主要主题:(1)帮助父母帮助孩子,(2)通过赋予孩子有意义的角色来改善家庭功能,(3)工作人员:不要让孩子“蒙在鼓里”,(4)对儿童的支持不是千篇一律的。结论:儿童和成人报告称,家庭获得性脑损伤后,急性脑损伤服务提供的支持存在显著差距。儿童和成人需要接受除患者之外的干预。为了填补已发现的差距,参与者建议临床工作人员投入更多,包括使用技术;具体来说,开发适合年龄的应用程序、教育视频和互动游戏。
p53 家族对黑色素瘤靶向治疗的耐药性
摘要:转移性黑色素瘤是最具侵袭性的肿瘤之一,其频繁突变会影响 MAPK 通路的组成部分,主要是蛋白激酶 BRAF。尽管对 BRAF 抑制剂的初始反应很有希望,但黑色素瘤会因耐药性的产生而进展。除了频繁重新激活 MAPK 或激活 PI3K/AKT 信号通路外,最近还有研究表明 p53 通路会导致对靶向 MAPK 抑制剂治疗的获得性耐药。经典肿瘤抑制因子 p53 在黑色素瘤中通过多种机制失活。TP53 基因和其他两个家族成员 TP63 和 TP73 编码多种蛋白质亚型,这些亚型在肿瘤发生过程中表现出不同的功能。p53 家族亚型可以通过使用替代启动子和/或在 C 端和 N 端剪接来产生。各种 p53 家族亚型在黑色素瘤细胞系和肿瘤样本中都有表达,其中几种亚型已被证实在黑色素瘤中具有特定功能,影响增殖、存活、转移潜能、侵袭、迁移和治疗反应。特别令人感兴趣的是 p53 家族亚型表达增加,并直接参与黑色素瘤细胞对 MAPK 抑制剂的获得性耐药性,这意味着调节它们的表达或靶向它们的功能通路可能是克服黑色素瘤对 MAPK 抑制剂耐药性的潜在治疗策略。