XiaoMi-AI文件搜索系统
World File Search System2020; 16(14): 2595-2611. doi: 10.7150/ijbs.45886 研究论文 西达本胺使非小细胞肺癌对克唑替尼的敏感性增加 12 倍
引言:克唑替尼是一种靶向c-MET/ALK/ROS1的激酶抑制剂,是治疗ALK突变非小细胞肺癌(NSCLC)的一线药物。尽管35-72%的NSCLC中c-MET经常过表达,但大多数NSCLC主要对克唑替尼治疗有耐药性。方法:使用一组NSCLC细胞系在体外和体内测试西达本胺对原发性克唑替尼耐药的影响。通过一系列分子生物学检测系统地研究了西达本胺的协同作用与c-MET表达和RNA甲基化之间的关系。结果:我们首次发现西达本胺可以在一组无ALK突变的NSCLC细胞系中增强克唑替尼的作用,尤其是那些c-MET表达水平高的细胞系。值得注意的是,在不含肝细胞生长因子 (HGF;一种 c-MET 配体) 的无血清培养基中培养的 NSCLC 细胞对克唑替尼的敏感性,西达本胺无法增加该细胞对克唑替尼的敏感性。相反,在无血清/无 HGF 的培养基中添加 HGF 可以恢复西达本胺的协同作用。此外,用 c-MET 抗体治疗或 siRNA 敲低 c-MET 表达也可以消除西达本胺的协同作用。虽然 c-MET 表达低或无表达的细胞主要对西达本胺-克唑替尼联合治疗具有抗性,但强制 c-MET 过表达可以增加这些细胞对西达本胺-克唑替尼联合治疗的敏感性。此外,西达本胺可以通过下调 METTL3 和 WTAP 表达来抑制 mRNA N6-甲基腺苷 (m6A) 修饰,从而降低 c-MET 表达。西达本胺联合克唑替尼治疗可显著抑制c-MET下游分子的活性。结论:西达本胺通过降低c-MET mRNA的m6A甲基化水平,下调c-MET的表达,从而以c-MET/HGF依赖的方式增加NSCLC细胞对克唑替尼的敏感性。
一个新颖的外显子14跳突变对肺腺癌中克里唑替尼的反应
为了探测靶向治疗的肿瘤的基因组谱,对组织标本和相关的血液样本进行了NGS分析,并确定了Met Exon 14跳过突变(C.3026_3028+11DEL)(图1B和1C)。未发现其他驱动基因变体。突变等位基因频率为33.87%。同样,组织样品的放大片段小于18S rRNA,与Met Exon 14跳过H569细胞系相似,进一步证实了Met Exon 14跳过的出现(图1D)。根据这些发现,患者每天两次开始用250毫克Crizotinib治疗。最值得注意的是,经过一个月的治疗后成像显示肿瘤显着减少。他的肺肿瘤的大小为1.0 cm×0.8 ccm×0.4 cm,符合recist的部分反应标准(-98%,图1E)。这持续了4个月,直到他经历了与疾病无关的死亡。
人乳寡糖:结构和功能
寡糖(来自希腊语ὀλίγοςOlígos,“少数”和σάκχαρSácchar,“糖”)是糖(糖)聚合物,其中包含少量数量(通常为3-10个或更多)单糖(简单糖)。与大多数其他哺乳动物的牛奶不同,人乳是独特的,因为它含有高浓度的150多种不同且结构上不同的寡糖。实际上,对于5-15 g/L,成熟牛奶中的人牛奶寡糖(HMO)的总浓度通常超过人奶蛋白的总浓度,使HMOS成为仅次于简单的牛奶糖乳糖和脂质的第三大分子,而不是计算水[1]。HMO包含多达5个不同的构建块(单糖):葡萄糖(GLC),半乳糖(GAL),N-乙酰基葡萄糖胺(GLCNAC),Fucose(FUC)和唾液酸(SIA)。根据使用了哪些构建块以及如何将它们链接在一起[1],从而生成不同的HMO。图1a显示了HMO结构组件的蓝图。所有HMO在还原端携带乳糖(GALβ1-4GLC)。乳糖可以通过二糖乳糖-N-生物(GALβ1–3GLCNAC)或n-乙酰氨基胺(GALβ1-4GLCNAC)的添加来拉长。乳糖或细长链可以用唾液酸在α2-3-或α2-6-链接中修饰,在α1-2-,α1-3-或α1-3-或α1-4链接中进行葡萄糖基化,从而大大扩展了HMO结构组合的多样性。对于外部,每种唾液酸单糖都包含一个羧基,并引起对HMO分子的负电荷,从而改变了其结构特性。HMO结构通常决定其功能[2]。尽管HMO组成遵循基本的蓝图和150多个不同的HMO,但迄今已确定了150多个不同的HMO,但重要的是要注意,每个女性都合成并分泌出不同的HMO组成曲线,在不同女性之间有很大的不同(图1b),但在同一妇女的哺乳过程中保持相当恒定[3]。到目前为止,我们的实验室已经分析了从世界各地女性收集的10,000多个牛奶样本中的HMO组成,作为各种协作项目的一部分。图1C列出了主成分(PC)图中的某些数据,再次强调了女性之间的HMO组成图谱有所不同,但也存在明显的HMO剖面簇或HMO lactotypes。
无乳链球菌疫苗:现状和...
无乳链球菌是新生儿、老年人和患有合并症的成年人侵袭性感染的主要原因之一。新生儿感染无乳链球菌的主要危险因素是妊娠期间母亲直肠阴道定植,无乳链球菌可导致宫内感染、早产和/或死产 (1)。2020 年,全球约有 2000 万孕妇被这种微生物定植,近 40 万儿童患有早发性无乳链球菌病 (EOD,出生后 0 至 6 天) 或晚发性无乳链球菌病 (LOD,出生后 7 至 89 天)。此外,还有 9 万名儿童死亡,其中近一半发生在撒哈拉以南非洲。2020 年,约有 46,000 例因宫内感染无乳链球菌而导致的死产和超过 500,000 例早产可能与无乳链球菌定植有关 (2)。母体无乳链球菌定植造成的众多负面影响意味着需要采取有效的预防方法来降低多种后果的风险。高收入国家在妊娠晚期末期对被无乳链球菌定植的孕妇进行筛查,并对那些被无乳链球菌定植的孕妇进行分娩期抗生素预防 (IAP)
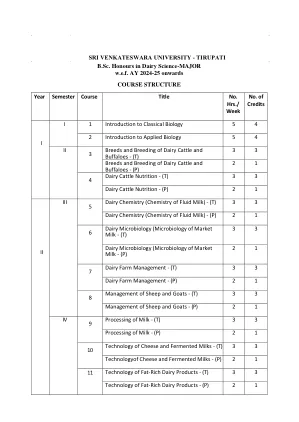
乳业科学-Tirupati
学习成果1。了解生物多样性的分类和保存原则2。了解植物的解剖,生理和生殖过程。3。关于动物分类,生理学,胚胎发展及其经济重要性的知识。4。概述细胞成分,细胞过程,例如细胞分裂,遗传和分子过程。5。理解塑造和驱动大分子和生命过程的化学原理。单元1:系统学,分类学和生态学概论1.1。系统学 - 定义和概念,分类学 - 定义和层次结构。1.2。命名法 - ICBN和ICZN,二项式和三项术命名。1.3。生态学 - 生态系统,生物多样性和保护的概念。1.4。污染和气候变化。单位2:植物学2.1的必需品。植物王国的分类。2.2。植物生理过程(光合作用,呼吸,蒸腾,植物激素)。2.3。花的结构 - 微观和宏观生成,授粉,施肥和
乳杆菌Delbrueckii Letm
L. delbrueckii le tm的delbrueckii形式具有出色的免疫调节特性。它通过非特异性和特定的联系影响先天和适应性免疫,从而根据受试者的免疫状态来控制Th1和Th2途径对免疫反应的协调。通过刺激关键细胞因子IFN,TNF,NK细胞,IL-1,IL-2和IL-6的产生来诱导特定的抗体产生并平衡人免疫系统的能力,以保护感染和癌细胞。它也是一种免疫调节剂,可以通过细胞介导的免疫来平衡和归一化的非特异性反应,并在病原剂存在下诱导更高的反应。它在慢性疾病,炎症和免疫失速(如肿瘤)中提供了免疫平衡(通过抑制)。LE菌株因此调节了对内源性和外源致病剂的免疫反应。
使用四唑测试1
摘要:“ Faveira”(Dimorphandra Gardneriana Tul。)是一种具有巨大商业价值的药用植物,这主要是由于其在全球范围内生产鲁丁的能力。此外,它是提取其他次级代谢产物的原材料来源。这项研究旨在标准化四唑测试的方法,并评估其在估计Faveira不同父植物的种子生存能力方面的适用性。使用四唑(2、3、5-三苯基四唑烷氯化物)确定种子的活力和活力,以四个浓度(0.025、0.050、0.075和0.075和0.1%和0.1%)和四个沉浸周期:30、60、60、90、90和120分钟,与virodition的模式相提并论。发芽和幼苗出现测试。最合适的D. gardneriana种子的制剂在25°C下进行78小时,然后在胚胎相对的区域切割。四唑测试有效地评估了D. gardneriana种子的生存能力和活力,其理想的种子颜色是在40°C下使用0.075%四唑溶液获得120分钟的理想种子颜色。在20个父植物中,父母植物2、3、6、8、9、12和13中的种子最有活力。
泌乳期间的孕产妇饮食干预会影响母乳和人乳微生物
1妇产科,西澳大利亚大学,珀斯,华盛顿州珀斯,澳大利亚6008; azhar.sindi@research.uwa.edu.au或asmsindi@uqu.edu.sa 2 Applied Medical Sciences学院,Umm al-Qura University,Makkah,Makkah 24381-8156,沙特阿拉伯Arabia 3 Abrastia 3 Abrastia Network,perth,Perth,WA 6000,澳大利亚,澳大利亚,澳大利亚,澳大利亚; lisa.stinson@uwa.edu.au(l.f.s. ); zoya.gridneva@uwa.edu.au(Z.G. ); donna.geddes@uwa.edu.au(d.t.g.) 4 UWA人类哺乳研究与翻译中心,珀斯,华盛顿州6009,澳大利亚5分子科学学院,西澳大利亚大学,珀斯,华盛顿州珀斯,澳大利亚6009; Mary.wlodek@uwa.edu.au或m.wlodek@unimelb.edu.au 6农业,食品和葡萄酒学校,阿德莱德大学,阿德莱德大学,阿德莱德,澳大利亚5064,澳大利亚; gabriela.leghivoyer@gmail.com(g.e.l。 ); beverly.muhlhausler@adelaide.edu.au或bev.muhlhausler@csiro.au(b.s.m.) 7妇女和儿童主题,南澳大利亚健康与医学研究所(SAHMRI),阿德莱德,SA 5000,澳大利亚; merryn.netting@adelaide.edu.au 8儿科学学科,阿德莱德大学,阿德莱大学,阿德莱德大学,SA 5006,澳大利亚9号妇女和儿童医院,阿德莱德,澳大利亚10号阿德莱德,澳大利亚10号,澳大利亚10号,妇产科,墨尔本大学,墨尔本大学,澳大利亚墨尔本大学,澳大利亚,澳大利亚3010年,澳大利亚,5000年,澳大利亚,澳大利亚,澳大利亚,澳大利亚3010年,5000年,统计,西澳大利亚大学,珀斯,华盛顿州6009,澳大利亚; Alethea.rea@murdoch.edu.au(A.R. ); michelle.trevenen@uwa.edu.au(M.L.T。)1妇产科,西澳大利亚大学,珀斯,华盛顿州珀斯,澳大利亚6008; azhar.sindi@research.uwa.edu.au或asmsindi@uqu.edu.sa 2 Applied Medical Sciences学院,Umm al-Qura University,Makkah,Makkah 24381-8156,沙特阿拉伯Arabia 3 Abrastia 3 Abrastia Network,perth,Perth,WA 6000,澳大利亚,澳大利亚,澳大利亚,澳大利亚; lisa.stinson@uwa.edu.au(l.f.s.); zoya.gridneva@uwa.edu.au(Z.G.); donna.geddes@uwa.edu.au(d.t.g.)4 UWA人类哺乳研究与翻译中心,珀斯,华盛顿州6009,澳大利亚5分子科学学院,西澳大利亚大学,珀斯,华盛顿州珀斯,澳大利亚6009; Mary.wlodek@uwa.edu.au或m.wlodek@unimelb.edu.au 6农业,食品和葡萄酒学校,阿德莱德大学,阿德莱德大学,阿德莱德,澳大利亚5064,澳大利亚; gabriela.leghivoyer@gmail.com(g.e.l。 ); beverly.muhlhausler@adelaide.edu.au或bev.muhlhausler@csiro.au(b.s.m.) 7妇女和儿童主题,南澳大利亚健康与医学研究所(SAHMRI),阿德莱德,SA 5000,澳大利亚; merryn.netting@adelaide.edu.au 8儿科学学科,阿德莱德大学,阿德莱大学,阿德莱德大学,SA 5006,澳大利亚9号妇女和儿童医院,阿德莱德,澳大利亚10号阿德莱德,澳大利亚10号,澳大利亚10号,妇产科,墨尔本大学,墨尔本大学,澳大利亚墨尔本大学,澳大利亚,澳大利亚3010年,澳大利亚,5000年,澳大利亚,澳大利亚,澳大利亚,澳大利亚3010年,5000年,统计,西澳大利亚大学,珀斯,华盛顿州6009,澳大利亚; Alethea.rea@murdoch.edu.au(A.R. ); michelle.trevenen@uwa.edu.au(M.L.T。)4 UWA人类哺乳研究与翻译中心,珀斯,华盛顿州6009,澳大利亚5分子科学学院,西澳大利亚大学,珀斯,华盛顿州珀斯,澳大利亚6009; Mary.wlodek@uwa.edu.au或m.wlodek@unimelb.edu.au 6农业,食品和葡萄酒学校,阿德莱德大学,阿德莱德大学,阿德莱德,澳大利亚5064,澳大利亚; gabriela.leghivoyer@gmail.com(g.e.l。); beverly.muhlhausler@adelaide.edu.au或bev.muhlhausler@csiro.au(b.s.m.)7妇女和儿童主题,南澳大利亚健康与医学研究所(SAHMRI),阿德莱德,SA 5000,澳大利亚; merryn.netting@adelaide.edu.au 8儿科学学科,阿德莱德大学,阿德莱大学,阿德莱德大学,SA 5006,澳大利亚9号妇女和儿童医院,阿德莱德,澳大利亚10号阿德莱德,澳大利亚10号,澳大利亚10号,妇产科,墨尔本大学,墨尔本大学,澳大利亚墨尔本大学,澳大利亚,澳大利亚3010年,澳大利亚,5000年,澳大利亚,澳大利亚,澳大利亚,澳大利亚3010年,5000年,统计,西澳大利亚大学,珀斯,华盛顿州6009,澳大利亚; Alethea.rea@murdoch.edu.au(A.R.); michelle.trevenen@uwa.edu.au(M.L.T。)13数学和统计,默多克大学,默多克,华盛顿州6150,澳大利亚 *通信:matthew.payne@uwa.edu.au.au†在澳大利亚母乳喂养 +哺乳研究与科学翻译会议上发表(澳大利亚和哺乳动物会议,2023年),澳大利亚,澳大利亚,11月2023日。
NCI-MATCH 试验中,克唑替尼用于治疗具有 ALK 或 ROS1 重排的肿瘤患者。
NCI-MATCH 旨在表征靶向疗法对组织学不可知的驱动突变阳性恶性肿瘤的疗效。子方案 F 和 G 旨在评估克唑替尼在具有 ALK 或 ROS1 重排的罕见肿瘤中的作用。在至少接受过一次全身治疗后病情进展的恶性肿瘤患者被纳入 NCI-MATCH 进行分子分析,而具有可操作的 ALK 或 ROS1 重排的患者分别被邀请参与子方案 F 或 G。有五名患者进入 F 组(ALK),四名患者进入 G 组(ROS1)。观察到少数 3 级或 4 级毒性,包括肝功能异常和急性肾损伤。对于子方案 F(ALK),反应率为 50%(90% CI 9.8 – 90.2%),4 名符合条件的患者中有 1 名完全反应。中位 PFS 为 3.8 个月,中位 OS 为 4.3 个月。对于子方案 G(ROS1),响应率为 25%(90% CI 1.3 – 75.1%)。中位 PFS 为 4.3 个月,中位 OS 为 6.2 个月。来自 3 家商业供应商的数据显示,ALK 和 ROS1 重排在非小细胞肺癌和淋巴瘤以外的组织学中的患病率很低(分别为 0.1% 和 0.4%)。我们观察到对克唑替尼的反应符合 ALK 融合的主要终点,尽管患者数量很少。尽管累积人数有限,但一些具有这些致癌融合的患者可以对克唑替尼产生反应,这可能在这种情况下发挥治疗作用。