机构名称:
¥ 1.0
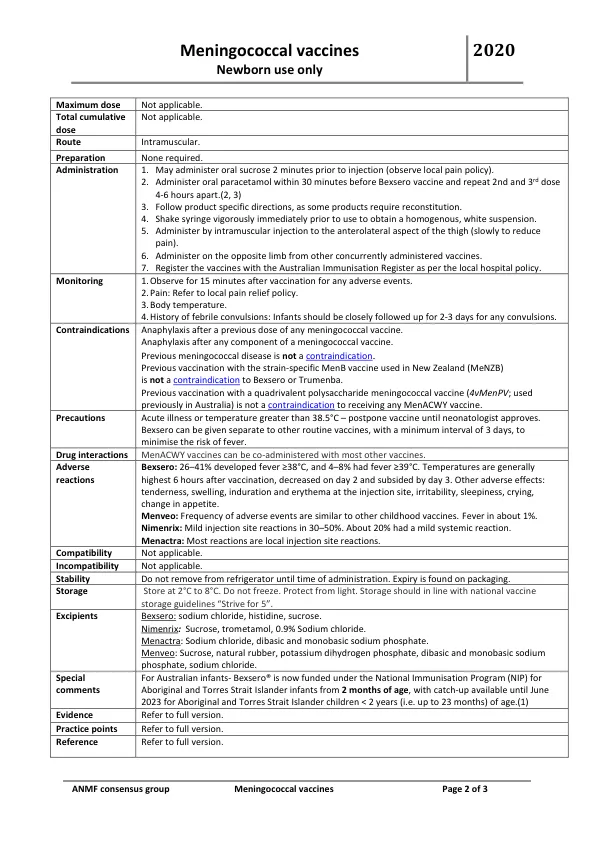
Bexsero:26–41% 出现发热≥38°C,4–8% 发热≥39°C。体温通常在接种疫苗后 6 小时达到最高,第 2 天下降,第 3 天消退。其他不良反应:注射部位压痛、肿胀、硬结和红斑、烦躁、嗜睡、哭闹、食欲改变。 Menveo:不良事件发生频率与其他儿童疫苗相似。约 1% 出现发热。 Nimenrix:30–50% 出现轻微注射部位反应。约 20% 出现轻微全身反应。 Menactra:大多数反应是局部注射部位反应。 兼容性 不适用。 不兼容性 不适用。 稳定性 在注射前请勿从冰箱中取出。有效期见包装。 储存 储存在 2°C 至 8°C 的环境中。请勿冷冻。避光。储存应符合国家疫苗储存指南“争取 5 年”。辅料 Bexsero:氯化钠、组氨酸、蔗糖。 Nimenrix:蔗糖、氨丁三醇、0.9%氯化钠。 Menactra:氯化钠、磷酸氢二钠和磷酸二氢钠。 Menveo:蔗糖、天然橡胶、磷酸二氢钾、磷酸氢二钠和磷酸二氢钠、氯化钠。 特别说明
脑膜炎球菌疫苗 2020
主要关键词