XiaoMi-AI文件搜索系统
World File Search System医疗专业人士生物仿制药指南
• 在开具、分发或管理生物仿制药时,为其决策过程提供信息和帮助。 • 阐明“参考生物药物”和“生物仿制药”之间的区别、生物仿制药获得上市许可(监管部门批准)的要求以及如何考虑到这些药物的特殊性。 • 解决阿联酋市场中与生物仿制药药物警戒有关的问题。 • 定义不同医疗保健专业人员的角色和职责、实施范围、患者教育以及对任何药物不良反应的建议监测和评估。
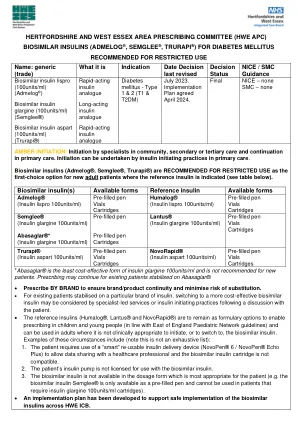
生物仿制药胰岛素(Ambelog semglee和trurapi)
预填充的笔小瓶墨盒 *abasaglar®是胰岛素glargine 100units/ml的成本效益最低的形式,不建议新患者使用。在Abasaglar®上稳定的现有患者可能会继续开处方。•通过品牌开出来,以确保品牌/产品连续性并最大程度地降低替代风险。•对于在特定品牌的胰岛素上稳定的现有患者,可以在与患者讨论后,可以考虑使用专业主导的服务或胰岛素启动实践来考虑更具成本效益的生物仿制药胰岛素。•参考胰岛素(Humalog®,Lantus®和Novorapid®)将保留作为配方式选择,以便在儿童和年轻人(与英格兰东部儿科网络指南一致)中处方,并且可以在成年人中使用,在成年人中不适合临床起初,或者可以启动,或者可以转移到生物含量的胰岛素。这些情况的示例包括(注意这不是详尽的列表):1。患者需要使用“智能”可重复使用的胰岛素输送设备(Novopen®6 /novopen®回声< / div < / div>
阿达木单抗生物仿制药追踪
Humira 和生物仿制药 WAC 来源于 Micromedex Redbook *低成本生物仿制药 WAC 平均值包括无品牌的 Hyrimoz、Yusimry 和 Hadlima;高成本是 Amjevita 5% 和 50% WAC 折扣 NDC 的加权平均值 **估计净成本考虑了 340B 的潜在折扣、患者援助和 SP 费用,来源于 IQVIA NSP 销售数据和制造商财务报表 来源:美国市场准入战略咨询分析;
Zydus 推出 IBYRA——Olaparib 的仿制药——...
Zydus Lifesciences Limited 是一家创新型全球生命科学公司,致力于发现、开发、制造和销售各种医疗疗法,其首要目标是让人们自由地过上更健康、更充实的生活。该集团在癌症相关疗法方面占有重要地位,并提供包括细胞毒性、支持性和靶向药物在内的各种解决方案。该集团在全球拥有 26,000 多名员工,其中包括 1,400 名从事研发的科学家,其使命是通过影响生命的优质医疗解决方案,在生命科学领域开启新的可能性。该集团渴望通过开创性的发现改变生活。如需了解更多详情,请访问 www.zyduslife.com 并在 LinkedIn 和 Twitter 上关注该公司。
Medicare Part中的仿制药利用和支出...
•医疗保险D部分的仿制药有110亿份处方,占近20亿比斯的同等处方,57亿美元的患者自付费用(OOP费用)和329亿美元的总药品成本。•如果仿制药的所有填充物的供应量为30天,总OOP将为16亿美元 - 减少了41亿美元或约71%。•在5310万Medicare D部分(82%)中,有4330万,至少填充了一种仿制药处方。其中2860万(54%)至少有一个通用填充,OOP的成本大于2美元。将近650万名(超过12%)至少有一个通用填充,OOP大于20美元。•总共有70.5%的30天当量填充售价为2美元或以下。•即使是最常用的通用药物,成本分布也存在很大差异。尽管普通高胆固醇治疗的平均OOP支出Atorvastatin不到2美元,而30天同等处方处方的近30%的参与者成本超过2美元。•在医疗保险参与者(Medicare bisulfate,Gabapentin,Gabapentin,Pantoprozole钠,Metoprolol琥珀酸酯和Omeprazole)中,最常用的20种仿制药中有五种药物的40天同等处方中的40%以上,其OOP的价格大于2美元。•在20种最常用的药物中,有9种平均OOP大于2美元。•低收入补贴(LIS)和非LIS参与者的通用分配率相似,但LIS参与者的仿制药(0.59美元)的支付费用要比平均非LIS参与者($ 4.00)的OOP少得多。•与独立D部分计划(PDPS)(82.7%)或
模型集成证据(MIE)行业会议仿制药试验计划:简介
•以创新性具有创新性并且没有资格且无法在现有的ANDA和ANDA科学会议计划下充分解决与单个产品或多个产品有关的复杂问题(例如,验证验证与单个产品或多个产品的常见策略)的复杂问题(CFD)模型/平台相对于ofos ofos osidos osidos ofoseos osids osids osid osids osid osids,•无法有资格或无法充分解决与单个产品或多个产品相关的复杂问题,以解决与单个产品或多个产品相关的复杂问题。 •具有复杂建模方法的非复合产品,支持基于BCS的生物效果和其他研究豁免,这些豁免是当前建议的。 •新型数据分析工具,例如建模方法的发展或建模方法的新应用,例如,复杂粒度分布(PSD)的等效分析,用于相同性评估的新定量方法以及新型数据分析方法(例如机器学习方法论)进行等效评估。•无法有资格或无法充分解决与单个产品或多个产品相关的复杂问题,以解决与单个产品或多个产品相关的复杂问题。•具有复杂建模方法的非复合产品,支持基于BCS的生物效果和其他研究豁免,这些豁免是当前建议的。•新型数据分析工具,例如建模方法的发展或建模方法的新应用,例如,复杂粒度分布(PSD)的等效分析,用于相同性评估的新定量方法以及新型数据分析方法(例如机器学习方法论)进行等效评估。
原创研究 消费者风险规避下,药品供应链中仿制药的区块链应用:博弈论模型
背景:区块链有望减轻药品供应链中消费者对仿制药的风险规避和质量不确定性。本研究调查了区块链采用对披露市场上与原药竞争的仿制药质量信息的影响,并提出了相应的法律措施。方法:我们采用博弈论模型分析包括仿制药制造商、原药制造商和零售商的药品供应链。我们研究供应链成员何时应采用区块链来处理仿制药以及区块链如何影响药品供应链。结果:我们的结果表明,仿制药的质量信息决定了区块链采用如何影响仿制药和原药的价格和销售数量。此外,我们观察到,只有当消费者的风险规避程度足够低时,仿制药制造商和零售商才会决定采用区块链。此外,较低的风险规避程度可以通过采用区块链提高整个供应链的盈利能力,并为消费者、仿制药制造商和零售商创造采用区块链的三赢局面。结论:为了减轻消费者的风险规避,法律应该维护消费者权益。区块链的应用在一定条件下可以惠及药品供应链和消费者,但也需要供应链成员利益的协调和质量信息的公开。关键词:仿制药,药品供应链,风险规避,质量不确定性,区块链应用
传染病仿制预防疫苗产品开发计划
1 在大多数 I 期疫苗试验中,受试者通常是健康的成年受试者。由于主要目标是证明安全性,因此疫苗的有效性通常不会得到证明。但是,作为次要或探索性参数的一部分,常见终点可能包括血清抗体滴度、血清 IgG、中和抗体滴度和一些细胞免疫反应。 2 必须决定是否在美国或其他地方进行 I 期临床试验。如果 I 期临床试验在美国进行,则必须遵守 FDA 规定。如果在其他地方(例如欧洲)进行,则必须遵守欧洲的规定。这可能会影响疫苗的生产和发布方式。美国和其他国家的监管要求在非临床数据包、临床试验执行、GLP 毒理学要求方面可能不相同。请务必咨询适当的监管专家或顾问。 3 如果提出多种给药途径,必须有非临床数据证明拟议给药途径的实用性。TPP 并非旨在涵盖所有可能性,而是一个有证据支持的概况。