XiaoMi-AI文件搜索系统
World File Search System反义寡核苷酸
核酸有两种形式:脱氧核糖核酸 (DNA) 和核糖核酸 (RNA)。RNA 的结构多种多样,可分为信使 RNA(mRNA,编码蛋白质)、非编码 RNA、转移 RNA (tRNA)、核糖体 RNA (rRNA) 和长链非编码 RNA (lncRNA) – DNA 是一种更稳定的分子 [1]。DNA 中的遗传信息编码为 RNA,即转录,然后翻译成蛋白质。由于蛋白质的作用机制和化学特性,大多数现有药物(如小分子和抗体)主要针对蛋白质。近年来,可结合信使 RNA (mRNA) 的化合物的使用引起了越来越多的兴趣,因为抑制蛋白质表达有助于控制炎症和肿瘤疾病的病程。该领域的两种主要治疗方法是抑制 mRNA 翻译的反义寡核苷酸 (ASO) 和通过 RNA 干扰 (RNAi) 途径发挥作用的寡核苷酸 [2]。
寡核苷酸药物分子
如果所讨论的蛋白质对于病毒的复制或癌细胞的不受控制的生长很重要,则可以观察到治疗作用。从理论上讲,反义寡核苷酸也可用于阻断正常细胞中蛋白质的合成,以便可以确定特定蛋白质的生物学作用。但是,在此应用程序中,最近开发的RNAi方法更受欢迎。RNA:反义寡核苷酸和靶mRNA之间形成的DNA混合双链体直接干扰蛋白质合成,从而降低了编码蛋白的表达。这种抑制作用可能是由于核糖体与反义寡核苷酸结合和/或杂化无法通过核糖体和直接蛋白质表达的核糖体周围组装的抑制作用。核糖核酸酶H(RNase H)对与反义寡核苷酸杂交的mRNA分子的核酸酶H(RNase H)的内核酸酶活性增强了反义作用。rNase h破坏了mRNA链,RNase H酶和反义寡核苷酸在循环结束时保持完整:因此,反义效应是催化的(图1)。单个反义寡核苷酸可以通过该机制销毁许多mRNA分子。酶RNase H发生在正常细胞中,在正常细胞中,它在去除DNA复制滞后的短链中起着重要作用。
利用寡核苷酸机会
寡核苷酸疗法彻底改变了制药行业的格局。它们是一类由短链 RNA 或 DNA 组成的药物,可以通过合成操纵来改变多种致病蛋白的表达。直到最近,市场上大多数经美国食品药品监督管理局 (FDA) 批准的寡核苷酸都用于治疗罕见疾病。然而,用于治疗心血管疾病的 inclisiran 于 2021 年获得批准,现在凸显了它们治疗多种常见临床适应症的潜力。Inclisiran 展示了寡核苷酸带来的机遇,它是一种针对大量患者群体的治疗方式,针对多种常见疾病,包括心血管疾病、肿瘤学和代谢紊乱。然而,必须承认,当前的寡核苷酸供应链是不可持续的,在扩大规模方面面临重大障碍,凸显了需要解决的关键供需缺口。
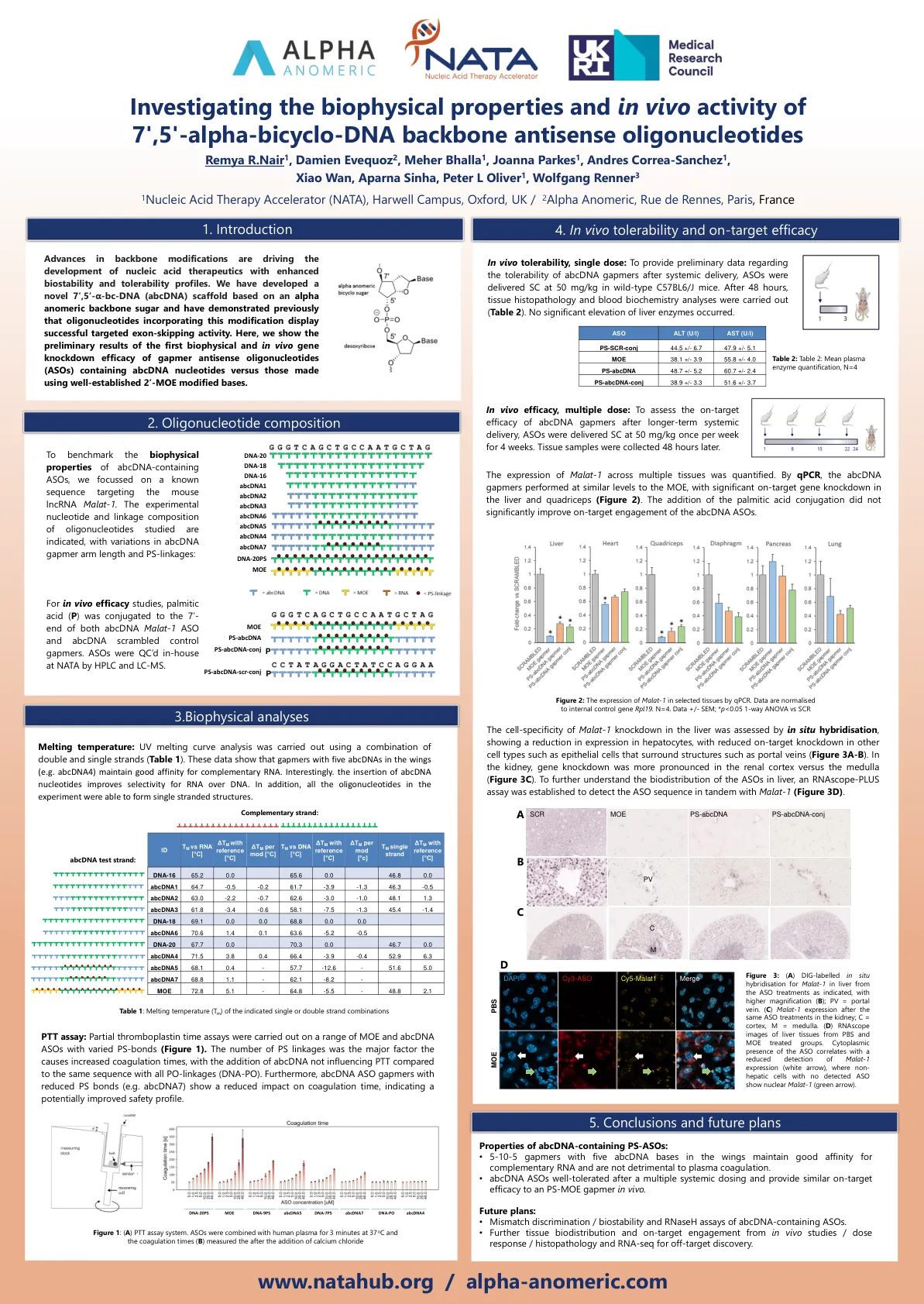
alpha-bicyclo-DNA骨架反义寡核苷酸
主链修饰的进步正在推动具有增强的生物稳定性和耐受性谱的核酸治疗剂的发展。我们已经开发了一种基于α异源主链糖的新型7',5'-α-BC-DNA(ABCDNA)支架,并先前证明了寡核苷酸含有这种修饰的寡核苷酸,该修饰显示了成功的靶向外显子鞋鞋。在这里,我们显示了含有AbcDNA核苷酸的Gapmer反义寡核苷酸(ASOS)的第一个生物物理和体内基因敲低功效的初步结果,而不是使用完善的2'MoE修饰碱基。
分析寡核苷酸合成的原料
作为生物制药生产过程的第一步,必须对最佳质量产品进行彻底分析任何合成的原材料。在寡核苷酸的情况下,这些原材料称为核苷磷光矿,并在随后的DNA合成中充当构件。在本应用注释中,我们基于生物相容性的Agilent 1290 Infinity II Bio Lc开发了LC方法。通过将LC与Agilent 6545xt AdvanceBio LC/Q-TOF耦合,可以通过准确的质量来识别几种杂质,并且方法开发可以通过四通道敏捷1290 Infinity II II II Bio Flexible柔性泵来轻松进行,这表现出极好的保留时间和面积精度。基于此,进行了其他方法开发,以将LC运行时间减少66%,保留了出色的性能,并进行了方法兼容性实验,显示了从常规的Agilent 1290 Infinity II LC中的无缝方法转移。总的来说,这些结果表明,1290个Infinity II Bio LC是对寡核苷酸合成原材料的强大和多功能分析的理想选择。
寡核苷酸疗法含有肽核酸...
在第1、3、5、5、8、15、22和29天,在3.75、15、37.5和60 mg/kg/剂量下皮下施用APT-110。在给药上治疗剂量后立即观察到血小板和补体途径的短暂激活。肾脏和肝组织学改变也被发现。
定制寡核苷酸修饰指南
寡核苷酸通过反相高效液相色谱法 (RP-HPLC) 纯化。根据客户要求,也可提供脱盐寡核苷酸(未经 HPLC 纯化)。除非另有说明,所有寡核苷酸均为冻干。根据客户要求,也可订购浓缩溶液形式的寡核苷酸。
主题 1:基于 RNA 和寡核苷酸的治疗
Knud Jørgen Jensen,哥本哈根大学化学系 简要说明:寡核苷酸药物正成为治疗癌症、肌肉和神经系统疾病以及疫苗生产的绝佳工具。限制其应用的一个主要问题是,虽然我们有很好的工具将它们输送到细胞中,但只有约 5% 的物质能够释放到细胞中,其余的仍被困在内体中。优化寡核苷酸逃逸和疾病控制中心的范围首先是了解寡核苷酸内体逃逸的机制,其次是利用这些信息增加输送,从而治疗心血管和代谢疾病。我们将使用先进的显微镜测量它们与活细胞的相互作用,使用 AI 工具分析数据并设计和合成更好的逃离内体的 DNA 和 RNA 药物。该中心将成为哥本哈根大学、哈佛医学院和波士顿儿童医院以及里斯本大学分子医学研究所之间的桥梁。