XiaoMi-AI文件搜索系统
World File Search System出显子7/外显子8缺失的患病率和脊柱肌肉萎缩症患者
脊柱肌肉萎缩(SMA)是由于脊髓前角细胞的变性而导致的神经肌肉疾病。SMA的估计发病率为1:6,000-1:10,000。SMN1基因的外显子7的完全缺失是大多数人群中95-98%的SMA患者的标志。对涉嫌患有SMA的儿童或年轻患者的第一条调查应为多重结扎依赖性探针扩增(MLPA)测试,用于对外显子7和SMN1基因中的外显子7和外显子8的纯合缺失。在本文中,我们报告了参加喀拉拉邦一家三级护理医院遗传诊所的SMN 1外显子7缺失测试的结果,其中有一个或多个症状,尤其是软盘婴儿,性低下,肌肉虚弱,舌头,舌头障碍等。SMN1外显子7和外显子8缺失在总计33例低调患者的58%(19)中得到了证实。在SMA阳性病例中,SMA I型,II型和III型分别为68.4%(13),21%(4)和10.5%(2)。对非语言父母的载体测试表明,所有父母都是杂合携带者。直到2016年,这种疾病的治疗仅是支持的。最近Nusinersen,Zolgensma和Risdiplam已适用于SMA患者。先前有SMA儿童历史的父母的携带者测试对于在未来怀孕中实施这种疾病的产前诊断至关重要。本文强调了这种罕见的神经肌肉疾病的重要性。
神经丝蛋白作为脊柱肌肉萎缩的生物标志物:综述和参考范围
SMA中的神经变性阻碍了有效的疾病管理。 神经丝纤维蛋白(NFL)是SMA中神经司长损伤的促进生物标志物,并反映了接受治疗的SMA儿童的疾病进展。 最近,欧洲药品局发表了一份支持信,以认可NFL作为儿童神经疾病(包括SMA)的生物标志物的潜在利用。 在这篇综述中,我们全面评估了NFL作为儿科发作SMA疾病严重程度和治疗反应的监测生物标志物的潜在应用。 我们为0 - 18岁的神经健康儿童提供了正常水平的基于血清NFL的参考范围。 这些参考范围可以准确地描述儿童中NFL水平的相互作用,并可以加速NFL进入临床实践。SMA中的神经变性阻碍了有效的疾病管理。神经丝纤维蛋白(NFL)是SMA中神经司长损伤的促进生物标志物,并反映了接受治疗的SMA儿童的疾病进展。最近,欧洲药品局发表了一份支持信,以认可NFL作为儿童神经疾病(包括SMA)的生物标志物的潜在利用。在这篇综述中,我们全面评估了NFL作为儿科发作SMA疾病严重程度和治疗反应的监测生物标志物的潜在应用。我们为0 - 18岁的神经健康儿童提供了正常水平的基于血清NFL的参考范围。这些参考范围可以准确地描述儿童中NFL水平的相互作用,并可以加速NFL进入临床实践。
2024最新信息:欧洲关于脊柱肌肉萎缩基因治疗的共识声明
神经医学和肌肉障碍系,医学中心 - 弗雷堡大学,弗雷堡大学,弗雷堡,德国B神经肌肉中心,儿科和青少年医学系,维也纳,维也纳,奥地利C clinic favoriten
线粒体靶向药物 MitoQ 改善 C26 肿瘤小鼠的肌肉萎缩、虚弱和氧化代谢
癌症恶病质是一种衰弱综合征,其特征是骨骼肌萎缩、虚弱和疲劳。多种致病机制可导致这些肌肉紊乱。已知线粒体变异、代谢改变和氧化应激增加会促进肌肉无力和肌肉分解代谢。为了改善恶病质,已测试了几种药物来刺激线粒体功能并使氧化还原平衡正常化。本研究的目的是测试 Mitoquinone Q (MitoQ) 的潜在有益抗恶病质作用,MitoQ 是最广泛使用的靶向线粒体的抗氧化剂之一。我们在这里表明,体内施用 MitoQ(每日 25 mg/kg 饮用水)能够改善 Colon-26 (C26) 携带者的体重减轻,而不会影响肿瘤大小。使用 MitoQ 治疗后,C26 宿主的骨骼肌和强度持续改善。与骨骼肌质量的改善相一致,MitoQ 治疗能够部分纠正 E3 泛素连接酶 Atrogin-1 和 Murf1 的表达。相反,合成代谢信号并没有因治疗而改善,这表现为 AKT、mTOR 和 4EBP1 磷酸化没有变化。基因表达评估显示,肿瘤宿主的线粒体生物合成和体内平衡标志物的水平发生了改变,尽管只有 Mitofusin-2 水平受到治疗的显著影响。有趣的是,参与调节线粒体功能和代谢的基因 Pdk4 和 CytB 的水平也因 MitoQ 而部分增加,这与己糖激酶 (HK)、丙酮酸脱氢酶 (PDH) 和琥珀酸脱氢酶 (SDH) 酶活性的调节一致。尽管肌肉 LDL 受体表达没有变化,但接受 MitoQ 治疗的 C26 携带者的氧化代谢改善与肌骨变性(即肌内脂肪滤过)减少有关,因此表明 MitoQ 可以促进肌肉组织中的 β 氧化,并促进肌肉代谢和纤维组成从糖酵解向氧化的转变。总体而言,我们的数据表明 MitoQ 是一种有效的治疗方法,可改善肿瘤宿主的骨骼肌质量和功能,并进一步支持旨在测试靶向线粒体的抗氧化剂与常规化疗药物联合使用的抗恶病质特性的研究。
诊断基因组,外显子组和小组测序数据集的脊柱肌肉萎缩病的丢失病例
在基因组,外部和小组测序数据集中诊断出遗漏的脊柱肌肉萎缩病例本·韦斯堡(Ben Weisburd),1,2,* Rakshya Sharma,1,3 Villem Pata,4,5 Tiia Reimand,4,6 Vijay S. Ganesh,1,2,7,7,7,7,8 Christina Austin-Austin-tsei-emiDe,1,8 emiyl emwa suow om emolow om emrouwa os。 O'Heir, 1,8 Melanie O'Leary, 1 Lynn Pais, 1,8 Seth A. Stafki, 9 Audrey L. Daugherty, 9 Chiara Folland, 26 Stojan Peri ć , 10,11 Nagia Fahmy, 12 Bjarne Udd, 13 Magda Horakova, 14,15 Anna Łusakowska, 16 Rajanna Manoj, 17 Atchayaram Nalini, 17 Veronika Karcagi, 18 Kiran Polavarapu, 19 Hanns Lochmüller, 19,20,21 Rita Horvath, 22 Carsten G. Bönnemann, 23 Sandra Donkervoort, 23 Göknur Halilo ğ lu, 23,24 , Ozlem Herguner, 25 Peter B. Kang, 9 Gianina Ravenscroft,26,27 Nigel Laing,26,27 Hamish S.Scott,28AnaTöpf,29 Volker Straub,29 Sander Pajusalu,4,6 Katrin rinap,4,6 Grace Tiao,1 Heidi L. Rehm,1,2 Anne O'Donnell-Lurururiia-Lururiaia Lururiaia 1,2,8,* * <
医学药物临床标准
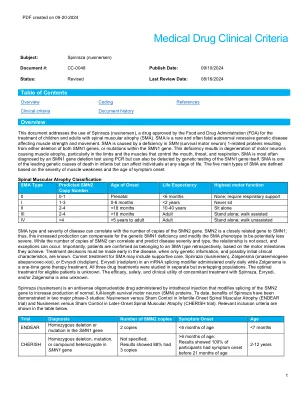
概述本文档介绍了Spinraza(Nusinersen)的使用,Spinraza(nusinersen)是一种由食品药品监督管理局(FDA)批准的药物,用于治疗患有脊柱肌肉萎缩(SMA)的儿童和成人。SMA是一种影响肌肉力量和运动的罕见且经常致命的常染色体隐性遗传疾病。SMA是由SMN(生存运动神经元)1相关蛋白缺乏引起的,这是由两个SMN1基因缺失或SMN1基因内的突变引起的。这种缺乏会导致运动神经元的退化,导致肌肉萎缩,尤其是在控制口,喉咙和呼吸的四肢和肌肉中。SMA通常是通过使用PCR进行的SMN1基因缺失测试来诊断的,但也可以通过对SMN1基因本身的基因检测来检测。SMA是婴儿死亡的主要遗传原因之一,但在生命的任何阶段都会影响个体。SMA的五种主要类型是根据肌肉无力的严重程度和症状发作时代定义的。脊柱肌肉萎缩分类
医学药物临床标准
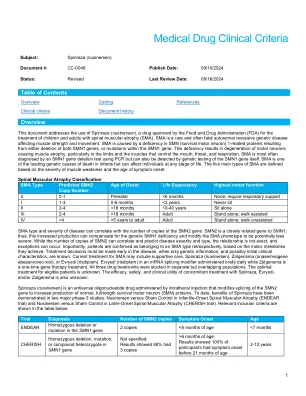
概述本文档介绍了Spinraza(Nusinersen)的使用,Spinraza(nusinersen)是一种由食品药品监督管理局(FDA)批准的药物,用于治疗患有脊柱肌肉萎缩(SMA)的儿童和成人。SMA是一种影响肌肉力量和运动的罕见且经常致命的常染色体隐性遗传疾病。SMA是由SMN(生存运动神经元)1相关蛋白缺乏引起的,这是由两个SMN1基因缺失或SMN1基因内的突变引起的。这种缺乏会导致运动神经元的退化,导致肌肉萎缩,尤其是在控制口,喉咙和呼吸的四肢和肌肉中。SMA通常是通过使用PCR进行的SMN1基因缺失测试来诊断的,但也可以通过对SMN1基因本身的基因检测来检测。SMA是婴儿死亡的主要遗传原因之一,但在生命的任何阶段都会影响个体。SMA的五种主要类型是根据肌肉无力的严重程度和症状发作时代定义的。脊柱肌肉萎缩分类
议程
11:30 - 11:40 AM治疗对III型脊柱肌肉萎缩的移动损失的影响:意大利ISMAC注册中心Giorgia Coratti,TNPEE,MSC,Ph.D。的见解。天主教大学的神圣心脏fondazione Policlinico commitorio agostino gemelli irccs11:30 - 11:40 AM治疗对III型脊柱肌肉萎缩的移动损失的影响:意大利ISMAC注册中心Giorgia Coratti,TNPEE,MSC,Ph.D。的见解。天主教大学的神圣心脏fondazione Policlinico commitorio agostino gemelli irccs
1 Musclesense -UCL Discovery
1 Deenen,J。C. W.等。神经肌肉疾病的流行病学:文献的全面概述。J. Neuromuscul。dis。2,73–85(2015)。 2 Finkel,R。S.等。 Nusinersen与婴儿性脊柱肌肉萎缩中的假手术对照。 N. Engl。 J. Med。 377,1723–1732(2017)。 3 Mendell,J。R.等。 单剂量基因替代疗法用于脊柱肌肉萎缩。 N. Engl。 J. Med。 377,1713–1722(2017)。 4 Voit,T。等。 Drisapersen对Duchenne肌肉营养不良的治疗的安全性和功效(需求II):探索性,随机,安慰剂对照的2期研究。 柳叶刀神经。 13,987–996(2014)。 5临床trials.gov。 可用:https://clinicaltrials.gov/。 (访问:2019年9月7日)2,73–85(2015)。2 Finkel,R。S.等。Nusinersen与婴儿性脊柱肌肉萎缩中的假手术对照。N. Engl。J. Med。 377,1723–1732(2017)。 3 Mendell,J。R.等。 单剂量基因替代疗法用于脊柱肌肉萎缩。 N. Engl。 J. Med。 377,1713–1722(2017)。 4 Voit,T。等。 Drisapersen对Duchenne肌肉营养不良的治疗的安全性和功效(需求II):探索性,随机,安慰剂对照的2期研究。 柳叶刀神经。 13,987–996(2014)。 5临床trials.gov。 可用:https://clinicaltrials.gov/。 (访问:2019年9月7日)J. Med。377,1723–1732(2017)。3 Mendell,J。R.等。 单剂量基因替代疗法用于脊柱肌肉萎缩。 N. Engl。 J. Med。 377,1713–1722(2017)。 4 Voit,T。等。 Drisapersen对Duchenne肌肉营养不良的治疗的安全性和功效(需求II):探索性,随机,安慰剂对照的2期研究。 柳叶刀神经。 13,987–996(2014)。 5临床trials.gov。 可用:https://clinicaltrials.gov/。 (访问:2019年9月7日)3 Mendell,J。R.等。单剂量基因替代疗法用于脊柱肌肉萎缩。N. Engl。J. Med。 377,1713–1722(2017)。 4 Voit,T。等。 Drisapersen对Duchenne肌肉营养不良的治疗的安全性和功效(需求II):探索性,随机,安慰剂对照的2期研究。 柳叶刀神经。 13,987–996(2014)。 5临床trials.gov。 可用:https://clinicaltrials.gov/。 (访问:2019年9月7日)J. Med。377,1713–1722(2017)。4 Voit,T。等。Drisapersen对Duchenne肌肉营养不良的治疗的安全性和功效(需求II):探索性,随机,安慰剂对照的2期研究。柳叶刀神经。13,987–996(2014)。 5临床trials.gov。 可用:https://clinicaltrials.gov/。 (访问:2019年9月7日)13,987–996(2014)。5临床trials.gov。可用:https://clinicaltrials.gov/。(访问:2019年9月7日)