XiaoMi-AI文件搜索系统
World File Search System脊柱肌肉萎缩(SMA)
什么是新生儿筛查?这些是出生后不久进行的常规测试。从婴儿的脚后跟抽取几滴血液,并放在一张吸收纸上(墨水)。血液已针对罕见的可治疗条件进行测试。进行这些测试是因为新生儿看起来很健康,但是有一种疾病,需要治疗。我们想找到患有这些疾病的婴儿,以便我们可以开始治疗以保持尽可能健康。如何报告阳性的新生儿屏幕结果?海上新生儿筛查的医疗保健提供者将与初级保健提供者和家人联系以讨论结果。他们将将婴儿连接到提供后续行动的临床团队。医疗保健提供者和/或临床团队将安排后续约会并尽快进行测试。家庭可能会担心婴儿的新生儿屏幕结果。在这种情况下,许多家庭感到这种感觉。医疗团队在下一步中为家庭提供支持。如果婴儿对脊柱肌肉萎缩(SMA)有阳性结果是什么意思?此结果意味着婴儿可能有一种SMA。需要进一步测试以确认SMA的诊断。什么是SMA?SMA是一种遗传神经肌肉疾病,这意味着婴儿天生就有它。SMA会影响运动神经元,该神经元是控制我们肌肉和运动的神经元。在SMA中,运动神经元会随着时间的流逝而丢失,这会导致肌肉减弱。SMA有四种主要类型。类型是根据症状开始的年龄和最先进的运动里程碑(例如,坐着,步行)的分类。类型1是四种类型中最严重的,也是最常见的。具有1型SMA症状通常出现在生命的前几周或几个月中,通常婴儿无法控制头部运动或无辅助。也可能存在吞咽困难和呼吸问题,如果没有治疗大多数1型SMA的婴儿,就不会生活超过两岁。SMA 2型和3型不那么普遍,在6个月后或生命的头几年后出现症状。患有SMA类型2或3的人可能无法站立或行走。4型SMA很少见,症状从成年开始。对患有严重SMA类型的婴儿有有效的治疗方法可以减慢或停止SMA的进展。有多少个婴儿有SMA?SMA是一种罕见的疾病,每10,000名婴儿中大约会影响1个。为什么要屏幕SMA?带有SMA的婴儿通常在出生时看起来正常,并且可能直到出生后几周或几个月才显示与SMA有关的任何健康问题。如果没有通过新生儿筛查对其进行筛选,则可能不会立即诊断出它们。有关于SMA的治疗方法,这些治疗方法在症状开始之前或不久后给予最有效的治疗方法。新生儿筛查使我们能够找到患有SMA的婴儿,因此他们可以尽快接受治疗。婴儿如何被诊断出患有SMA?要找出婴儿是否患有SMA,在IWK儿童康复诊所中的医生看到了它们,以评估他们的神经和肌肉。基因检测(血液调查)还有助于确认对SMA的诊断。家庭将与海上医学遗传学服务的遗传咨询师联系。可能需要几天的时间来确认婴儿患有SMA。这个等待期可能对家庭很难。在此期间,医疗团队在这里为家庭提供支持。如何治疗SMA?SMA接受针对SMA原因但不是治愈方法的特殊药物治疗。这些治疗方法是根据SMA的类型和遗传诊断提供的。IWK儿童康复诊所将与家人讨论治疗选择。两种批准的疗法是一种靶向疗法,称为Nusinersen(SpinRaza®)和一种称为Onasengenemogene Abeparvovec(Zolgensma®)的基因疗法。在SMA症状开始之前给予这些治疗方法最有效。
脊柱肌肉萎缩(SMA)
条件描述脊柱肌肉萎缩(SMA)是一种由生存运动神经1基因(SMN1)基因致病性变化引起的常染色体隐性神经退行性运动神经元。新生儿筛查(NBS)检测到SMN1中纯合缺失的患者,该患者约占病例的95%。SMA I型占一半以上的病例,并在出生后不久或出生后出生,呼吸和喂养困难。疾病的严重程度被相关基因SMN2的副本数量减弱。具有三个或更多副本的SMN2的个体,有后来的婴儿(SMA 2型),儿童期(SMA 3型)或成人发作SMA。通过NBS鉴定出具有两三个副本的SMN2的婴儿,在六周之前快速确认遗传诊断,评估和治疗起始,对于最佳结果至关重要。最严重的形式(SMA型0)与外显子7或整个基因中的较大缺失有关。
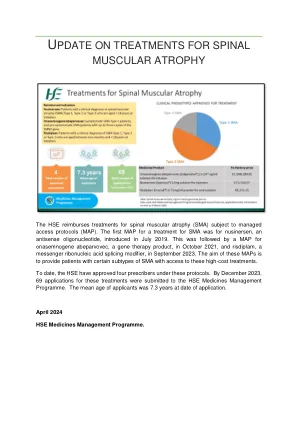
治疗脊柱肌肉萎缩的疗法
脊髓肌肉萎缩(SMA)是一种罕见的遗传神经肌肉疾病,最严重的病例影响了婴儿和幼儿。1,2 SMA发病率约为15,000分中的15,000分之一,在美国(美国)每年约有500例新的SMA病例。3 4 SMA的最常见原因是在5q染色体上的生存运动神经元1(SMN1)基因的等位基因的纯合缺失或缺失和突变。5-7 SMN1创建生存运动神经元(SMN)蛋白,这是一种对运动神经元发育必不可少的蛋白质。尽管生存运动神经元2(SMN2)基因也会产生SMN蛋白,但只有少量的蛋白质才能起作用。SMN2复制的数量调节了SMA的严重程度,但没有SMN1的患者的SMN蛋白水平不足,而不管SMN2拷贝的数量多少。8这种缺乏会导致运动神经元的不可逆变性,这导致肌肉无力,并防止患者达到运动里程碑或保持运动功能。1
脊柱肌肉萎缩 - 基因治疗 - Zolgensma
使用以下覆盖范围政策的说明适用于Cigna公司管理的健康福利计划。某些CIGNA公司和/或业务范围仅向客户提供利用审核服务,并且不做覆盖范围的确定。引用标准福利计划语言和覆盖范围确定不适用于这些客户。覆盖范围政策旨在为解释Cigna Companies管理的某些标准福利计划提供指导。请注意,客户的特定福利计划文件的条款[集团服务协议,覆盖范围证据,覆盖证证书,摘要计划描述(SPD)或类似计划文件]可能与这些承保范围政策所基于的标准福利计划有很大差异。例如,客户的福利计划文件可能包含与覆盖策略中涉及的主题相关的特定排除。发生冲突时,客户的福利计划文件始终取代覆盖策略中的信息。在没有控制联邦或州承保范围授权的情况下,福利最终取决于适用的福利计划文件的条款。在每个特定实例中的覆盖范围确定需要考虑1)根据服务日期生效的适用福利计划文件的条款; 2)任何适用的法律/法规; 3)任何相关的附带资料材料,包括覆盖范围政策; 4)特定情况的具体事实。应自行审查每个覆盖范围请求。使用医疗总监有望行使临床判断,并在做出个人覆盖范围确定方面有酌处权。覆盖范围政策与健康福利计划的管理仅有关。覆盖范围政策不是治疗的建议,绝不应用作治疗指南。在某些市场中,可以使用授权的供应商指南来支持医疗必要性和其他承保范围的确定。Cigna Healthcare覆盖范围政策o Verview Zolgensma是一种基于腺相关的病毒载体基因疗法,用于治疗生存运动神经元1(SMN1)基因的脊柱肌肉萎缩,在低于2岁的患者中。1使用的局限性是尚未评估重复给药的安全性和有效性。1尚未评估脊柱肌肉萎缩患者(例如,四肢完全麻痹,永久呼吸机依赖性)的使用。
脊柱肌肉萎缩医疗提供者
脊髓肌肉萎缩(SMA)是一种由生存运动神经元1(SMN1)基因致病性变化引起的常染色体隐性神经退行性运动神经元。新生儿筛查(NBS)旨在识别SMN1中纯合缺失的患者,该患者约为95%的病例。SMA在临床上是可变的,从出生到成年的发病年龄不等。SMA I型,也称为Werdnig-Hoffman病,占患有低调,呼吸和喂养困难后不久或出生后不久或出生后的一半以上。 大多数受影响的个体中存在舌头痴迷。 没有治疗,死亡通常发生在2岁之前。 疾病的严重程度被相关基因SMN2的副本数量减弱。 具有三个或更多副本的SMN2的个体,较晚的婴儿(SMA 2型),童年(SMA 3型)或成人发作(SMA IV)。 对于用两三个副本SMN2识别的婴儿,在6周龄之前的遗传诊断,评估和治疗起始的快速确认对于最佳结果至关重要。 最严重的形式(SMA型0)与外显子7或整个基因中的较大缺失有关。SMA I型,也称为Werdnig-Hoffman病,占患有低调,呼吸和喂养困难后不久或出生后不久或出生后的一半以上。大多数受影响的个体中存在舌头痴迷。没有治疗,死亡通常发生在2岁之前。疾病的严重程度被相关基因SMN2的副本数量减弱。具有三个或更多副本的SMN2的个体,较晚的婴儿(SMA 2型),童年(SMA 3型)或成人发作(SMA IV)。对于用两三个副本SMN2识别的婴儿,在6周龄之前的遗传诊断,评估和治疗起始的快速确认对于最佳结果至关重要。最严重的形式(SMA型0)与外显子7或整个基因中的较大缺失有关。
脊柱肌肉萎缩(SMA)ACT纸
瞄准者:本指南主要是为临床医生提供的教育资源,以帮助他们提供优质的医疗服务,不应将其包括在内的所有适当的程序和测试,或不包括其他程序和测试,这些程序和测试可合理地指导获得相同的结果。遵守本指南并不一定能确保成功的医疗结果。在确定任何特定程序或测试的适当性时,临床医生应将其自己的专业判断应用于个别患者或标本所呈现的特定临床情况。临床医生被鼓励记录使用特定程序或测试的原因,无论它是否符合本指南。还建议临床医生注意通过该指南的日期,并考虑在该日期之后可用的其他医学和科学信息。©美国医学遗传学学院,2009年(部分通过MCHB/HRSA/HHS授予#U22MC03957)