XiaoMi-AI文件搜索系统
World File Search SystemCrizotinib
劳拉替尼的最新进展
摘要:劳拉替尼是一种口服第三代间变性淋巴瘤激酶 (ALK) 抑制剂,对一线和后续治疗中晚期 ALK 阳性非小细胞肺癌 (NSCLC) 均有活性。3 期 CROWN 试验证明,对于未经治疗的晚期 ALK 阳性 NSCLC 患者,劳拉替尼的全身和颅内疗效优于第一代 ALK 酪氨酸激酶抑制剂 (TKI) 克唑替尼。在第一代和第二代 ALK TKI 治疗期间出现疾病进展后,劳拉替尼对单个和一些复合 ALK 耐药突变仍保留了抗肿瘤作用。目前,艾乐替尼、布格替尼、色瑞替尼、克唑替尼和劳拉替尼均已获批用于治疗晚期 ALK 阳性 NSCLC。但尚无直接比较劳拉替尼与第二代 ALK 抑制剂的头对头研究。本文旨在概述劳拉替尼的疗效和安全性,并讨论劳拉替尼在晚期 ALK 阳性 NSCLC 治疗方法中的地位。关键词:间变性淋巴瘤激酶,劳拉替尼,非小细胞肺癌
CAP 34 措施标题:生物标志物状态用于指导临床...
这一重要信息对于协调护理和有效利用资源至关重要。因此,了解 ROS1、ALK 和 EGFR 的突变状态对于晚期 NSCLC 的适当临床决策是必不可少的。如果在一线化疗之前或期间发现一种或多种这些重排,则应考虑替代疗法。1% 至 2% 的非小细胞肺癌会出现 ROS1 重排,并且可预测对一线治疗药物克唑替尼和色瑞替尼疗法的反应。反应率(包括完全反应)接近 70% (2-4)。对于 ALK1,除了识别可能对靶向疗法有反应的肿瘤外,了解 ALK 重排状态通常可预测对免疫疗法的反应较差。大约 5% 的肺腺癌具有涉及 ALK 基因的染色体重排,并与 ALK 蛋白过表达有关。患有此类肿瘤的患者对 ALK 酪氨酸激酶抑制剂(如克唑替尼)的治疗有反应 (2, 5)。最后,约 20% 的肺腺癌含有 EGFR 激活突变,这预示着对 EGFR 酪氨酸激酶抑制剂(如厄洛替尼)的治疗有反应 (2, 6-10)。
PRPC通过与C-MET相互作用在结直肠癌细胞中调节癌症干细胞的性质
复发,在癌症治疗中仍然是一个限制,这降低了CRC患者的存活率(3)。此外,癌细胞由异质种群组成,包括癌细胞作为具有自我更新能力的亚群。癌症的这些特征与肿瘤的发育和进展以及治疗衰竭有关(4,5)。因此,需要发现和开发新型疗法和分子靶标,对于开发有效的治疗策略,以防止治疗结直肠癌。酪氨酸 - 蛋白激酶Met(C-MET)是一种异源型跨膜酪氨酸激酶受体,被称为肝细胞生长因子受体(HGFR),并由MET原始癌基因编码。c-Met激活了多个信号转导途径,例如RAS GTPase(RAS),磷脂酰肌醇3-激酶(PI3K)和Notch信号通路,并通过它们调节了癌细胞的增殖,存活和运动性(6)。另外,在各种癌症中,C-MET的异常表达也有报道,例如CRC,非小肺癌,胃癌和乳腺癌(7-10)。此外,C-MET过表达与肿瘤的增殖,侵袭和血管生成有关(11,12)。crizotinib是一种针对多种受体酪氨酸激酶(RTK)的小分子抑制剂,例如C-MET,间变性淋巴瘤激酶(ALK)和ROS1受体(13)。此外,克佐替尼通过抑制下游效应子功能和诱导细胞凋亡,在非小细胞肺癌(NSCLC),结肠癌,胃癌和神经胶质瘤中显示抗癌作用(14)。此外,克里唑替尼对C-MET的抑制可以通过衰减下游信号通路和细胞周期停滞来提高CRC对放射疗法的敏感性(15)。细胞prion蛋白(PRP C)是一种在包括神经细胞在内的多种细胞类型中表达的糖基磷脂酰肌醇连接的细胞表面蛋白(16),并且与多种细胞功能有关,例如应激保护,增殖和细胞
ALK 阳性非小细胞肺癌
摘要 目的 一种可改善生存率和/或疾病进展的药物可以创造实际期权价值 (ROV),即通过延长生存期实现的未来创新带来的额外健康收益。ROV 可作为临床和付款人决策者的相关考虑因素。我们旨在估计一线 (1L) 艾乐替尼在间变性淋巴瘤激酶 (ALK) 阳性非小细胞肺癌 (NSCLC) 中的事前 ROV。方法 我们开发了一个马尔可夫模型来估计由于未来潜在的二线 (2L) 药物,1L 艾乐替尼与 1L 克唑替尼获得的生命年 (LY) 和质量调整生命年 (QALY)。转移概率来自 1L 艾乐替尼的 3 期试验和 2L 布格替尼的 2 期试验。我们确定了在阿来替尼一线获批时正在 ALK 阳性 NSCLC 中进行 2 期和 3 期试验的药物,并根据公开数据预测了这些药物上市的可能性和时间以及潜在疗效。结果考虑 ROV 后,阿来替尼的折扣增量 LY 和 QALY 分别增加了 12.9%(95% CR - 2.96%,34.82%;1.25 vs. 1.11)和 11.2%(95% CR - 2.14%,29.29%;1.03 vs. 0.92)。阿来替尼的增量 ROV 对未来药物的预计疗效、吸收水平和阿来替尼(与克唑替尼相比)无进展生存期的风险比很敏感。结论在预期创新水平高的治疗领域,事前 ROV 可能是一个重要的价值考虑因素。未来药物的潜在疗效和预计到达时使用阿来替尼的增量生存率是评估 ROV 的重要考虑因素。
卫生技术简报2023年2月
尽管针对NSCLC ROS1阳性突变进行了新的靶向疗法,但在先前治疗的酪氨酸激酶抑制剂(TKIS)的患者中,仍有越来越多的获得性抗性突变,例如一线Crizotinib治疗,尤其是一线性crizotinib治疗,尤其是左右突变。现有的TKI可以显示出对获得的突变的敏感性,并且可以限制治疗持续时间的毒性。仍然有高度未满足的医学需求,以开发出克服内在的抗药性,治疗脑转移和延长反应持续时间的新型疗法,并具有更宽容的总体安全性。2,4据信,重核的紧凑和刚性结构使其能够精确有效地结合激酶的ATP结合口袋,并有可能避免空间干扰,从而导致对较大的激酶抑制剂的抵抗力,尤其是溶解的-Front和Gatekeeper,尤其是Ros1 trk和Alk Kink kink kink kink kink kink kink kink kink kink kink kink kink kin and solvent-flockase抑制剂。2靶向ROS1的ATP结合位点并克服由不同突变产生的空间干扰的能力意味着重新支出对多种电阻机制的活性,包括转移,旁路途径和不同的突变。5如果获得许可,则重新对抗将为患有ROS1阳性突变的NSCLC患者提供额外的治疗选择。
补充信息
补充图 6 . 剂量反应曲线表征 CUTO-28 亲本、CUTO-28 对照 HDR 编辑和 CUTO-28 L2086F 突变细胞系对酪氨酸激酶抑制剂的敏感性。a. 在不同浓度的克唑替尼、恩曲替尼、他曲替尼、劳拉替尼、雷帕替尼、卡博替尼、美瑞替尼和吉特替尼下暴露 72 小时后,所示细胞系的细胞活力以载体处理细胞为标准。图中标明,平均值和 SEM 取自三个技术重复。bd.对 CUTO-28 亲本和 TPM3-ROS1 L2086F 细胞产生的裂解物的磷酸化和总 MAPK(ERK1/2)以及蛋白质 S6 进行免疫印迹分析,这些细胞分别用 25 nM 恩曲替尼、卡博替尼和吉利替尼处理 2、4、6、8 和 24 小时。
靶向癌症治疗
Lymphoma: Ibritumomab tiuxetan (Zevalin) , denileukin diftitox (Ontak) , brentuximab vedotin (Adcetris) , rituximab (Rituxan) , vorinostat (Zolinza) , romidepsin (Istodax) , bexarotene (Tartene) , borzotremi (Velcatremia) (Velcatremia) tyn) , ibrutinib (Imbruvica) , siltuximab (Sylvant) , idelalisib (Zydelig) , belinostat (Beleodaq) , obinutuzumab (Gazyva) , nivolumab (Opdivo) , pembrolizumab (Keytruda) , rituximab and hyaluronidase (Rhuman hydroxide) Aliqopa) , axicabtagene ciloleucel (Yescarta) , acalabrutinib (Calquence) , tisagenlecleucel (Kymriah) , venetoclax (Venclexta) , mogamulizumab-kpkc (Poteligeo) , duvelisib (Copiktra) , poltuzutinib-poladopinib (Bruxiq, Zanquiq) insa) , tazemetostat hydrobromide (Tazverik) , selinexor (Xpovio) , tafasitamab-cxix (Monjuvi) , brexucabtagene autoleucel (Tecartus) , crizotinib (Xalkori) , umbralisib tosylate (Ukoniq) , mara lisocab (Bleugene)
无法治愈的实体癌症的发病轨迹
一名 58 岁女性患者,主诉严重的髋部疼痛和进行性呼吸困难。她被诊断为 4 期非小细胞肺癌,伴有淋巴结和骨骼转移。髋部疼痛是由骨转移引起的,她接受了大剂量芬太尼和萘普生治疗。由于细菌性肺炎的发展,她的呼吸困难加重,她被转入重症监护室,在那里开始使用广谱抗生素和人工通气。由于患者有原癌基因酪氨酸蛋白激酶 1 重排,因此还开始使用靶向治疗克唑替尼治疗。一周内,呼吸困难减轻,对人工通气的需求也随之减轻。患者的髋部疼痛也大大减轻,因此可以减少大剂量的阿片类药物。转入重症监护室几天后,她身体状况良好出院。
Alectinib诱导SJS/10:案例报告和评论
肺癌是世界上第二常见的CER类型,腺癌是最常见的变体之一,速率为35-40%。[1]近年来,在NSCLC中,与遗传改变有关,生物分子标记物已成为高级NSCLC治疗的基石,该治疗超过了标准的化学疗法。egfr,Alk,Ros1,Met和Braf是在腺癌中调查的最常见的驱动器突变。已重新排列的患者的反应率和无疾病生存率提高了。[2]针对性的治疗中的响应率范围为50至80%。总体生存率增加到18到38.6个月。[3,4] ALK突变在百分比3-5岁的患者中,尤其是年轻的患者,不吸烟女性。[5]有几种类型的ALK-TKI,包括第一代克唑替尼;第二代Alectinib,Ceri-Tinib,Brigatinib和第三代Lorlatinib。[6] Alectinib-基于Alex,J-Alex和Alesia研究,目前在ALK阳性NSCLC中首选的高度选择性的口服第二代ALK-TKI是优选的一线治疗。[7,8]患有Alectinib患者的患者的PFS率明显高于Crizotinib的PFS率明显高于10.9个月,HR:0.43,95%CI:0.32–0.58)。[9]同样,Peters等人。[10]证明克唑替尼和阿尔氏PFS率分别为48.7%,分别为68.4%。在更新的亚历克斯研究中,中位治疗为28.1个月,在152名患者中,任何级别
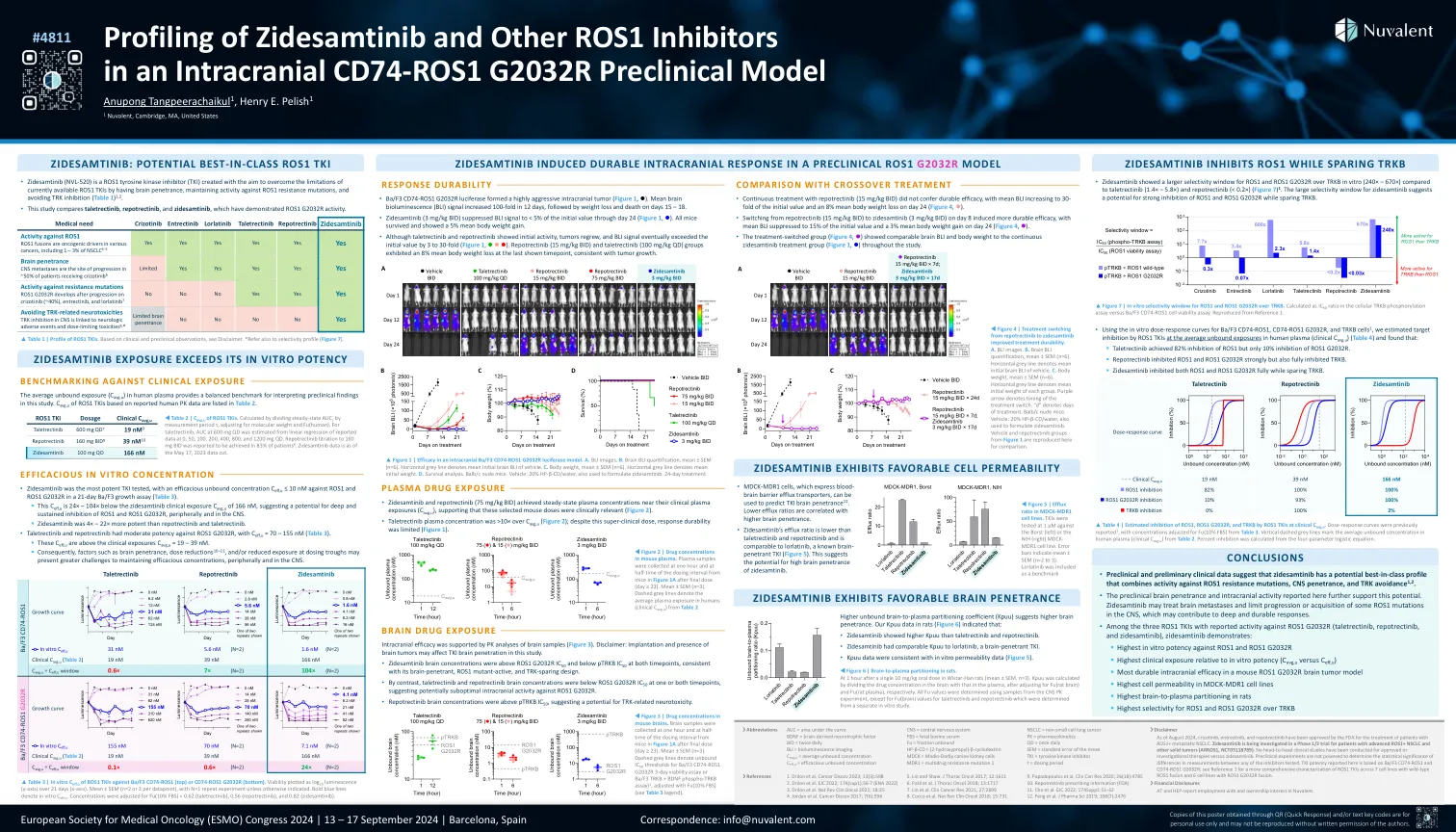
#4811 Zidesamtinib和其他ROS1抑制剂在颅内CD74-ROS1 G2032R临床前模型
截至2024年8月,FDA已批准Crizotinib,Entretectinib和Repotrectinib用于治疗ROS1 +转移性NSCLC患者。Zidesamtinib正在针对晚期ROS1 + NSCLC和其他实体瘤患者的1/2期试验中进行研究(ARROS1,NCT05118789)。与Zidesamtinib批准或研究疗法没有进行头对头临床研究。临床前实验没有能力确定测量的任何抑制剂之间测量值差异的统计显着性。TKI效力基于BA/F3 CD74-ROS1和CD74-ROS1 G2032R;有关在具有野生型ROS1融合的7个细胞系和具有ROS1 G2032R融合的6个细胞系的ROS1 TKI的更全面的表征,请参见参考1。❯财务披露