XiaoMi-AI文件搜索系统
World File Search System开发潜在的细胞和基因治疗产品
本指导文件仅供评论之用。请在《联邦公报》上公布指导草案的日期之前,提交一套电子或书面意见。将电子意见提交至 https://www.regulations.gov 。将书面意见提交至食品药品管理局卷宗管理人员(HFA-305),5630 Fishers Lane,Rm。1061,Rockville,MD 20852。您应该在《联邦公报》上公布的可用性通知中列出的卷宗编号中注明所有意见。可从通信、推广和发展办公室(OCOD)获取本指导的更多副本,地址为 10903 New Hampshire Ave.,Bldg. 71,Rm。 3128, Silver Spring, MD 20993-0002,或致电 1-800-835-4709 或 240-402-8010,或发送电子邮件至 ocod@fda.hhs.gov,或通过互联网访问 https://www.fda.gov/vaccines-blood-biologics/guidance-compliance-regulatory-information-biologics/biologics-guidances。如对本指南内容有疑问,请通过上述电话号码或电子邮件地址联系 OCOD。
中性粒细胞中加油动物D的NLRP1依赖性激活控制皮肤利什曼病
1洛桑大学免疫生物学系,瑞士,2岁,WHO免疫研究与培训合作中心,洛桑大学,瑞士大学,瑞士大学,3个媒介分子生物学科,疟疾实验室,疟疾实验室和媒介研究所,摩洛克国立卫生部,玛丽·诺斯特·诺斯特,摩克斯特式,摩洛克,国际研究所。 States of America, 4 Post Graduate Department of Zoology, Barasat Government College, Barasat, West Bengal, India, 5 INSERM, CNRS, Centre D'Immunologie de Marseille-Luminy, Aix-Marseille Universite´, Marseille, France, 6 Department of Molecular Microbiology and Immunology, Keck School of Medicine, University of Southern California, Los Angeles, California, United States of America
改进的胞嘧啶碱基编辑器的基因组和转录组范围的脱靶分析
1 博伊斯汤普森研究所,纽约州伊萨卡 14853,美国;2 马里兰大学植物科学与景观建筑系,马里兰州帕克分校,美国;3 扬州大学农学院,江苏省作物基因组学与分子育种重点实验室/植物功能基因组学教育部重点实验室,扬州 225009,中国;4 扬州大学江苏省粮食作物现代生产技术协同创新中心,扬州 225009,中国;5 康奈尔大学植物育种与遗传系,纽约州伊萨卡 14853;6 马里兰大学生物科学与生物技术研究所,马里兰州罗克维尔 20850。Ɨ 上述作者对本文贡献相同。
急性髓样白血病:抗治疗性和四跨胶质膜支架的潜在作用分子病理学教育:基因组医学中的初级保健居民培训的建议框架:分子病理培训协会培训与教育委员会的报告
来自培训和教育委员会的分子遗传病理学课程工作组,*分子病理协会,马里兰州罗克维尔;纽约纽约纪念斯隆·凯特林癌症中心病理与实验室医学系;爱荷华州爱荷华州爱荷华州Z大学病理学系,爱荷华州爱荷华城;细胞遗传学和分子病理学,X传统健康,俄勒冈州波特兰; {新墨西哥大学,新墨西哥州阿尔伯克基大学病理学系;俄亥俄州俄亥俄州韦克斯纳医学中心K病理学系,俄亥俄州哥伦布;新罕布什尔州黎巴嫩达特茅斯 - 希区柯克医学中心病理与实验室医学系;以及新罕布什尔州YY Hanover的Dartmouth的Geisel医学院
在代谢疾病患者中发现的人类 GPR17 错义变异具有不同的下游信号传导特征
来自 1 美国印第安纳州印第安纳波利斯印第安纳大学医学院儿科系 Herman B. Wells 儿科研究中心和 2 糖尿病与代谢疾病中心;3 美国马里兰州罗克维尔国立卫生研究院国家转化科学促进中心;4 美国纽约州纽约市西奈山伊坎医学院伊坎基因组学和多尺度生物学研究所遗传学和基因组科学系;5 美国康涅狄格州斯坦福德西奈山大学 Sema4 项目;6 美国印第安纳州印第安纳波利斯印第安纳大学医学院药理学和毒理学系、7 斯塔克神经科学研究所、8 生物化学和分子生物学系和 9 解剖学、细胞生物学和生理学系
沟通和传播策略,以促进与健康相关的证据使用
我们欢迎对该系统评价的评论。可以通过邮件发送到下面的任务订单官员,网址为:医疗保健研究与质量机构,540 Gaither Road,Rockville,MD 20850,或通过电子邮件发送至epc@ahrq.hhs.gov。Richard G. Kronick博士Jean Slutsky,P.A.,M.S.P.H. 医疗保健研究与质量质量研究和质量质量史蒂芬妮·张(Stephanie Chang,M.D.) 玛丽安·詹姆斯(Marian James),博士学位,硕士 EPC计划任务命令官员成果和证据中心的董事和医疗保健研究和质量质量机构的证据中心和质量质量机构威廉·劳伦斯(M.D.),硕士 任务订单官员中心和医疗保健研究和质量证据局Richard G. Kronick博士Jean Slutsky,P.A.,M.S.P.H.医疗保健研究与质量质量研究和质量质量史蒂芬妮·张(Stephanie Chang,M.D.)玛丽安·詹姆斯(Marian James),博士学位,硕士EPC计划任务命令官员成果和证据中心的董事和医疗保健研究和质量质量机构的证据中心和质量质量机构威廉·劳伦斯(M.D.),硕士任务订单官员中心和医疗保健研究和质量证据局
2041设施总体规划 - 马里兰卫生部
John L. Gildner Rica,位于马里兰州罗克维尔市Broschart Road 15000号,是一种基于社区的治疗方法和特殊教育设施,为患有严重情绪障碍的青少年提供服务。 现场学校是通过MDH和蒙哥马利县公立学校之间的合作伙伴关系来管理的。 该设施已获得卫生保健质量办公室的许可和认证,并获得联合委员会的认可。 联合委员会联合委员会认证并认证了美国的22,000多个医疗保健组织和计划,包括医院和医疗保健组织,这些医院和医疗保健组织提供基于门诊和办公室的手术,行为健康,家庭医疗保健,实验室和护理中心服务。 是一个独立的,非营利的组织,联合委员会是该国最古老,最大的标准制定和认可的卫生保健机构。 长期急诊医院(“ LTACH”)John L. Gildner Rica,位于马里兰州罗克维尔市Broschart Road 15000号,是一种基于社区的治疗方法和特殊教育设施,为患有严重情绪障碍的青少年提供服务。现场学校是通过MDH和蒙哥马利县公立学校之间的合作伙伴关系来管理的。该设施已获得卫生保健质量办公室的许可和认证,并获得联合委员会的认可。联合委员会联合委员会认证并认证了美国的22,000多个医疗保健组织和计划,包括医院和医疗保健组织,这些医院和医疗保健组织提供基于门诊和办公室的手术,行为健康,家庭医疗保健,实验室和护理中心服务。是一个独立的,非营利的组织,联合委员会是该国最古老,最大的标准制定和认可的卫生保健机构。长期急诊医院(“ LTACH”)
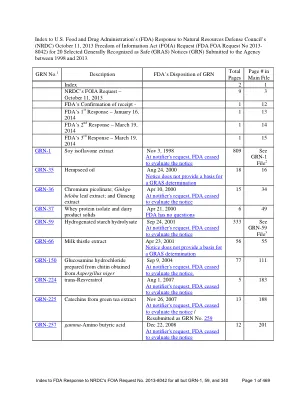
NRDC:食品中化学物质的安全漏洞 - FDA 对 NRDC FOIA 请求编号 2013-8042(除 GRN-1、59 和 340 外)的回应索引 (PDF)
2013 年 10 月 11 日 通过传真和挂号邮件 食品药品管理局 信息自由司 共享服务办公室 公共信息和图书馆服务办公室 12420 Parklawn Drive ELEM-1029 Rockville, MD 20857 传真:(301) 827-9267 事由:FOIA 要求提供有关机构收到的一般公认安全通知的记录 尊敬的 FOIA 官员: 我代表自然资源保护委员会 (NRDC) 写信,请求根据《信息自由法》(“FOIA”),5 U.S.C. 披露记录。§ 552 和适用的食品药品管理局 (FDA) 法规,21 C.F.R.第 20 部分。I.所寻求记录的描述 请提供 FDA 在 2013 年 9 月 30 日或之前持有、保管或控制的与附录 A 中描述的一般公认安全 (GRAS) 通知相关的记录 1。我们特别寻求以下记录:
以患者为中心的药物研发:将临床结果评估纳入监管决策的终点
指导草案 本指导文件仅供评论之用。有关本草案的评论和建议应在《联邦公报》上公布指导草案发布通知后 ___ 天内提交。将电子评论提交至 https://www.regulations.gov 。将书面评论提交至食品药品管理局档案管理人员 (HFA-305),地址:5630 Fishers Lane, Rm. 1061, Rockville, MD 20852。所有评论都应标明《联邦公报》上公布的发布通知中列出的档案编号。如对本草案文件有疑问,请联系 (CDER) 药品信息部通讯办公室,邮箱:druginfo@fda.hhs.gov,电话:855-543-3784 或 301-796-3400,或 (CBER) 通讯、外联和发展办公室,邮箱:800-835-4709 或 240-402-8010,或 (CDRH) 患者科学和参与计划,邮箱:CDRH-PRO@fda.hhs.gov,电话:301-796- 6715。
以患者为中心的药物研发
本指导文件仅供评论之用。对本文件草案的评论和建议应在《联邦公报》上公布指导草案发布通知后 90 天内提交。将电子评论发送至 http://www.regulations.gov。将书面评论发送至食品药品管理局卷宗管理人员(HFA-305),地址:5630 Fishers Lane, rm. 1061, Rockville, MD 20852。所有评论均应注明《联邦公报》上公布的发布通知中所列的卷宗编号。如对本文件草案有疑问,请联系(CDER)药品信息部通讯办公室,邮箱:druginfo@fda.hhs.gov,电话:855-543-3784 或 301-796-3400;或(CBER)沟通、推广和发展办公室,邮箱:ocod@fda.hhs.gov,电话:800-835-4709 或 240-402-8010;或战略伙伴关系和技术创新办公室、设备和放射健康中心,邮箱:cdrh-pro@fda.hhs.gov,电话:800-638-2041 或 301-796-7100。