XiaoMi-AI文件搜索系统
World File Search Systemruxolitinib
JAK抑制增强了霍奇金淋巴瘤患者的检查点阻滞性封锁免疫疗法
通过检查点抑制剂免疫疗法释放抗肿瘤T细胞活性,对癌症患者有效,但临床反应受到限制。通过JAK/STAT途径的细胞因子信号传导与检查点免疫疗法抗性相关。我们报告了Hodgkin淋巴瘤患者在检查点抑制剂免疫疗法后复发或难治性的Hodgkin淋巴瘤患者中使用抗PD-1抗体nivolumab对JAK抑制剂ruxolitinib进行的I期临床试验。该组合的最佳总体响应率为53%(10/19)。r核替尼显着降低了中性粒细胞与淋巴细胞的比率和髓样抑制细胞的百分比,但增加了细胞因子产生的T细胞的数量。ruxolitinib拯救了耗尽的T细胞的功能,并增强了免疫检查点阻滞在临床前实体瘤和淋巴瘤模型中的功效。该协同作用的特征是从抑制性降低到免疫刺激性髓样细胞的转换,从而增强了T细胞分裂。
报销建议
加拿大卫生部根据其适应症审查了鲁索替尼乳膏的证据,该适应症将鲁索替尼乳膏的使用范围限制在轻度至中度 AD 患者,这些患者的病情无法通过 TCS 和/或 TCI 得到充分控制,并且不适合接受这些治疗。然而,两项双盲、随机、载体对照试验(TRuE-AD1,N = 631;TRuE-AD2,N = 618)招募了轻度至中度 AD 患者,且未根据对先前 TCS 和/或 TCI 治疗的反应限制试验入选人数。尽管关键试验的结果表明,对于 12 岁及以上的轻度至中度 AD 患者,使用 1.5% 芦可替尼乳膏治疗 8 周,与使用载体乳膏相比,在实现研究者总体评估-治疗成功率 (IGA-TS) 和湿疹面积和严重程度指数 75 (EASI-75) 反应方面具有额外的临床益处,但试验人群并未反映根据所审查的适应症预期使用芦可替尼乳膏的情况。近期有 TCS 和/或 TCI 治疗史的患者的事后亚组分析已作为支持证据提交;然而,亚组分析中对 TCS 和/或 TCI 反应不足的患者比例仍然未知。此外,由于方法学限制,包括缺乏样本量考虑和多重性控制,这些事后亚组分析的结果尚无定论。
当前预防和治疗急性和慢性GVHD
摘要:虽然AGVHD具有强烈的炎症成分,而CGVHD显示自身免疫和纤维化特征;发病率和危险因素相似,但不完全相同;实际上,AGVHD是CGVHD的主要危险因素。钙调蛋白抑制剂(CNI)具有甲氨蝶呤(MTX)或霉酚酸酯(MMF)仍然代表HLA匹配的同种异体干细胞移植(HSCT)中的标准预防。其他策略侧重于ATG,移植后环磷酰胺(PTCY),Abatacept和移植物操纵。尽管率很高,但AGVHD的一线治疗以皮质类固醇为代表,而鲁索利替尼是标准的二线治疗。研究方法包括菌群移植和间充质干细胞的输注。GVHD是一种涉及任何解剖区的多效性疾病;同样,鲁唑替尼代表了这种情况下类固醇难治性CGVHD的标准。这是一种涉及任何解剖区的多效性疾病;同样,鲁唑替尼代表了这种情况下类固醇难治性CGVHD的标准。体外光疗法(ECP)仍然是用于类固醇折射率或实现类固醇比例的选项。对于ruxolitinib-fractory CGVHD,Belumosudil和Axatilimab代表了最有前途的药物。支气管炎闭塞性综合征(BOS)仍然是一个挑战。在靶向非免疫效应子的化合物中,中性粒细胞弹性酶抑制剂Alvelestat在BOS中似乎很有希望。最后,在AGVHD和CGVHD中,生物学标记与特定疾病表现的关联可以帮助完善风险分层以及可靠的生物标志物用于特定治疗。
转换1:随机,双盲,安慰剂 - ...
Transform-1: randomed, double-blind, placebo-controlled, multiticenter, international phase 3 study of navitoclax in combination with ruxolitinib versus ruxolitib plus placebo with untreted myelo MrcP, Frcpath, Phd 2 , 3 , Tim cp Somevaille, Pldfrcp Frcpath 4 , James Kcloskey, McCloskey, McCloskey, MD 5 , MD 6,Steffen Koschmieder 7,David Lavie MD 11,MariaTeresaGómez-Cares,MD PhD 12,Emanueleme Amunna,MD PLD 13,Ho-Jin Shin,MD 14,Keita Kirito,Keita Kirito,MD tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy devos, tmothy 16 Chuah 19 , Atanas Radinoff 20 , Andrija Bodanovic,21,22教授,Rasislav Mosal,Pharmd 23,Qi Jiang 23,Avijeet S Chopra 23,Jalaja Pot 23 Passmonti,MD 25
完整处方信息-AccessData.fda.gov
ruxolitinib在器官发生期间口服给怀孕的大鼠或兔子,大鼠的剂量为15、30或60 mg/kg/天,兔子的10、30或60 mg/kg/day。任何剂量都没有与治疗相关的畸形。在最高和母体毒性剂量为60 mg/kg/天的大鼠中,胎儿体重的降低约为9%。这种剂量导致全身性暴露约22倍的临床全身性暴露于最大建议的人剂量(MRHD; Ruxolitinib Cream的临床全身性暴露,每天两次适用于25-40%的十二-40%的特应性皮肤炎受皮肤炎影响的人体表面积,用于计算人类暴露于人类的多重暴露量)。在兔子中,较低的胎儿体重约为8%,而晚期疗效增加,最高和母体毒性的剂量为60 mg/kg/day。这种剂量导致系统性暴露约70%,MRHD临床全身暴露。
Krazati(Adagrasib)的EU风险管理计划
1。药用产品的名称opzelura 15 mg/g奶油2。定性和定量组成一克奶油中含有15毫克的鲁唑替尼(作为磷酸盐)。具有已知作用丙二醇(E1520),150 mg/g的奶油cetyl饮料,30 mg/g奶油硬脂醇,17.5 mg/g的奶油甲基甲基甲基二苯甲酸酯(E218),1 mg/g的奶油丙基parahydrox -0.5 mg/g g的。羟基苯二酚(作为石蜡中的抗氧化剂,白色软)(E321)有关赋形剂的完整列表,请参见第6.1节。 3。 制药形式奶油白色至灰白色奶油。 4。 临床细节4.1治疗指示OPZELURA用于治疗非段性白癜风,面部参与12岁的成年人和青少年。 4.2 opzelura的生态学和方法应由具有诊断和治疗非段性白癜风的经验的医生开始和监督。 Posology成年人推荐的剂量是每天两次涂上薄薄的奶油,最多可占身体表面积(BSA)的10%(BSA),在两种ruxolitinib奶油施用之间至少8小时。 10%BSA代表用5个手指的一只手的棕榈的10倍。 ruxolitinib奶油应在必需的最小皮肤区域使用。 应使用每月不超过100克的两个管。 令人满意的重新构度可能需要在24周内进行治疗。 如果在第52周的治疗区域中的重新调整少于25%,则应考虑治疗中断。。羟基苯二酚(作为石蜡中的抗氧化剂,白色软)(E321)有关赋形剂的完整列表,请参见第6.1节。3。制药形式奶油白色至灰白色奶油。4。临床细节4.1治疗指示OPZELURA用于治疗非段性白癜风,面部参与12岁的成年人和青少年。4.2 opzelura的生态学和方法应由具有诊断和治疗非段性白癜风的经验的医生开始和监督。Posology成年人推荐的剂量是每天两次涂上薄薄的奶油,最多可占身体表面积(BSA)的10%(BSA),在两种ruxolitinib奶油施用之间至少8小时。10%BSA代表用5个手指的一只手的棕榈的10倍。ruxolitinib奶油应在必需的最小皮肤区域使用。应使用每月不超过100克的两个管。令人满意的重新构度可能需要在24周内进行治疗。如果在第52周的治疗区域中的重新调整少于25%,则应考虑治疗中断。一旦达到令人满意的重新调整,就可以停止在这些地区进行治疗。如果在治疗中停用后会出现脱位,则可以在患病区域重新启动治疗。
使用食品和药物管理不良事件报告S
用JAK抑制剂和MST事件之间的治疗之间的时间间隔因药物而异。upadacitib的发作时间比其他抑制剂要短得多。由于upadacitib是一种批准的特应性皮炎药物,看起来与皮肤癌非常相似,因此有时很难确定皮肤癌是否与药物有关或是错误的判断。应在报告的情况下考虑这一点。tofacitinib和ruxolitinib的发作时间最长。在收集的JAK抑制剂和MST事件的案例研究中[13-17],发作
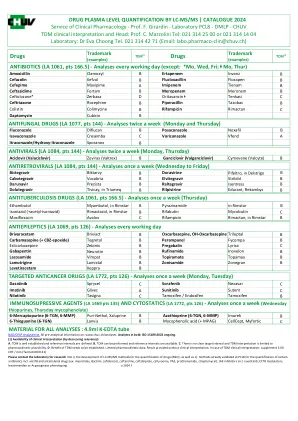
通过 lc-ms/ms 定量药物血浆浓度
请联系实验室研究 i) 开发用于药物量化的 LC-MS/MS 方法(研发),以及 ii) 已在 PCL8 上验证的用于量化某些抗生素的方法,包括抗结核病和抗疟药(例如:大环内酯类、复方新诺明、头孢地洛、头孢比普、头孢呋辛、PAS、丙硫异烟胺、链霉素);JAK 抑制剂包括芦可替尼;CFTR 调节剂;左西孟旦或天冬酰胺酶表型分析。v.2024.f
针对骨髓增生性肿瘤中的 PI3K 通路
摘要简介:在部分患者中,Janus 激酶 (JAK) 抑制剂(如芦可替尼)的疗效随时间推移而降低以及初始反应不佳是与骨髓增生性肿瘤 (MPN)(主要是骨髓纤维化)相关的关键临床挑战。涵盖的领域:讨论了磷脂酰肌醇-3 激酶 (PI3K) 在 MPN 疾病进展和治疗耐药性中的作用,以及作为对 JAK 抑制失去反应的患者的潜在治疗靶点。了解 MPN 发病机制中涉及的复杂信号网络已确定了潜在的新治疗靶点和治疗策略,例如抑制除 JAK/信号转导和转录激活因子 (STAT) 通路之外的其他信号通路。PI3K 在 JAK 信号下游在挽救肿瘤细胞增殖方面起着至关重要的作用,其中 PI3Kδ 在血液系统恶性肿瘤中尤为重要。同时靶向 PI3K 和 JAK/STAT 通路可能提供一种创新的治疗策略,以最大限度地提高疗效。专家意见:基于我们对潜在机制和 PI3K 通路信号在 JAK 抑制剂治疗反应丧失或耐药性中的作用的理解以及临床研究的初步结果,parsaclisib(PI3Kδ 抑制剂)和芦可替尼的组合具有巨大的临床潜力。如果在更大规模的临床试验中得到证实,parsaclisib 可能会为 MPN 患者提供更多的治疗选择并改善临床结果。
lnk/sh2b3是少年脊髓细胞的新型驱动器...
在近90%的少年脊髓细胞性白血病(JMML)的患者中,检测到五个规范RAS途径基因(NF1,NRAS,KRAS,PTPN11和CBL)的突变,这是早期童年的致命性恶性肿瘤。在本报告中,我们描述了七名被诊断为SH2B3突变的JMML的患者,其中包括5例被发现有启动,基因功能丧失突变的患者。SH2B3编码适配器蛋白LNK,这是RAS途径上游正常出血poiesis的负调节剂。这些突变被确定为种系,体细胞或两者的组合。在其他髓样恶性肿瘤中观察到的LNK功能的丧失,由于细胞因子超敏反应和JAK/STAT信号通路的激活而导致HE Matopoietic细胞的异常增殖。在诱导多能干细胞衍生的JMML样造血祖细胞中的体外研究也表明SH2B3-MU感染了造血祖细胞对JAK抑制作用的敏感性。 最后,我们描述了两名用JAK1/2抑制剂ruxolitinib治疗的JMML和SH2B3突变的患者。 本报告扩大了JMML中启动突变的频谱,并提高了针对SH2B3突变患者的JAK/STAT途径的可能性。在诱导多能干细胞衍生的JMML样造血祖细胞中的体外研究也表明SH2B3-MU感染了造血祖细胞对JAK抑制作用的敏感性。最后,我们描述了两名用JAK1/2抑制剂ruxolitinib治疗的JMML和SH2B3突变的患者。本报告扩大了JMML中启动突变的频谱,并提高了针对SH2B3突变患者的JAK/STAT途径的可能性。