XiaoMi-AI文件搜索系统
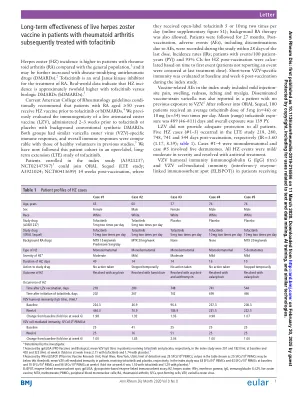
World File Search System带状疱疹活疫苗对随后接受托法替尼治疗的类风湿关节炎患者的长期有效性
目前,美国风湿病学会指南有条件地建议年龄≥50岁的类风湿性关节炎患者在服用托法替尼或bDMARDs之前接种HZ疫苗。4 我们之前评估了减毒带状疱疹疫苗 (LZV) 的免疫原性,该疫苗在服用托法替尼或安慰剂前 2-3 周接种,背景为常规合成 DMARDs。两组患者对水痘带状疱疹病毒 (VZV) 的特异性免疫反应相似,总体免疫反应与之前研究中的健康志愿者相当。5 我们现在已经对这组患者进行了一项开放标签、长期扩展 (LTE) 的托法替尼研究。参与指数研究 (A3921237; NCT02147587) 的患者可在接种疫苗后 14 周加入 ORAL Sequel (LTE 研究; A3921024; NCT00413699),其中
在Omicron BA.2爆发期间,福建为有症状的Covid-19灭活疫苗有效性
此外,一项建模研究表明,北京属于的地方的累积感染率超过90%(1),这与中国大陆疫苗覆盖率不一致。共有三种类型的共证疫苗,包括灭活的疫苗,腺病毒载体疫苗和重组蛋白疫苗。其中,超过90%的中国公民已经完成了2剂替代的替代疫苗,由Sinovac Biotech Ltd.和Sinopharm Group Co. Ltd.(2)完成。在2020年根据野生型SARS-COV-2开发,并且在三角洲变体波中的效果显着降低。在Omicron Ba.2变体波中,Wan等。 先前已经报道说,疫苗对冠状动脉疫苗感染的疫苗有效性在加强剂量后为19.8%,在2剂剂量后未观察到(3)。 毫无疑问,灭活的COVID-19疫苗对感染和症状是不可能的。 然而,了解何时失活的疫苗失去其有效性仍然具有未来疫苗开发和对Covid-19的反应的显着参考价值。在Omicron Ba.2变体波中,Wan等。先前已经报道说,疫苗对冠状动脉疫苗感染的疫苗有效性在加强剂量后为19.8%,在2剂剂量后未观察到(3)。毫无疑问,灭活的COVID-19疫苗对感染和症状是不可能的。然而,了解何时失活的疫苗失去其有效性仍然具有未来疫苗开发和对Covid-19的反应的显着参考价值。
针对因黄热病而来的乘客的指南......
24 小时内可以接种多种不同类型的活疫苗。但是,如果接种第一种活疫苗(例如:MMR、BCG、口服伤寒、鼠疫、口服脊髓灰质炎、流感、斑疹伤寒)后已过 24 小时,则应在 28 天后接种另一种活疫苗(例如黄热病)。这是基于科学研究,研究表明,当两种不同类型的活疫苗间隔超过 24 小时但少于 28 天时,免疫反应会降低。
AIP-Principles-Immunization-HSCT-SOT.pdf
患者已停用免疫抑制药物至少三个月。这是活疫苗*的绝对要求。非活疫苗可在 6 – 12 个月时接种;但免疫原性有限,因此最好等到 24 个月或更晚。移植后头两年内禁用活疫苗*(包括黄热病)。此后,如果患者没有复发或活动性移植物抗宿主病,并且患者停用免疫抑制药物,则可以接种活疫苗*。对于旅行疫苗,请将个人转介给当地旅行健康专业人士。
灭活疫苗BBIBP-CORV(VERO细胞)的长期有效性针对摩洛哥的严重住院和关键住院
,我们从2021年2月至2021年10月在摩洛哥进行了18岁或长达18岁以上的人群进行了测试,病例对照研究。来自国家实验室COVID-19数据库;我们确定了在严重和关键的COVID-19病例中呈RT-PCR呈阳性的病例,以及对SARS-COV-2进行负RT-PCR检验的对照。 来自国家疫苗接种登记册(NVR);鉴定出并鉴定出未接种疫苗的疫苗(VERO细胞)疫苗接种的个体,并包括在研究中。 基于疫苗收据的时间与SARS-COV-2 RT-PCR测试日期进行了数据库之间的联系以研究疫苗接种状态。 对于对SARS-COV-2测试阳性的每个人,我们确定了一个受测试的匹配对照参与者。 我们使用有条件的逻辑回归估计针对SARS-COV-2严重疾病/住院的疫苗有效性。来自国家实验室COVID-19数据库;我们确定了在严重和关键的COVID-19病例中呈RT-PCR呈阳性的病例,以及对SARS-COV-2进行负RT-PCR检验的对照。来自国家疫苗接种登记册(NVR);鉴定出并鉴定出未接种疫苗的疫苗(VERO细胞)疫苗接种的个体,并包括在研究中。基于疫苗收据的时间与SARS-COV-2 RT-PCR测试日期进行了数据库之间的联系以研究疫苗接种状态。对于对SARS-COV-2测试阳性的每个人,我们确定了一个受测试的匹配对照参与者。我们使用有条件的逻辑回归估计针对SARS-COV-2严重疾病/住院的疫苗有效性。
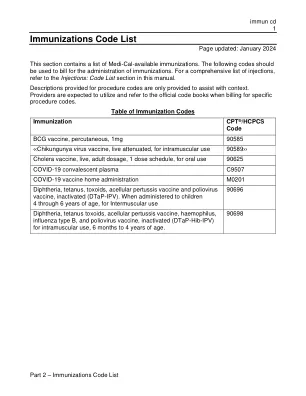
免疫接种代码表 (immun cd)
日本脑炎病毒灭活疫苗,肌肉注射用 90738 麻疹/腮腺炎/风疹病毒活疫苗 (MMR) 90707 麻疹、腮腺炎、风疹和水痘活疫苗 (MMRV) 90710 脑膜炎球菌结合疫苗,血清群 A、C、Y 和 W-135,四价(MCV4 或 MenACWY)
369118 R1 狂犬病和犬钩端螺旋体病联合灭活疫苗
剂量和给药方法 皮下注射 1 毫升疫苗。Nobivac RL 适用于 8 周龄以上的狗。当狗需要同时接种狂犬病和钩端螺旋体病疫苗时,请使用该疫苗。狂犬病的初次疫苗接种从 12 周龄开始,仅需接种一次。初次疫苗接种可以在更早的年龄进行,但必须从 12 周龄开始重复接种,并且第一次接种后至少 2 周。钩端螺旋体病的初次疫苗接种需要间隔 2-4 周接种两次。
嗜水气单胞菌热灭活疫苗候选株的免疫原性
嗜水气单胞菌经常攻击养殖的鲶鱼,并在印度尼西亚南加里曼丹省引起运动性气单胞菌败血症 (MAS) 疾病爆发。嗜水气单胞菌攻击造成的死亡可能达到 100%,因此需要通过接种疫苗进行预防。本研究旨在检查 6 种热灭活嗜水气单胞菌疫苗候选物的潜在免疫原性,该菌株是印度尼西亚南加里曼丹省班加尔地区的一种菌株。嗜水气单胞菌菌株是从印度尼西亚南加里曼丹省班加尔区周围的水产养殖池塘中感染的鲶鱼中获得的。从10条感染MAS的鱼中分离出14株细菌,其中Sungai Batang村分离出8株(AGC-1、AGC-2、AGC-3、AGC-4、AGC-6、AKC-2、AKC-3、AKC-5),Cindai Alus村分离出6株(AGC-8、AGC-9、AKC-7、AKC-8、AKC-9、AKC-10)。AGC表示从鳃中分离出的气单胞菌,AKC表示从肾脏中分离出的气单胞菌。热灭活A.hydrophila疫苗的候选抗原是在100℃加热60分钟使其失活。结果显示,AGC-2和AGC-8菌株的抗原具有较高的免疫原性,因为与其他菌株和对照相比,它们可以提高抗体滴度。加强免疫两周后鲶鱼体内抗体滴度升高并趋于一致。交叉反应试验结果表明AGC-2和AGC-8株抗原能与AGC-1、AKC3、AKC-5株发生交叉反应,但不能与AKC-7发生交叉反应,因此AGC-2和AGC-8可推荐作为印尼南加里曼丹省MAS病的疫苗候选疫苗。