机构名称:
¥ 2.0
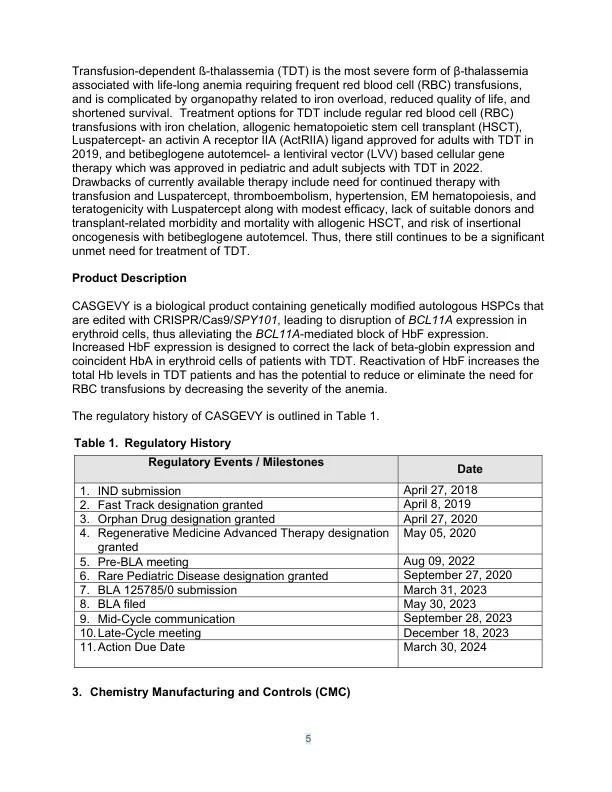
1. 简介 Vertex Pharmaceuticals Inc.(申请人)于 2023 年 3 月 31 日提交了生物制品许可申请 (BLA) 125785,以许可 exagamglogene autotemcel(exa-cel,以下简称为 CASGEVY,专有名称),用于治疗 12 岁及以上的输血依赖性 β-地中海贫血 (TDT) 患者。在提交 STN 125785 后,CASGEVY 还根据另一项 BLA(STN 125787)接受审查,用于不同的适应症,并于 2023 年 12 月 8 日根据该 BLA 获得批准,用于治疗 12 岁及以上的镰状细胞病 (SCD) 和复发性血管闭塞性危象 (VOC) 患者。经批准后,BLA STN 125785 将在行政上关闭,并且这两项适应症的未来监管活动将在 BLA STN 125787 下进行。
2024 年 1 月 16 日监管行动依据摘要