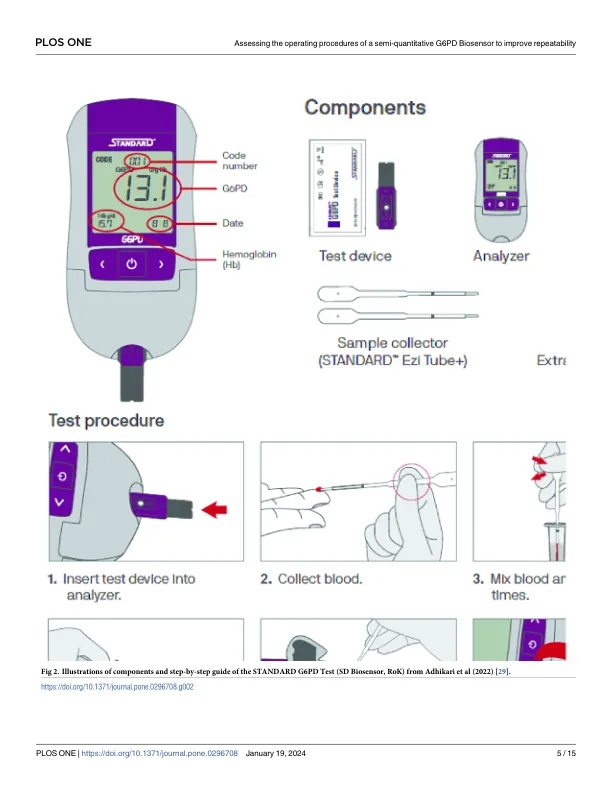
在偏远社区中,诊断G6PD缺乏症是具有挑战性的。我们评估了改进的测试程序的影响和延迟的测试诊断标准G6PD(SDBIOSENSOR,ROK)的影响,并评估了建议的临界值。我们测试了指纹(标准方法)和微晶剂(BD,美国;方法1),来自真空吸水剂的静脉血(BD,USA;方法2),不同的样品申请方法(方法3)和使用的微夹,而不是测试的单使用移液器(方法4)。通过比较配对度量之间的中位差异来评估可重复性。在实验室条件下对三名志愿者进行了20次测试。在印度尼西亚和尼泊尔测试了具有最佳重复性的标准方法和方法。在印度尼西亚,两种方法都以两种方式对60名参与者进行了测试,在尼泊尔120位参与者中,通过这两种方法都以两种方式进行了测试。生物传感器标准方法读数的调整后的男性中位数(AMM)定义为100%活性。在印度尼西亚,比较了标准方法和修改方法的配对读数之间的差异,以评估延迟测试的影响。在试点研究中的可重复性并没有显着差异(p = 0.381);方法3显示最低的变异性。一个尼泊尔参与者的活动<30%,一名印尼和10名尼泊尔参与者具有中间活动(30%至<70%的活动)。与标准方法相比,延迟5小时后,通过方法3进行的G6PD测量值为0.4U/GHB(IQR:-0.2至0.7,P = 0.005)。我们无法提高可重复性。可重复性在印度尼西亚没有显着差异(标准:0.2U/GHB [IQR:0.1-0.4];方法3:0.3U/GHB [IQR:0.1-0.5]; P = 0.425)或NEPAL(标准:0.4U/GHB [0.4U/GHB [IQR:0.2-0.6]; 0.2-0.6];方法3:0.3.3:0.3:0.3:0.B [iq]; p [iq]; 0.330)。通过标准方法对100%活动的定义与制造商推荐的截止值匹配70%的活动。最多5小时的延迟并未导致
半...
主要关键词