XiaoMi-AI文件搜索系统
World File Search System成簇规律间隔短回文基因编辑技术
摘要 利用CRISPR-Cas9技术开展遗传疾病治疗已取得重大进展。本文讨论了 CRISPR-Cas9 的历史和工作原理,重点介绍了其在遗传疾病治疗中的应用。这项研究的重点包括囊性纤维化、地中海贫血和杜氏肌营养不良症等疾病。利用 CRISPR-Cas9 进行基因治疗涉及编辑特定基因以纠正致病突变,从而开辟更有效治疗的可能性。然而,该技术的使用存在各种障碍,例如可能出现脱靶效应、伦理问题和长期安全性。然而,人们正在努力提高 CRISPR-Cas9 的特异性和准确性,以便开发有效的递送方法和提高安全性成为研究的主要重点。未来,CRISPR-Cas9 可能成为一种更具针对性和个性化的基因疗法,为在分子水平上治疗遗传疾病开辟机会,并为以前难以治疗的疾病提供替代疗法。此外,该技术还有可能早期预防遗传疾病并开发更实惠的基因疗法。跨学科合作是优化 CRISPR-Cas9 潜力的关键,以确保开发出符合伦理道德且有益于未来人类健康的遗传疾病疗法。关键词:CRISPR-Cas9,遗传病,基因编辑技术,基因治疗
来自Makurdi Metropolis选定市场出售的未经糊化牛奶的细菌分离株的细菌学评估。遗传疾病治疗基因治疗的进步
基因治疗是一种有前途的治疗策略,旨在用健康的基因修复或替代有缺陷的基因,以预防和治疗遗传疾病。有7000种影响全球超过3.5亿儿童的遗传疾病,而这些疾病中只有5%可以接受治疗。[1]。突破性事件在1990年代首次成功的临床试验和2012年Glybera的批准标志着[2]。基因疗法在治疗各种疾病,从肌肉营养不良和神经系统疾病到血液疾病和罕见遗传疾病方面显示出希望。通过传递故障基因的功能副本,这种方法具有治疗以前无法保育的条件的潜力[3]。近年来,通过成功的临床试验,精制媒介技术和其他复杂的输送系统,基因治疗已取得了迅速的进步。这表明基因疗法可以彻底改变医学。但是,基因治疗仍然面临着诸如高成本,监管障碍,道德问题,长期疗效和安全性等挑战[4]。本综述概述了基因疗法的最新进展,重点是批准的药物及其临床应用。该评论涵盖了各个医学领域的认可基因疗法的范围,包括罕见的遗传疾病,肿瘤学和遗传疾病。通过检查这些批准的疗法,我们旨在强调将基因疗法研究转化为临床实践的切实进步。
9。基因组和应用
近年来,随着基因组技术和分析方法的传播,遗传性遗传疾病以及各种癌症的差异诊断,预后的确定,该疾病的后果在开创性速度方面发展了发展。基因组方法,可快速,同时确定患者基因组中的遗传或体细胞突变,为更快地检测原始治疗目标铺平了道路。基因组分析方法包括整个基因组序列(WGS),整个外部布置(WES)和靶向排列以及整个转录序列(WTS)。可能与癌症和其他遗传疾病发展有关的许多突变和转录已通过诸如整个外部排列,整个基因组序列和所有转缩序列等方法确定。在多种突变共同促进的遗传疾病中,特殊设计的靶向基因面板在诊断和预后改善的背景下具有巨大的潜力。此外,通过超靶向的序列确定循环无DNA突变的是诊断遗传疾病,包括癌症,预后和对治疗反应的估计。通过基因组分析也可以使用有关Covid-19疾病对我们当前生活的临床重要信息。在本书部分中,它重点介绍了基因组方法在生物多样性领域的当前和潜在应用。近年来基因组方法中最突出的方法之一是通过CRISPR-CAS9进行的基因组调节,此方法的各种应用为遗传疾病和基因表征提供了机会。
婴儿癫痫痉挛综合征的遗传进步和精密医学的机会
摘要:婴儿癫痫痉挛综合征(IESS)是一种毁灭性的发育性癫痫发作(DEE)(DEE),由癫痫痉挛以及EEG上的一种或一种或停滞的发育回归或停滞或停滞的回归或停滞。无数的病因与IES的发展有关;从广义上讲,有60%的病例被认为是结构性,代谢或感染性的,其余的遗传或未知原因。癫痫遗传学是一个增长的领域,迄今为止已经发现了与IESS相关的28个拷贝数变体和70个单基因致病变异。虽然并不详尽,但一些最常见的遗传病因包括21三体和TSC1,TSC2,CDKL5,ARX,KCNQ2,STXBP1,STXBP1和SCN2A等基因中的病原变异。了解IES的遗传机制可能会提供更好的机会,以更好地识别IES的病理生理学并改善这种情况的治疗方法。这篇叙述性评论概述了我们目前对IES遗传学的理解,重点是IES发病机理的动物模型,IESS的遗传病因(即染色体疾病,单基因疾病,单核苷酸重复性疾病和三位核疾病和遗传疾病)的遗传学疾病及其遗传疾病以及他们的遗传疾病,以及他们的遗传疾病以及各种方法,以及他们的遗传疾病,以及他们的某些方法。与精密医学和癫痫遗传学有关的未来机会也探讨了IES的治疗。
生物多样性研究中心研究和保护Telangana国家生物多样性
入学申请分子和人类遗传学自我 - 学术会议的财务2024-2026最后日期,以提交填写和扫描的应用程序,向计划协调员,遗传疾病研究所,遗传疾病研究所,奥斯曼尼亚大学,贝格佩特大学,Hyderabad-500016是30.06.06.2024,均为30.06.2024。600/ - 最多10.07.2024。
BSC_CON_2.02基因测试:遗传疾病诊断的外显子组和基因组测序原始政策日期:2022年6月1日生效日期:MA
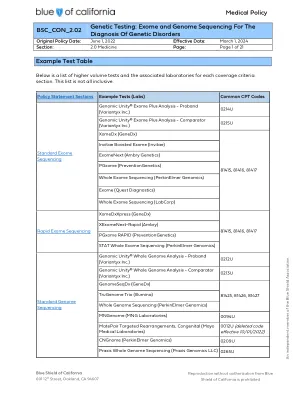
1。可用时至少有3代的完整家族史(或符号为何不符号)2。概率表3的完整详细描述。任何以前的基因检测结果(例如染色体微阵列/CMA,单基因或小面板)4。如果没有进行过以前的测试,则该成员的临床表现不符合良好描述的综合征,该综合征(例如,可以进行特定的测试(例如,单基因测试,CMA))5。外显子测试可能避免的任何侵入性测试6。为什么遗传病因可能是临床和历史发现II的可能解释。标准基因组测序(81425,81426,81427,0209U,0212U,0213U,0265U,0267U)被认为是研究的。iii。重复上述适应症的重复标准外显子组测序(不是重新分析*)可能是
托管护理和临床医生的见解,以优化不断变化的市场中遗传疾病的管理:AMCP市场见解的发现
表2:HTC卓越中心(COE)的国家电子调查(COE)在18个州的27个中心参加了出血障碍COE调查。 对四种co进行了调查和代表(基于大学,41%;独立设施,26%;综合递送系统,26%;儿童医院,15%),其中大多数(89%)报告了他们对血友病和von willebrand病的患者进行治疗,而von willbrand疾病的患者也大大减少了SCD(7%)和β-β-β-β-β-β-β-β-β-β-β-β-β-sp(4%)(4%)(4%)(4%)。表2:HTC卓越中心(COE)的国家电子调查(COE)在18个州的27个中心参加了出血障碍COE调查。对四种co进行了调查和代表(基于大学,41%;独立设施,26%;综合递送系统,26%;儿童医院,15%),其中大多数(89%)报告了他们对血友病和von willebrand病的患者进行治疗,而von willbrand疾病的患者也大大减少了SCD(7%)和β-β-β-β-β-β-β-β-β-β-β-β-β-sp(4%)(4%)(4%)(4%)。
遗传负担与Saguenay – Lac
摘要,位于魁北克省的Saguenay-Lac-Saint-Jean(SLSJ)地区是19世纪由17世纪从法国开始的连续移民浪潮颁发的19世纪的先驱者,一直持续到20世纪初。SLSJ群体的遗传结构被认为是三重创始人效应的产物,其特征是某些罕见的遗传疾病的患病率更高。进行了几项研究,以阐明当前SLSJ居民的历史,人口统计和遗传背景,以评估这些罕见疾病的起源及其在人群中的分布。由于开发了新的测序技术,确定了负责最普遍条件的基因和变体。结合了其他资源,例如BALSAC人口数据库,确定因果基因和允许评估某些创始人突变对人口健康的影响的致病变异,并根据运营商测试设计了基于运营商测试的Precision Medicine公共卫生策略。此外,它刺激了许多公共计划的建立。我们在这里报告了SLSJ地区的遗传疾病和创始人突变子集的审查和更新。数据是从已发表的科学来源收集的。这项工作扩大了有关这些罕见疾病的当前频率的知识,该人群中其他罕见遗传疾病的频率,对人群提供的携带者测试的相关性,以及当前的可用治疗方法以及有关这些遗传疾病的未来治疗方法的研究。