XiaoMi-AI文件搜索系统
World File Search System核酸适体在血液系统恶性肿瘤中的研究进展
摘要:目前,针对血液系统恶性肿瘤的研究十分深入,取得了许多突破性进展,其中基于适体的靶向治疗研究尤为突出。适体作为一种靶向工具,具有许多独特的优势(易合成、低毒性、易修饰、免疫原性低、纳米尺寸、稳定性高等),因此许多专家在各类血液系统恶性肿瘤的诊断和治疗中筛选相应的适体。本文试图总结并提供适体研究在血液系统恶性肿瘤诊断和治疗中的最新进展。到目前为止,在血液系统恶性肿瘤中已报道了29项适体研究,其中12个适体进行了体内测试,其余17个适体仅在体外测试。本案例中,11个适体与化疗药物联合用于血液系统恶性肿瘤的治疗,4个适体与纳米材料联合用于血液系统恶性肿瘤的诊断和治疗,还有一些研究利用适体进行siRNA和miRNA的靶向运输,达到靶向治疗的效果,这些研究为实现更靶向的目标提供了多种途径,这些发现为血液系统恶性肿瘤的基础和临床试验研究带来了光明和令人鼓舞的未来。
从诊断到死亡的结直肠和肛门恶性肿瘤的姑息治疗
在介绍(3)中。CRC是美国目前在所有性别中诊断出的第三种最常见的癌症类型(4)。自2000年以来,CRC的发病率在很大程度上下降,这在很大程度上是由于结肠镜检查改善了癌症筛查。但是,在过去的5年中,年轻人(25-45岁)的近端CRC癌症发生率有所增加(4)。这种增加的原因是许多研究的主题,但可能与突变,易感综合症和熟悉的CRC有关(5)。由于年轻人缺乏常规筛查,大多数在年轻人中被诊断出的癌症被诊断出来(6)。诊断时约有20%的CRC患者患有转移性疾病(7)。尽管成功治疗了原发性肿瘤,但另有20–30%的患者最终患有转移性疾病(5)。已经开发了较新的化学治疗剂以及靶向治疗。免疫检查点抑制剂已被证明在少数具有熟练不匹配修复疾病的患者中是有益的(8)。由于治疗疗法的改善,即使在疾病发生转移性的情况下,患者的疾病寿命更长(1)。尽管如此,寿命更长的患者在整个疾病过程中也有可能经历更多的身体和心理症状,这可能会对生活质量产生负面影响(QOL)(9)。治疗通常包括手术,遵循或进行化学疗法进行,以确保最佳治疗成功机会(1)。鉴于CRC患者的重大症状负担,广泛的发病率和死亡率,国家综合癌症网络(NCCN)指南建议该患者人群的姑息治疗(PC)早期整合(10,11)。转移性疾病患者通常接受姑息化疗治疗。转移切除术或局部疗法通常用于罕见病例,患者出现寡聚疾病或仅肝脏疾病(12)。转移性结肠癌的生存率正在改善,通常超过两年半(4)。
基于嵌合抗原受体的细胞疗法治疗 T 细胞恶性肿瘤
T 细胞恶性肿瘤可分为前体(T 急性淋巴细胞白血病/淋巴母细胞淋巴瘤,T-ALL/LBL)和成熟 T 细胞肿瘤,由 28 种不同的实体组成。这些恶性肿瘤大多具有侵袭性,预后较差。复发/难治性 (R/R) 疾病的预后尤其糟糕,进展后预期生存期仅为数月。靶向治疗,例如抗 CD30 免疫毒素 brentuximab vedotin、抗 CD38 抗体 daratumumab 和抗 CCR4 抗体 mogamulizumab 仅对部分 T 细胞肿瘤患者有效。嵌合抗原受体 T 细胞 (CAR-T) 通常用于治疗 R/R B 细胞恶性肿瘤,然而,它们在 T 细胞白血病和淋巴瘤中的应用存在一些特定的障碍,包括自相残杀、恶性细胞转染风险和 T 细胞发育不全。这些问题的解决方案依赖于靶抗原选择、CRISPR/Cas9 或 TALEN 基因编辑、CAR-T 表面抗原表达的翻译后调控和安全开关。使用基因编辑产品观察到染色体结构变化和基因表达的整体变化。我们在 www.clinicaltrials.gov 上注册了 49 项基于 CAR 的疗法研究。它们中的大多数以 CD30 或 CD7 抗原为目标。只有少数研究的结果可用。一般而言,临床反应率超过 50%,但报告的随访时间很短。 CAR 疗法的特定毒性,即细胞因子释放综合征 (CRS),似乎与目标抗原和制造细胞的来源有关。抗 CD7 CAR-T 细胞中的 CRS 比抗 CD30 细胞中更常见,但在大多数患者中症状较轻。在基因编辑的同种异体 CAR-T 细胞后观察到更严重的 CRS。免疫效应细胞相关神经毒性 (ICANS) 较轻且不常见。还观察到先前造血干细胞供体的同种异体 CAR-T 细胞后的移植物抗宿主病 (GvHD)。与抗 CD19 CAR-T 细胞类似,最常见的毒性是血细胞减少症。基于 CAR 的细胞疗法对于 T 细胞恶性肿瘤似乎是可行且有效的,然而,基于 CAR 的产品的最佳设计仍然未知,需要长期随访以评估其真正潜力。
尼沃单抗用于治疗晚期儿童恶性肿瘤
摘要。背景/目的:Nivolumab 是一种免疫检查点抑制剂,对特定肿瘤具有高抗肿瘤活性。本研究旨在评估 nivolumab 对患有各种类型高度恶性晚期肿瘤的儿科患者的疗效和安全性。患者和方法:研究纳入了 10 名患者,平均年龄为 15.1 岁。治疗指征为:恶性皮肤黑色素瘤(n=5)、脑肿瘤(n=2)、脑恶性黑色素瘤(n=1)、霍奇金淋巴瘤(n=1)和软组织肉瘤(n=1)。结果:4 名患者出现完全缓解。全组确诊后 24 个月的总生存率为 0.36。接受 nivolumab 和 ipilimumab 联合治疗的两名患者未达到缓解。10 名患者中有 4 名出现免疫治疗不良事件。结论:Nivolumab 是治疗儿童晚期肿瘤的有希望的选择
小儿恶性肿瘤患者的嗜铬细胞瘤敏感性TMEM127基因的完整性
抑制肿瘤基因TMEM127的种系突变发生在神经克雷斯特衍生的肿瘤中,炎性细胞瘤和paragangliomas(Qin等人 2010,Yao等。 2010,Neumann等。 2011),也已在肾细胞癌中检测到(Qin等人 2014)。 在其他恶性肿瘤中也突变出对嗜铬细胞瘤和肾脏癌的敏感性涉及的基因。 确定TMEM127突变是否也使影响小儿种群的癌症易感性,我们研究了TMEM127的完整性,其中155例18岁以下患者的155种癌症类型的样本中,包括16例胃肠道静脉曲菌样品,四个生殖线和12名患者,来自13名患者。 第二组涵盖了139名儿科患者的种系DNA,其中包括53例血液恶性肿瘤(39种急性淋巴淋巴性白血病,3个急性髓性白血病,五个霍奇金和6种非霍奇金的淋巴瘤,22个无霍夫金的淋巴瘤,22 cnseosarcoma the two consearsarcomamal two tt Two consemomans tt Two cns consomantomant( gliomas, one craniopharyngioma, one atypical teratoid rhabdoid tumor, and five with unspecified histology), 12 germ cell tumors, eight Ewing's sarcomas, six neuroblastic tumors, five Wilms' tumors, four retinoblastomas, three rhabdomyosarcomas, three liver tumors (two hepatoblastomas and one hepato-癌),一个滑膜肉瘤,一个brosarcoma,一种间皮瘤,一种肾上腺皮质癌,一个脱粘性肿瘤,一个非晶状体组织细胞增多症和一个原始的鼻弓类固有性质质肿瘤。 三名患者患有多个肿瘤。 2010)。 1)。 2010,Abermil等。 2012),也已经抑制肿瘤基因TMEM127的种系突变发生在神经克雷斯特衍生的肿瘤中,炎性细胞瘤和paragangliomas(Qin等人2010,Yao等。 2010,Neumann等。 2011),也已在肾细胞癌中检测到(Qin等人 2014)。 在其他恶性肿瘤中也突变出对嗜铬细胞瘤和肾脏癌的敏感性涉及的基因。 确定TMEM127突变是否也使影响小儿种群的癌症易感性,我们研究了TMEM127的完整性,其中155例18岁以下患者的155种癌症类型的样本中,包括16例胃肠道静脉曲菌样品,四个生殖线和12名患者,来自13名患者。 第二组涵盖了139名儿科患者的种系DNA,其中包括53例血液恶性肿瘤(39种急性淋巴淋巴性白血病,3个急性髓性白血病,五个霍奇金和6种非霍奇金的淋巴瘤,22个无霍夫金的淋巴瘤,22 cnseosarcoma the two consearsarcomamal two tt Two consemomans tt Two cns consomantomant( gliomas, one craniopharyngioma, one atypical teratoid rhabdoid tumor, and five with unspecified histology), 12 germ cell tumors, eight Ewing's sarcomas, six neuroblastic tumors, five Wilms' tumors, four retinoblastomas, three rhabdomyosarcomas, three liver tumors (two hepatoblastomas and one hepato-癌),一个滑膜肉瘤,一个brosarcoma,一种间皮瘤,一种肾上腺皮质癌,一个脱粘性肿瘤,一个非晶状体组织细胞增多症和一个原始的鼻弓类固有性质质肿瘤。 三名患者患有多个肿瘤。 2010)。 1)。 2010,Abermil等。 2012),也已经2010,Yao等。2010,Neumann等。2011),也已在肾细胞癌中检测到(Qin等人2014)。在其他恶性肿瘤中也突变出对嗜铬细胞瘤和肾脏癌的敏感性涉及的基因。确定TMEM127突变是否也使影响小儿种群的癌症易感性,我们研究了TMEM127的完整性,其中155例18岁以下患者的155种癌症类型的样本中,包括16例胃肠道静脉曲菌样品,四个生殖线和12名患者,来自13名患者。第二组涵盖了139名儿科患者的种系DNA,其中包括53例血液恶性肿瘤(39种急性淋巴淋巴性白血病,3个急性髓性白血病,五个霍奇金和6种非霍奇金的淋巴瘤,22个无霍夫金的淋巴瘤,22 cnseosarcoma the two consearsarcomamal two tt Two consemomans tt Two cns consomantomant( gliomas, one craniopharyngioma, one atypical teratoid rhabdoid tumor, and five with unspecified histology), 12 germ cell tumors, eight Ewing's sarcomas, six neuroblastic tumors, five Wilms' tumors, four retinoblastomas, three rhabdomyosarcomas, three liver tumors (two hepatoblastomas and one hepato-癌),一个滑膜肉瘤,一个brosarcoma,一种间皮瘤,一种肾上腺皮质癌,一个脱粘性肿瘤,一个非晶状体组织细胞增多症和一个原始的鼻弓类固有性质质肿瘤。三名患者患有多个肿瘤。2010)。1)。2010,Abermil等。2012),也已经从所有患者(已获得UTHSCSA和NIH IRB委员会批准)和TMEM127编码区的测序获得了知情同意,如前所述(Yao等人。检测到两个种系TMEM127错义变体:c。 67C O A,P.Leu23met,一种新型变体,在一个Ewing的肉瘤和C.268G O A,P.VAL90MET的患者中val90met变体以前已在嗜铬细胞中报道(Qin等人
小儿血液恶性肿瘤中Venetoclax组合疗法的最新更新
摘要:Venetoclax是一种强有效的B细胞淋巴瘤-2抑制剂(BCL-2),能够选择性地恢复癌细胞的凋亡潜力。已经证明,与免疫疗法,靶向疗法以及诸如甲基化剂(HMAS)或低剂量细胞酸酯(LDAC)等较低强度疗法结合使用,该药物可以改善成人急性髓样白血病(AML),慢性淋巴细胞瘤的成年患者的整体结果血液学恶性肿瘤,但其对小儿血液学的好处尚不清楚。随着许多临床前和临床试验的出现,最新的发现表明,在许多年轻患者中,即使经常导致严重的感染。研究旨在确定Bcl-2抑制剂在治疗原发性和难治性急性白血病中的活性,并结合标准和高剂量化学疗法。需要进行更多的研究来确定儿科人群的最佳基于威尼诺克拉抗体的方案及其对患者结局的长期影响,但它可能成为儿科肿瘤学的潜在治疗剂。
在T细胞恶性肿瘤中代谢重新布线的调节剂
褪黑激素(N-乙酰基-5-甲氧基氨胺)吲哚胺会发挥多割作用,并调节与昼夜节律,免疫调节和季节性繁殖有关的许多细胞途径和分子靶标,包括T细胞恶性期间的代谢复活。t细胞恶性肿瘤包含一组血液癌,其特征是恶性T细胞的生长和增殖。这些癌细胞表现出独特的代谢适应性,这是癌症的标志,因为它们可以重新连接其代谢途径,以满足恶性肿瘤所必需的能量需求和生物合成的增强,这是Warburg效应,其特征在于朝着糖酵解的转变,即使氧气也可以使用。此外,T细胞恶性肿瘤通过抑制丙酮酸酶脱氢酶激酶(PDK)而导致代谢转移,从而导致乙酰基COA酶产生和细胞糖酵解活性增加。此外,褪黑激素在负责营养摄取和代谢重新布线的必需转运蛋白(GLUT1,GLUT2)的表达中起调节作用,例如T细胞中的葡萄糖和氨基酸转运蛋白。这种调节显着影响T细胞的代谢性,因此影响了它们的分化。此外,已经发现褪黑激素调节参与T细胞激活的临界信号分子的表达,例如CD38和CD69。这些分子是T细胞粘附,信号传导和激活不可或缺的。本综述旨在提供有关褪黑激素抗癌特性机制,涉及在T细胞恶性肿瘤期间代谢的机理。本综述涵盖了致癌因子的参与,肿瘤微环境和代谢改变,标志,代谢重编程以及褪黑激素对各种癌细胞的抗核/癌症影响。
简报:胸部恶性肿瘤患者 SARS-CoV-2 疫苗接种率下降
由于免疫功能低下患者固有的风险因素以及初次接种疫苗后几个月内血清学反应减弱的表现,11 根据 FDA 于 2021 年 8 月 12 日、2021 年 9 月 22 日和 2022 年 3 月 29 日做出的授权,疾病控制中心 (CDC) 建议额外接种疫苗剂量,以给该患者群体提供最佳保护。值得注意的是,FDA 于 2021 年 8 月 12 日的授权是针对中度或重度免疫功能低下的个体,而对于什么构成足够的免疫抑制以符合条件的解释各不相同。在这里,我们试图调查过去一年中 242 名胸部恶性肿瘤患者对 SARS-CoV-2 疫苗接种的体液免疫反应和推荐额外剂量的给药率。
表征有效的paracaspase malt1抑制剂用于血液系统恶性肿瘤
在酶测定中测量了Schrodinger的MALT1抑制剂的效力。用于OCI-LY3和OCI-LY10细胞中的体外靶标参与测定法,通过使用MSD测定法(Messoscale discovery)测量了细胞裂解物中未溶解的BCL10的MALT1抑制剂24小时的浓度处理24小时。用于在OCI-LY3和OCI-LY10细胞中的细胞增殖测定法,用浓度的MALT1抑制剂处理96小时,然后用CellTiter-Glo分析(Promega)处理以测量细胞活力。
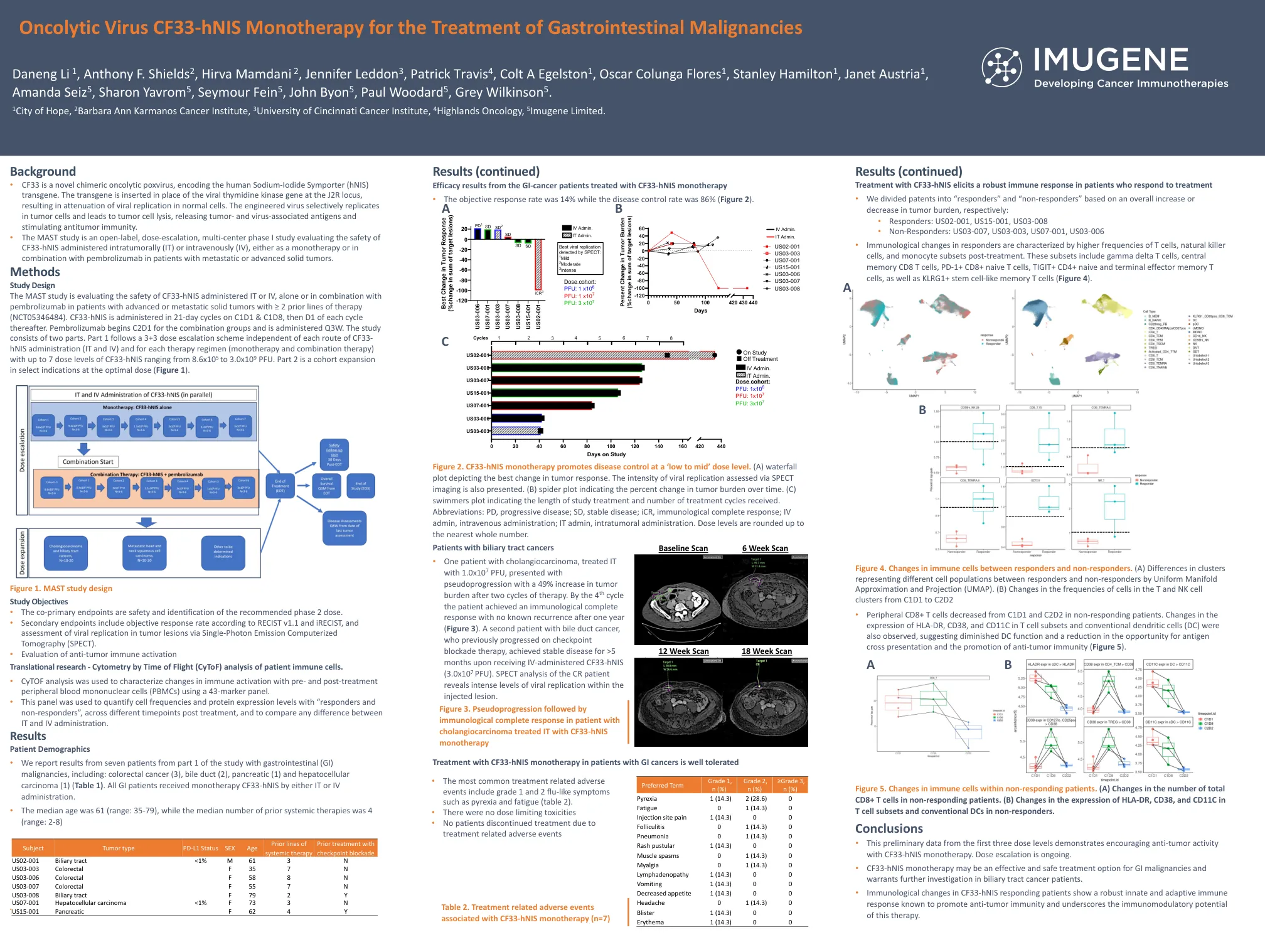
溶瘤病毒CF33-hNIS单一疗法治疗胃肠道恶性肿瘤
背景 • CF33 是一种新型嵌合溶瘤痘病毒,编码人类钠碘转运体 (hNIS) 转基因。转基因插入 J2R 基因座的病毒胸苷激酶基因位置,导致正常细胞中病毒复制减弱。工程病毒选择性地在肿瘤细胞中复制并导致肿瘤细胞裂解,释放肿瘤和病毒相关抗原并刺激抗肿瘤免疫。 • MAST 研究是一项开放标签、剂量递增、多中心 I 期研究,评估 CF33-hNIS 肿瘤内 (IT) 或静脉内 (IV) 给药的安全性,无论是作为单一疗法还是与派姆单抗联合用于转移性或晚期实体瘤患者。方法研究设计 MAST 研究正在评估 CF33-hNIS 单独或与帕博利珠单抗联合通过 IT 或 IV 给药的安全性,适用于既往接受过 ≥ 2 种治疗方案的晚期或转移性实体瘤患者(NCT05346484)。CF33-hNIS 在 C1D1 和 C1D8 以 21 天为一个周期给药,之后每个周期的 D1 给药。联合组的帕博利珠单抗从 C2D1 开始,每三周给药一次。该研究分为两部分。第 1 部分遵循 3+3 剂量递增方案,与每种 CF33- hNIS 给药途径(IT 和 IV)和每种治疗方案(单一疗法和联合疗法)无关,CF33-hNIS 剂量水平最多可达 7 个,范围从 8.6x10 5 至 3.0x10 9 PFU