XiaoMi-AI文件搜索系统
World File Search SystemCRISPR/Cas9技术消除慢性粒细胞白血病中的BCR/ABL1致癌基因并恢复正常造血
CRISPR/Cas9 技术可以消除慢性粒细胞白血病中的 BCR/ABL1 致癌基因,恢复正常造血。Elena Vuelta 1,2,3、Jose Luis Ordonez 1,4、Veronica Alonso-Perez 1,4、Lucia Mendez 3、Patricia Hernandez-Carabias 3、Raquel Saldana 5、Julian Seville 6、Elena Sebastian 6、Sandra Muntion 1,2,6,8、Fermin Sanchez-Guijo 1,2,6,8、Jesus Maria Hernandez-Rivas 2,4,7、Ignacio Garcia-Tunon 1,4* 和 Manuel Sanchez-Martin 2,3,4*。 *这些作者共同拥有高级作者身份。通信地址为:ignacio.tunon@usal.es; adolsan@usal.es
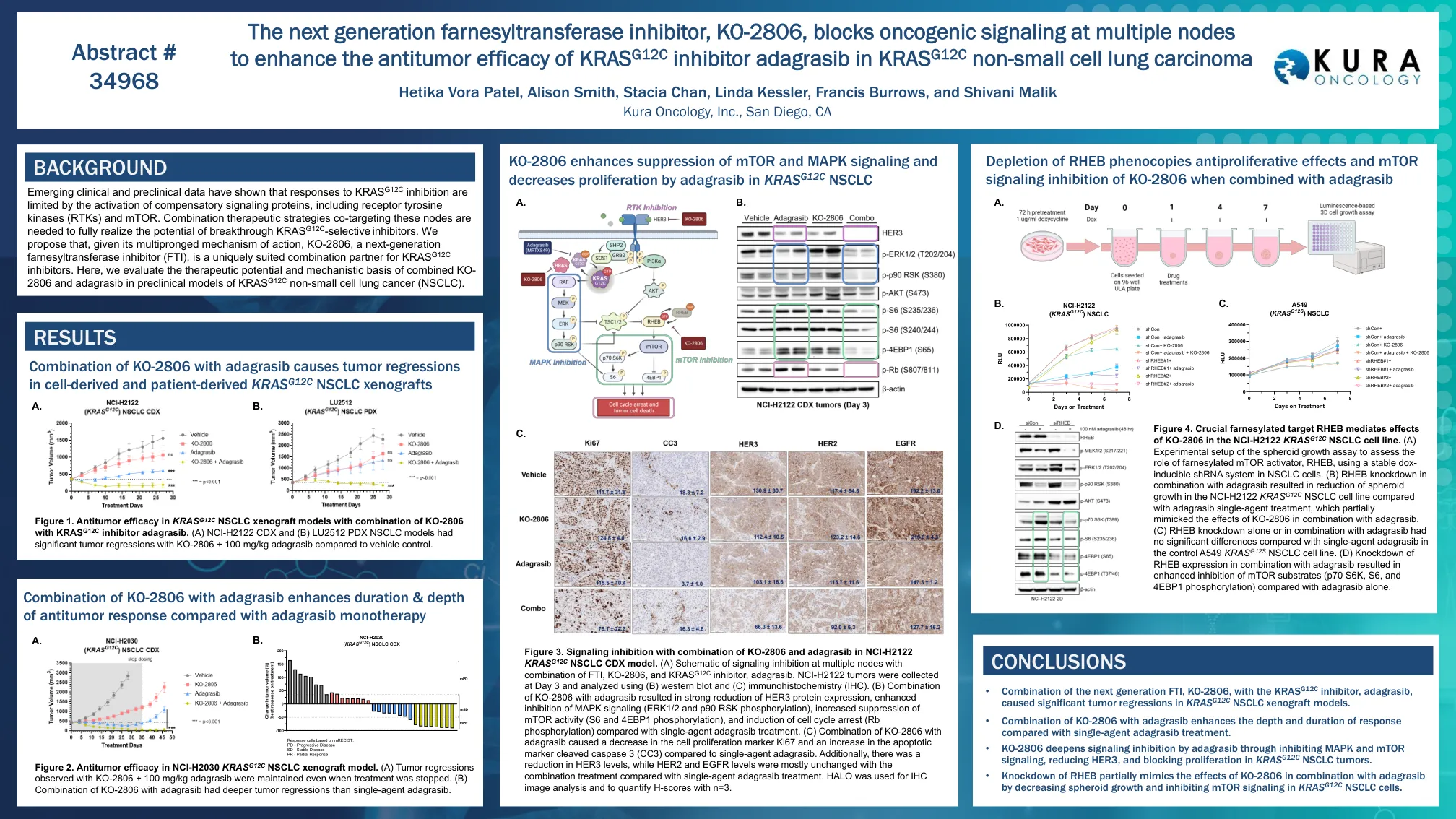
下一代Farnesylsylansferase抑制剂KO-2806,阻止多个节点的致癌信号传导,以增强KRAS G12的抗肿瘤功效
图3。NCI-H2122 KRAS G12C NSCLC CDX模型中KO-2806和Adagrasib结合使用的信号传导抑制。(a)在多个节点上抑制信号传导的示意图与FTI,KO-2806和KRAS G12C抑制剂Adagrasib的组合。NCI-H2122肿瘤,并使用(b)Western印迹和(c)免疫组织化学(IHC)分析。(b)KO-2806与AdagrasiB的组合导致HER3蛋白表达的大幅度降低,增强了对MAPK信号传导(ERK1/2和P90 RSK磷酸化)的抑制作用,增加了MTOR活性的抑制(S6和4EBP1磷酸化),以及对单个Cell Cycer Cyprant(RB Pranscratib)的抑制。(c)KO-2806与Adagrasib的组合导致细胞增殖标记Ki67的降低,而与单药adagrasib相比,凋亡标记裂解的caspase 3(CC3)的增加。此外,与单药Adagrasib治疗相比,HER3水平降低了,而HER2和EGFR水平的组合处理大多是没有变化的。halo用于IHC图像分析,并用n = 3量化H得分。
泛癌症分析揭示实体肿瘤中反复出现的 BCAR4 基因融合
摘要 ◥ 染色体重排通常会导致活性调控区域与致癌基因上游并列,从而产生表达的基因融合。共同的下游伴侣的反复激活(在患者群体中上游区域不同)表明其具有保守的致癌作用。对 32 种实体瘤类型的 9,638 名患者的分析显示,注释的长链非编码 RNA (lncRNA)——乳腺癌抗雌激素抗性 4 (BCAR4) 是 11 种癌症中最普遍、未表征的下游基因融合伴侣。使用具有内源性 BCAR4 基因融合的多种细胞系证实了其致癌作用。此外,在未转化的细胞系中过度表达临床上普遍存在的 BCAR4 基因融合足以诱导致癌表型。我们表明,所有基因融合的最小共同区域都包含一个驱动增殖所必需的开放阅读框。
水平指标 2.2:建筑和拆除废物和材料
根据欧盟废物框架指令,危险 CDW 是指具有附件 III(同一指令)所列的一种或多种危险特性的废物。2016 年欧盟建筑和拆除废物管理协议进一步将危险 CDW 定义为具有危险特性并可能对人类健康或环境造成危害的碎片。这包括受污染的土壤和疏浚弃土、可能包括粘合剂、密封剂和胶粘剂(易燃、有毒或刺激性)的材料和物质、焦油(有毒、致癌)、可吸入纤维形式的石棉基材料(有毒、致癌)、用杀菌剂、杀虫剂等处理过的木材(有毒、生态毒性、易燃)、卤化阻燃剂涂层(生态毒性、有毒、致癌)、含 PCB 的设备(生态毒性、致癌)、汞照明(有毒、生态毒性)、含 CFC 的系统、含 CFC 的绝缘材料、危险物质(溶剂、油漆、粘合剂等)的容器以及可能受污染废物的包装。
针对超级增强子复合物是一种很有前途的……
摘要:多种恶性肿瘤中均存在关键致癌基因的过度激活和过表达。近年来,超级增强子(SE)对致癌基因的异常激活机制引起了广泛关注。癌细胞中发生的一系列基因组变化(插入、缺失、易位和重排)可能产生新的SE,导致SE驱动的致癌基因过表达。SE由典型的增强子密集地负载介导复合物、转录因子和染色质调节剂组成,驱动与细胞身份和疾病相关的致癌基因的过表达。细胞周期蛋白依赖性蛋白激酶7(CDK7)和溴结构域蛋白4(BRD4)是与SE介导的转录相关的关键介导复合物。临床试验表明,针对SE的新兴小分子抑制剂(CDK7和BRD4抑制剂)对癌症治疗具有显著效果。越来越多的证据表明SE及其相关复合物在各种癌症的发展中起着关键作用。本文讨论了SE的组成、功能和调控及其对致癌转录的贡献。此外,还讨论了针对SE的创新治疗方法、其优缺点以及临床应用中的问题。研究发现,以SE为靶点可用于常规治疗并为癌症患者开辟更多治疗途径。
特刊 - 癌症中的MYC癌基因
Myc癌基因是肿瘤发生的关键驱动力,调节对癌细胞存活,增殖和代谢重编程必不可少的多种过程。其内在的致癌功能可实现不受控制的细胞生长,从而促进遗传不稳定性和对凋亡的抗性。除了这些细胞自主效应之外,MYC通过发挥免疫抑制作用而在塑造肿瘤微环境中起关键作用。通过MYC驱动的癌症利用机制,例如免疫抑制细胞因子分泌,调节免疫细胞的募集以及抗原表现的调节以逃避免疫监测。MYC功能的这种双重性强调了它作为内在的致癌途径的驱动力和癌症免疫景观的调节剂的重要性。针对MYC的治疗策略,包括间接抑制和免疫调节剂,代表了破坏其在肿瘤进展中的多方面作用的有希望的方法。了解MYC的致癌功能和免疫调节功能之间的相互作用对于开发靶向疗法以减轻其致癌潜力至关重要。
癌症治疗评论
识别分子致癌驱动因素对于精准肿瘤学至关重要。涉及和激活受体酪氨酸激酶 (RTK) 的基因重排(包括基因融合和基因扩增)在实体肿瘤中反复出现,尤其是在非小细胞肺癌中。检测这些变异的工具的进步加深了我们对潜在生物学和肿瘤特征的理解,并促使开发针对激活 RTK 的新型抑制剂。如今,约 15% 的肺腺癌中发现了可用药物治疗的致癌重排。然而,单独来看,这些变异的患病率都很低,这对它们的诊断提出了挑战。肺癌中新型可靶向致癌重排的识别和表征不断扩大,最近发现 0.4% 的肺腺癌中存在 CLIP1-LTK 融合就证明了这一点。虽然阻断 RTK 活性的酪氨酸激酶抑制剂通过改善这种疾病的预后代表了治疗领域的突破,但长期治疗不可避免地会导致获得性耐药性的产生。在这里,我们回顾了肺癌中涉及 RTK 的致癌融合和基因扩增。我们讨论了致癌 RTK 的遗传和分子结构以及诊断方法,强调了下一代测序技术的作用。此外,我们讨论了不同酪氨酸激酶抑制剂的治疗意义,包括当前的临床试验和导致获得性耐药性的机制。最后,我们概述了使用液体活检来监测疾病进程。
异常的非典型NF-κB信号传导重新编程表观基因组景观,以驱动多发性骨髓瘤的致癌转录组
AUV>作者:邮政信箱36067,圣胡安,波多黎各00936-5。 10027通讯作者:Annabell C. Segarra,博士,波多黎各大学医学院生理学系医学科学校园,邮政信箱365067,圣胡安,波多黎各00936-5067。电子邮件:787–758-2525分机。。
基因网络揭示了质量核心期间的干细胞状态收敛,并在多阶段皮肤致癌中发展为恶性肿瘤
在致癌过程中(11 - 13)。在小鼠中,已经鉴定出许多不同的干细胞标记,这些标记通过在上皮内重新室内隔室来促进体内平衡(14,15)。也已提出在正常皮肤中的某些干细胞在几种肿瘤类型(9,16)中充当癌症干细胞(CSC),以LGR5(17),LGR6(17),LGR6(18),Twist1(19),Sox2(Sox2(20)和Pitx1和Pitx1(21))。确定过渡期间出现的细胞塑性; 20
新兴的 RAS 导向癌症疗法
摘要 RAS 致癌基因是人类癌症中最常见的突变致癌基因,RAS 突变型癌症是人类疾病的主要负担。尽管这些致癌基因是几十年前发现的,但近年来人们对其结构和功能的了解取得了重大进展,包括不同亚型的治疗和预后意义。尽管在抑制 RAS 效应信号传导方面取得了一些成功,但针对这些突变的靶向性已被证明是困难的。最近,在试验环境中实现了直接 RAS 抑制。虽然这尚未转化为日常临床实践,但这一发展前景广阔。本综述总结了用于抑制 RAS 的各种方法,然后重点介绍了直接抑制 KRAS(G12C) 的最新进展。