机构名称:
¥ 1.0
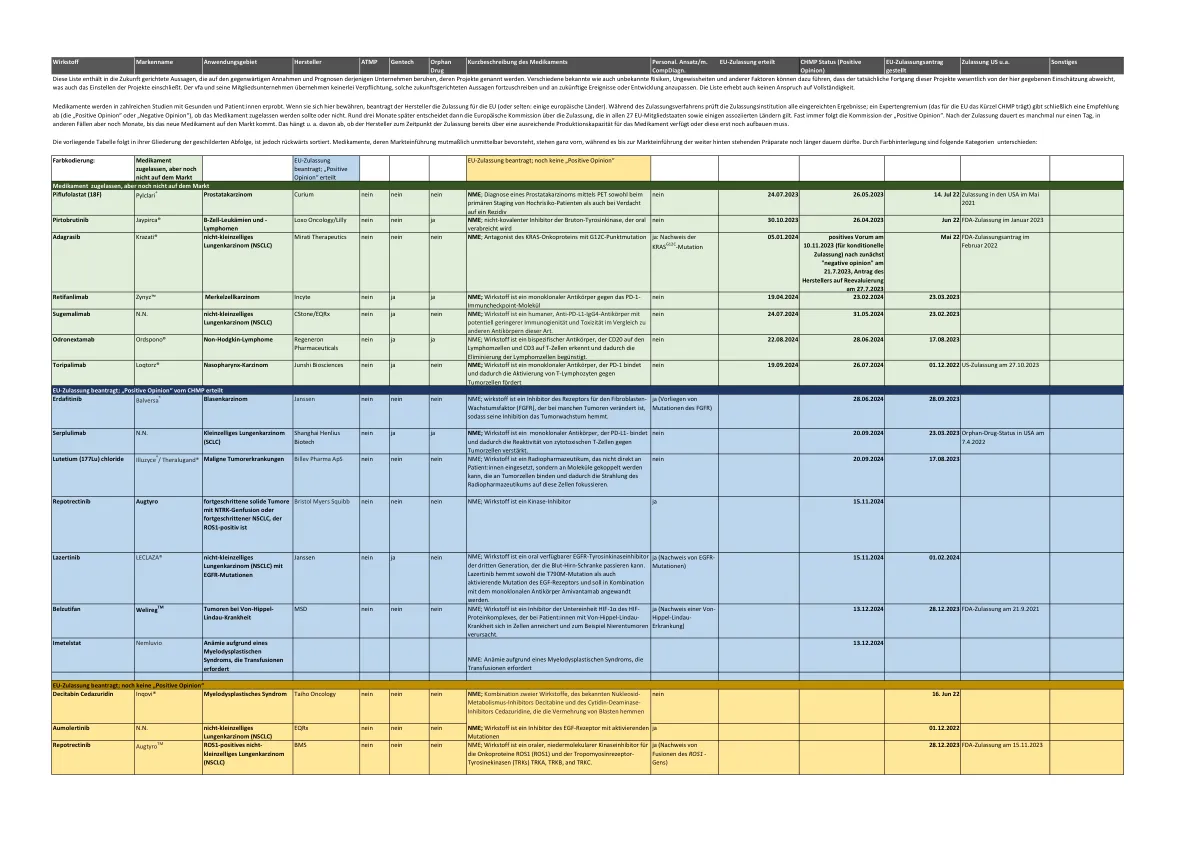
在与健康和患者的许多研究中测试了药物:内部。如果您在这里证明自己,制造商请求批准欧盟(或很少:某些欧洲国家)。在录取程序中,录取机构检查所有提交的结果;专家委员会(对欧盟的CHMP缩写)最终提出了是否应批准该药物的建议(“正面意见”或“否定意见”)。大约三个月后,欧洲委员会决定获得批准,该批准适用于所有27个欧盟成员国和一些相关国家。几乎总是遵循“积极意见”的委托。入院后,有时只需要一天,但是在其他情况下,新药物才能进入市场。取决于u。从制造商在批准时是否已经具有足够的药物生产能力。
krebs Medicinal.pdf