XiaoMi-AI文件搜索系统
World File Search System新西兰数据表 1. 产品名称
2. 定性和定量组成 JYNNEOS 是一种活疫苗,由改良的安卡拉-巴伐利亚北欧痘苗 (MVA-BN) 菌株产生,这是一种减毒的、非复制性正痘病毒。MVA-BN 在悬浮于不含直接动物来源物质的无血清培养基中的原代鸡胚成纤维细胞 (CEF) 中生长,从 CEF 细胞中收获,通过包括苯并酶消化在内的几个切向流过滤 (TFF) 步骤纯化和浓缩。每 0.5 mL 剂量配制成含有 0.5 x 10 8 至 3.95 x 10 8 个感染单位的 MVA-BN 活病毒,溶于 10 mM Tris(氨基丁三醇)、140 mM 氯化钠,pH 值为 7.7。每 0.5 mL 剂量可能含有残留的宿主细胞 DNA(≤ 20 mcg)、鸡蛋白(≤ 500 mcg)、Benzonase(≤ 0.0025 mcg)、庆大霉素(≤ 0.400 mcg)和环丙沙星(≤ 0.005 mcg)(见 4.3 节)。有关辅料的完整列表,请参阅 6.1 节。
2. 定性和定量组成
Vilda Denk 50 mg 2.定性和定量组成 活性物质:维格列汀 每片含50 mg维格列汀。 已知作用的辅料:每片含47 mg乳糖(无水)。有关辅料的完整列表,请参阅第 6.1 节。 3.剂型 片剂。白色至灰白色圆形扁平药片,一面刻有“VLD”。 4.临床特点 4.1治疗适应症 维格列汀适用于治疗成人2型糖尿病: 作为单一疗法,用于仅通过饮食和运动无法充分控制的患者,以及由于禁忌症或不耐受而不适合使用二甲双胍的患者。与二甲双胍联合作为双联口服疗法,适用于尽管使用二甲双胍单药治疗达到最大耐受剂量,但血糖控制仍不充分的患者;磺酰脲类药物;适用于尽管使用最大耐受剂量的磺酰脲类药物,但血糖控制仍不充分且由于禁忌症或不耐受而不适合使用二甲双胍的患者;噻唑烷二酮类药物;适用于血糖控制不足且适合使用噻唑烷二酮类药物的患者。当饮食和运动加上这些药物的双联疗法不能提供足够的血糖控制时,与磺酰脲类药物和二甲双胍联合作为三联口服疗法。当饮食和运动加上稳定剂量的胰岛素不能提供足够的血糖控制时,维达列汀也可与胰岛素(联合或不联合二甲双胍)联合使用。 4.2 用法用量和给药方法 用法用量 成人 单药治疗、与二甲双胍联合使用、与噻唑烷二酮联合使用、与二甲双胍和磺酰脲类药物联合使用或与胰岛素(联合或不联合二甲双胍)联合使用时,维格列汀的推荐日剂量为 100 毫克,早上服用一次 50 毫克,晚上服用一次 50 毫克。与磺酰脲类药物联合使用时,维格列汀的推荐剂量为早上服用一次 50 毫克。在这一患者群体中,每天服用 100 毫克维格列汀并不比每天服用 50 毫克维格列汀更有效。与磺酰脲类药物联合使用时,可考虑使用较低剂量的磺酰脲类药物以降低低血糖风险。不建议使用高于 100 毫克的剂量。
伤寒疫苗(Typhim Vi®、Vivotif®)
www.fda.gov/media/75988/download 。访问日期:2024 年 12 月 12 日。3. 伤寒 Vi 多糖疫苗(Typhim Vi )包装说明书 2020。可从以下网址获取:www.fda.gov/media/75993/download 。访问日期:2024 年 12 月 12 日。4. Kroger A、Bahta L、Long S、Sanchez P。免疫接种的一般最佳做法。可从以下网址获取:www.cdc.gov/vaccines/hcp/imz-best-practices 。访问日期:2024 年 12 月 12 日。5. CDC。黄皮书:国际旅行健康信息。2024 年。可从 https://wwwnc.cdc.gov/travel/page/yellowbook-home 获取。访问日期:2024 年 12 月 12 日。6. Collins J、Ryan E、Wong K 等人。霍乱疫苗:免疫实践咨询委员会的建议,2022 年。网址:www.cdc.gov/mmwr/volumes/71/rr/pdfs/rr7102a1-H.pdf。访问日期:2024 年 12 月 12 日。7. CDC。疫苗辅料摘要 2021 年。网址:
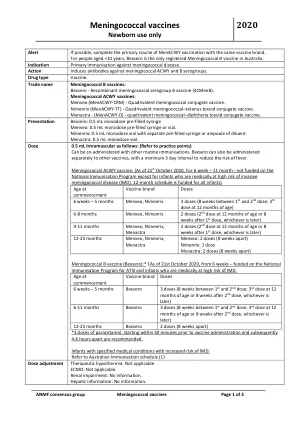
脑膜炎球菌疫苗 2020
Bexsero:26–41% 出现发热≥38°C,4–8% 发热≥39°C。体温通常在接种疫苗后 6 小时达到最高,第 2 天下降,第 3 天消退。其他不良反应:注射部位压痛、肿胀、硬结和红斑、烦躁、嗜睡、哭闹、食欲改变。 Menveo:不良事件发生频率与其他儿童疫苗相似。约 1% 出现发热。 Nimenrix:30–50% 出现轻微注射部位反应。约 20% 出现轻微全身反应。 Menactra:大多数反应是局部注射部位反应。 兼容性 不适用。 不兼容性 不适用。 稳定性 在注射前请勿从冰箱中取出。有效期见包装。 储存 储存在 2°C 至 8°C 的环境中。请勿冷冻。避光。储存应符合国家疫苗储存指南“争取 5 年”。辅料 Bexsero:氯化钠、组氨酸、蔗糖。 Nimenrix:蔗糖、氨丁三醇、0.9%氯化钠。 Menactra:氯化钠、磷酸氢二钠和磷酸二氢钠。 Menveo:蔗糖、天然橡胶、磷酸二氢钾、磷酸氢二钠和磷酸二氢钠、氯化钠。 特别说明
Nimenrix,A、C、W135 和 Y 群脑膜炎球菌结合疫苗
产品特性信息/产品特性摘要 1. 药品名称 Nimenrix ® - 预充注射器中的注射用粉末和溶剂 脑膜炎球菌 A、C、W-135 和 Y 群结合疫苗 2. 定性和定量组成 重构后,1 剂 (0.5 毫升) 含: A 群脑膜炎奈瑟菌多糖 1 5 微克 C 群脑膜炎奈瑟菌多糖 1 5 微克 W-135 群脑膜炎奈瑟菌多糖 1 5 微克 Y 群脑膜炎奈瑟菌多糖 1 5 微克 1 与破伤风类毒素载体蛋白结合 44 微克 有关辅料的完整列表,请参阅第 6.1 节。 3. 药物形式 注射用粉末和溶剂。粉末或粉饼呈白色。该溶剂清澈无色。 4. 临床特点 4.1 治疗指征 Nimenrix 适用于对6周龄及以上人群进行主动免疫,预防由A、C、W 135 和Y 群脑膜炎奈瑟菌引起的侵袭性脑膜炎球菌病。 4.2 用法用量 Nimenrix 应按照官方建议使用。初次免疫 6 周至 6 个月以下婴儿:2 剂,每剂 0.5 毫升,间隔 2 个月接种。 6个月以上婴儿、儿童、青少年及成人:一次给药0.5毫升。
Twinrix 成人,INN-甲型肝炎(灭活)和乙型肝炎(rDNA)(HAB)疫苗(吸附)
疫苗中可能含有制造过程中使用的微量新霉素(见第 4.3 节)。有关辅料的完整列表,请参阅第 6.1 节。 3. 剂型 注射用混悬液 不透明白色混悬液 4. 临床特点 4.1 治疗指征 Twinrix 成人版适用于无免疫力的成人和 16 岁以上有感染甲型肝炎病毒和乙型肝炎病毒风险的青少年。 4.2 用法用量 用法用量 对于 16 岁及以上的成人和青少年,建议剂量为 1.0 毫升。 - 基本免疫接种时间表 成人Twinrix疫苗的标准基本免疫接种包括三剂:第一剂在选定的免疫接种日接种,第二剂在第一次免疫接种后1个月接种,第三剂在第一次免疫接种后6个月接种。在特殊情况下,当预计在接种第一剂疫苗后一个月或更长时间进行旅行且没有足够时间遵循标准(0、1、6)疫苗接种时间表时,成人可以采用在第 0、7 和 21 天进行三次连续肌肉注射的时间表。使用此疫苗接种时间表时,建议在第一剂疫苗接种 12 个月后接种第 4 剂疫苗。
COVID-19 疫苗(灭活,佐剂)Valneva
1 武汉毒株 hCoV-19/Italy/INMI1-isl/2020 2 在 Vero 细胞(非洲绿猴细胞)上产生 3 吸附在氢氧化铝上(总共 0.5 mg Al 3 +),并总共用 1 mg CpG 1018(胞嘧啶磷酸鸟嘌呤)佐剂。 有关辅料的完整列表,请参阅第 6.1 节。 3. 剂型 注射用混悬液(注射剂) 白色至灰白色混悬液(pH 7.5 ± 0.5) 4. 临床特点 4.1 治疗适应症 COVID-19 疫苗(灭活,佐剂) Valneva 适用于主动免疫,以预防 18 至 50 岁人群中由 SARS-CoV-2 引起的 COVID-19。 该疫苗的使用应符合官方建议。 4.2 剂量和给药方法 剂量 主要系列 18 至 50 岁的个人 COVID-19 疫苗(灭活,佐剂)Valneva 以肌肉注射的方式给药,疗程为 2 剂,每剂 0.5 毫升。第二剂应在第一剂后 28 天注射(参见第 4.4 和 5.1 节)。目前没有关于 COVID-19 疫苗(灭活,佐剂)Valneva 与其他 COVID-19 疫苗互换以完成疫苗接种疗程的数据。已接种第一剂 COVID-19 疫苗(灭活,佐剂)Valneva 的个人应接种
产品特性总结
产品特性总结 1. 药品商品名 雷米普利-AC 2.5 mg 片剂 雷米普利-AC 5 mg 片剂 雷米普利-AC 10 mg 片剂 2. 定性和定量组成 雷米普利-AC 2.5 mg 每片含 2.5 mg 雷米普利。 RAMIPRIL-AC 5 毫克 每片含 5 毫克雷米普利。 RAMIPRIL-AC 10 毫克 每片含 10 毫克雷米普利。有关辅料的完整列表,请参阅第 6.1 节。 3.药物形式 雷米普利-AC 2.5毫克 双凸片,白色或近白色,直径6毫米,一面刻有“2.5”,另一面有凹口(不能分成两等份剂量)。 RAMIPRIL-AC 5毫克透镜状片剂,白色或近白色,直径7毫米,一面刻有“5”,另一面刻有2个垂直凹口(它们不具有分成两个相等剂量的作用)。 RAMIPRIL-AC 10 mg 双凸片,白色或近白色,直径9毫米,一面刻有“10”,另一面刻有2个垂直凹口(它们不具有分成两个相等剂量的作用)。 4. 临床资料 4.1.治疗指征- 治疗动脉高血压;
Vaxchora,霍乱疫苗(重组,活,口服)
该药物需要接受额外监控。这将有助于快速识别新的安全信息。要求医疗保健专业人员报告任何疑似不良反应。有关如何报告不良反应的信息,请参阅第 4.8 节。 1. 药品名称 Vaxchora 泡腾粉和口服混悬粉 霍乱疫苗(重组,活,口服) 2. 定性和定量组成 每剂疫苗含 4 × 10 8 至 2 × 10 9 个活霍乱弧菌活细胞,减毒菌株 CVD 103-HgR 1 。 1 利用重组 DNA 技术产生。这种药物含有转基因生物(GMO)。已知效果的赋形剂:每剂疫苗含有乳糖、蔗糖和 863 毫克钠。有关辅料的完整列表,请参阅第 6.1 节。 3. 药物形式泡腾粉和口服混悬粉。缓冲溶液为白色至灰白色粉末,活性物质为白色至米色粉末。 4 临床信息 4.1 治疗指征 Vaxchora 适用于对成人和 2 岁以上儿童进行针对 O1 血清群霍乱弧菌引起的疾病的主动免疫。该疫苗应按照官方建议使用。 4.2 剂量和给药剂量成人和 2 岁及以上的儿童应在可能接触霍乱弧菌 O1 组前至少 10 天进行单次口服给药。重新接种疫苗 目前没有关于重新接种疫苗间隔的数据。儿童人群
Vectormune FP ILT+AE;通用名:禽痘、禽传染性喉气管炎疫苗(活、重组)和禽脑脊髓炎疫苗(活)
1. 兽药名称 Vectormune FP ILT+AE 鸡用注射用冻干粉和悬浮液溶剂 2. 定性和定量组成 每剂(0.01 毫升)含: 活性物质: 表达膜融合蛋白和禽传染性喉气管炎病毒衣壳蛋白的活重组鸡痘病毒(rFP-LT) 2.7 至 4.5 log10 TCID50* 禽脑脊髓炎病毒,Calnek 1143 株(AE) 2.7 至 4.5 log10 EID50** * 50% 组织培养感染剂量 ** 50% 蛋感染剂量 有关辅料的完整列表,请参阅第 6.1 节。 3. 药物形式 注射用冻干粉和悬浮液溶剂。冻干粉:白褐色。溶剂:透明蓝色液体。 4.临床特点 4.1 适用物种 鸡 4.2 使用指征,指定适用物种 用于对8至13周龄的鸡进行主动免疫,以减少鸡痘引起的皮肤病变、禽传染性喉气管炎引起的临床症状和气管病变以及防止禽脑脊髓炎引起的产蛋损失。 免疫开始时间 鸡痘和禽传染性喉气管炎:接种后3周 禽脑脊髓炎:接种后20周 免疫持续时间: 鸡痘:接种后34周。 禽传染性喉气管炎和禽脑脊髓炎:接种后57周。 4.3 禁忌症 无。