机构名称:
¥ 1.0
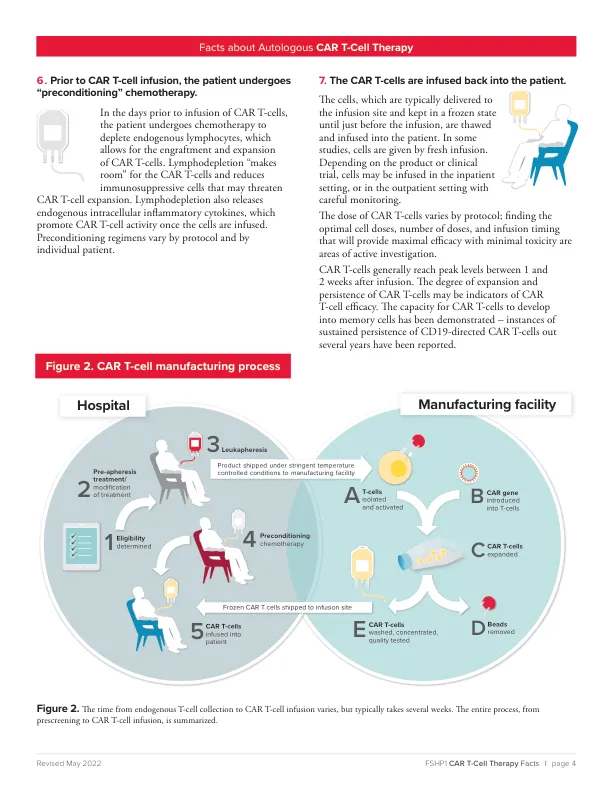
前两种自体 CAR-T 细胞疗法 tisagenlecleucel (Kymriah®) 和 axicabtagene ciloleucel (Yescarta®) 于 2017 年获得美国食品药品管理局批准。2020 年,FDA 批准了 brexucabtagene autoleucel (Tecartus TM )。Lisocabtagene maraleucel (Breyanzi®) 和 idecabtagene vicleucel (Abecma®) 于 2021 年获得批准。Ciltacabtagene autoleucel (Carvykti TM ) 于 2022 年 3 月获得批准。这些产品和其他目前正在开发的产品要投入临床实践,需要各方充分了解在癌症患者中使用这些个性化“活”生物制剂的技术和医疗管理。本出版物将解释 CAR T 细胞疗法背后的原理,描述已批准的疗法,总结迄今为止的疗效结果,详细说明已出现的重大风险,提供实用的医疗管理信息,并强调该疗法预期融入临床实践所涉及的一些独特挑战。
关于嵌合抗原受体 (CAR) T 细胞的事实...