机构名称:
¥ 1.0
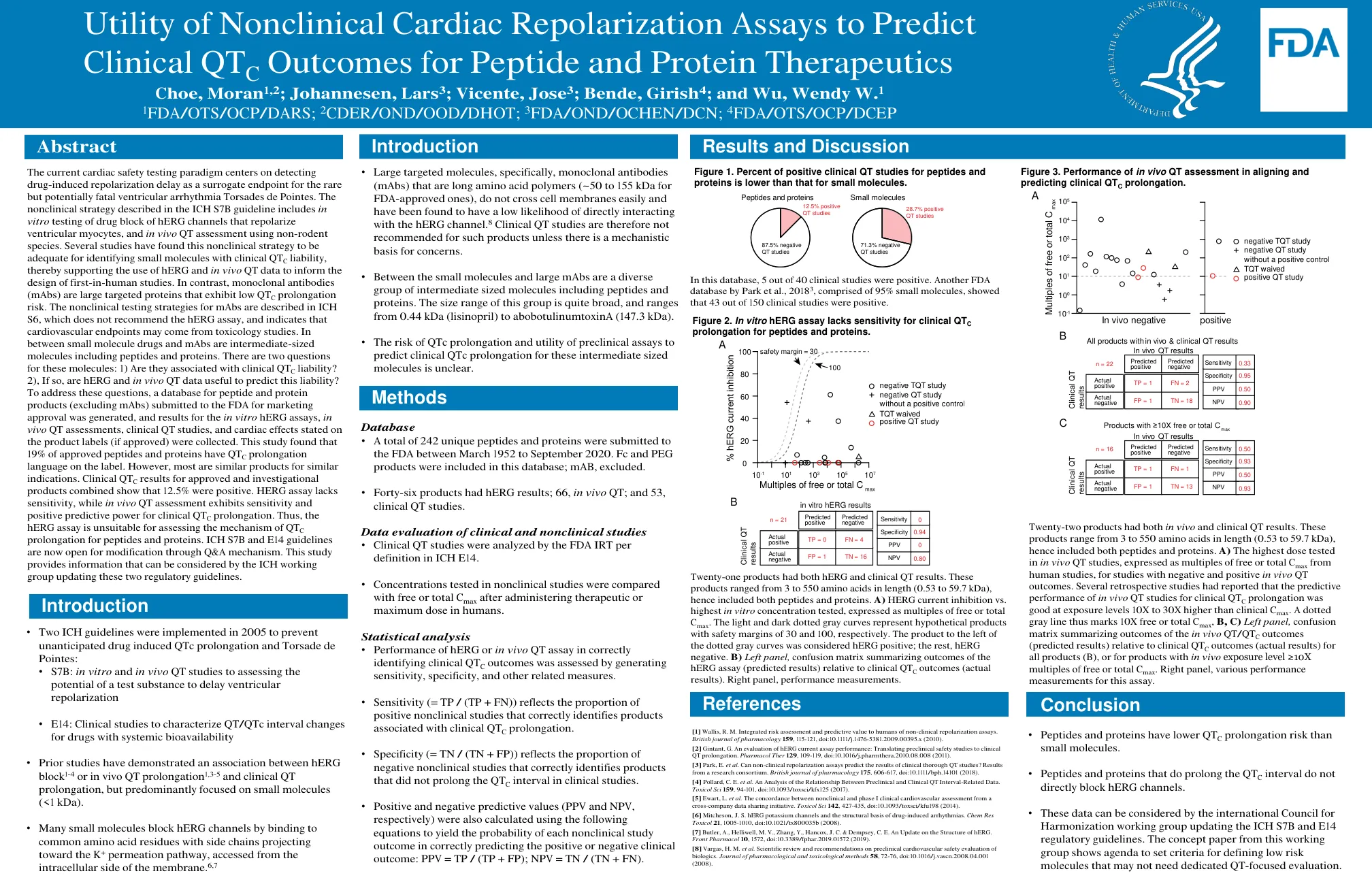
当前的心脏安全性测试范例以检测药物引起的复极延迟为中心,将其作为罕见但可能致命的室性心律失常尖端扭转型室性心动过速的替代终点。ICH S7B 指南中描述的非临床策略包括体外测试药物阻断 hERG 通道以复极心室肌细胞,以及使用非啮齿动物进行体内 QT 评估。多项研究发现,这种非临床策略足以识别具有临床 QT C 倾向的小分子,从而支持使用 hERG 和体内 QT 数据来指导首次人体研究的设计。相比之下,单克隆抗体 (mAb) 是表现出低 QT C 延长风险的大型靶向蛋白。ICH S6 中描述了 mAb 的非临床测试策略,它不推荐 hERG 检测,并表明心血管终点可能来自毒理学研究。小分子药物和 mAb 之间是中等大小的分子,包括肽和蛋白质。对于这些分子,有两个问题:1) 它们是否与临床 QT C 倾向有关?2) 如果是,hERG 和体内 QT 数据是否有助于预测这种倾向?为了回答这些问题,我们生成了提交给 FDA 以获得上市批准的肽和蛋白质产品(不包括 mAb)的数据库,并收集了体外 hERG 检测、体内 QT 评估、临床 QT 研究和产品标签上注明的心脏影响(如果已获批准)的结果。这项研究发现,19% 的获批肽和蛋白质在标签上有 QT C 延长的语言。但是,大多数是用于类似适应症的类似产品。已获批产品和研究产品的临床 QT C 结果综合显示 12.5% 为阳性。HERG 检测缺乏敏感性,而体内 QT 评估对临床 QT C 延长表现出敏感性和阳性预测力。因此,hERG 检测不适合评估肽和蛋白质的 QT C 延长机制。 ICH S7B 和 E14 指南现已开放通过问答机制进行修改。本研究提供的信息可供 ICH 工作组在更新这两项监管指南时参考。
肽和蛋白质治疗的成果
主要关键词