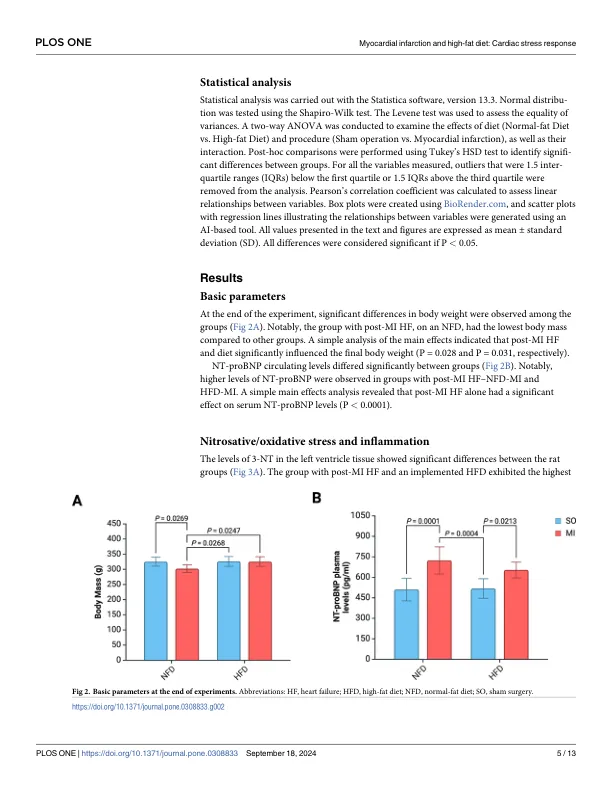
心肌梗死 (MI) 是世界范围内的重要死亡原因 [1]。由于现代治疗选择,MI 的死亡率一直在下降,MI 幸存者的数量也在不断增加 [2]。其中许多人随后出现心力衰竭 (HF) 的症状 [3,4]。心肌细胞因缺血死亡后,HF 的发展与不良的左心室重塑有关,导致功能丧失 [5,6]。高脂饮食 (HFD) 可通过心脏肥大、心肌细胞凋亡和间质纤维化等机制加剧 MI 后的重塑 [7,8]。实验研究表明,HFD 显著加剧老年大鼠的高血压心脏病,导致心房和心室重塑恶化以及相关的左心室收缩功能受损 [9]。此外,仅 12 周的 HFD 就会对心脏功能产生不利影响,这通过左心室斑点追踪成像 [10] 进行测量,该参数能够检测亚临床左心室。不幸的是,最近的临床研究表明,人类高脂肪产品的消费量一直在稳步增加 [11]。在 HF 的背景下,人们对亚硝化/氧化应激、炎症和内质网应激进行了很多讨论 [12-15]。然而,对于 HFD 对 HF 中这些过程的影响知之甚少。亚硝化/氧化应激是指当氧代谢紊乱时,一氧化氮 (NO) 和活性氧物质之间的生化反应。该过程导致活性氮物质 (如过氧亚硝酸根阴离子) 的产生,从而导致蛋白质硝化和损伤 [16]。这种损伤的标志是 3-硝基酪氨酸 (3-NT) [17]。一氧化氮合酶 (NOS) 催化一氧化氮的产生,一氧化氮合酶有三种亚型:诱导型一氧化氮合酶 (iNOS)、内皮型一氧化氮合酶 (eNOS) 和神经元型一氧化氮合酶 (nNOS) [18]。这些亚型在心血管健康和疾病中发挥着至关重要的作用。iNOS 在正常心脏组织中的表达水平非常低 [19]。炎症会导致 iNOS 活化和过表达,这会对心脏造成有害影响,而转基因动物中 nNOS 和 eNOS 的过表达会改善心肌梗死后的心脏功能 [20]。髓过氧化物酶 (MPO) 在炎症反应中起着至关重要的作用 [21]。它主要在中性粒细胞和单核细胞中表达。MPO 催化产生次氯酸,一种强效氧化剂 [22]。此外,这种蛋白质还可以直接参与活性氮物质的形成。循环中 MPO 水平升高与炎症和氧化应激有关 [ 23 ]。此外,最近的荟萃分析表明 MPO 可作为 HF 诊断的有价值标志物 [ 24 ]。当错误折叠或未折叠的蛋白质压倒内质网(内质网是蛋白质折叠和脂质生物合成的关键细胞器)时,就会发生内质网应激。如前所述,亚硝化/氧化应激会影响蛋白质折叠过程并导致内质网应激 [ 25 , 26 ]。后者会激活未折叠蛋白反应 (UPR),这是一种复杂的信号网络,旨在恢复蛋白质稳态或在不可能的情况下促进细胞凋亡。该过程在
心脏内质网应激和未折叠蛋白
主要关键词