机构名称:
¥ 1.0
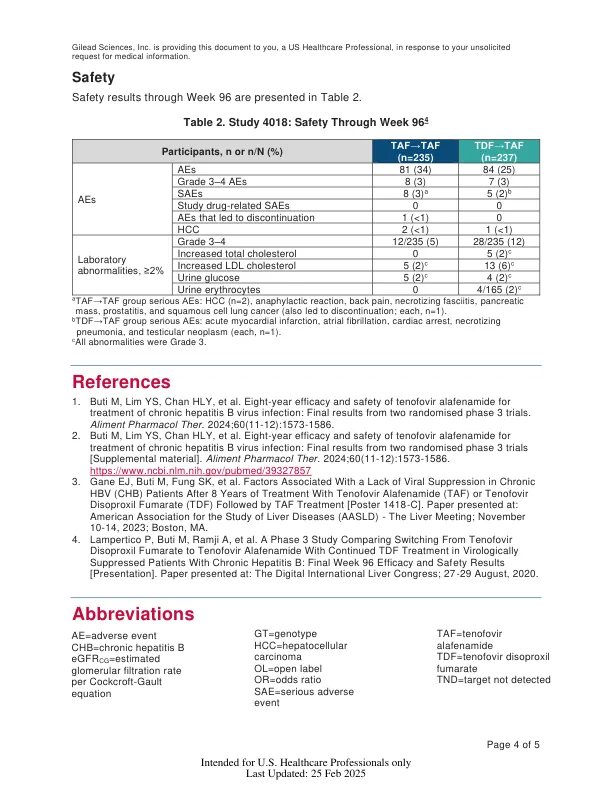
研究108和110是第三阶段临床试验,它们比较了TFF与TDF在主要核(T)IDE-IDE参与者中的疗效和安全性。共有1298名成人,单感染CHB和补偿肝功能的参与者以2:1的比例随机分配,以接收双盲TAF 25 mg或TDF 300 mg。完成盲人阶段后,两个臂的合格参与者都被招募到OL阶段并接受了TAF。在研究过程中,参与者接受了以下治疗方法之一:双盲,然后OL TAF总计8年(TAF8Y),双盲TDF 2年,然后OL TAF 6年(TDF2Y→TAF6Y)或Double Blblind TDF 3年,然后持续3年,然后OL TAF持续5年(TDF3Y→TDAF5Y)。1
vemlidy®持久性病毒症